
2011-veres-Zaklyuchne--Biohimiya
.pdf11
В ензиматичних реакціях, молекули, що вступають в перетворення, називають субстратами, які згодом перетворюються в інші молекули, котрі називають продуктами.
Більшість всіх процесів у біологічній клітині потребують ензимів для їх проходження з підвищеною швидкістю.
Оскільки ензими вибірково каталізують реакції з певними субстратами, то підвищується тільки кілька реакцій серед інших можливих, а такий набір ензимів визначає метаболічний шлях у клітині.
Більшість ензимів є набагато більшими за субстрат і тому вони діють тільки своєю малою частиною (біля 3–4 амінокислот) у каталітичному процесі.
Область, на якій зосереджені ―активні‖ залишки амінокислот, зв'язує субстрат і там проходить відповідна реакція. Таку область називають активним сайтом.
Ензими також мають місця – сайти, які зв'язують кофактори, що необхідні для каталізу.
Деякі ензими також мають зв'язувальні сайти для малих молекул, часто прямих чи непрямих продуктів або ж субстратів каталізованої реакції.
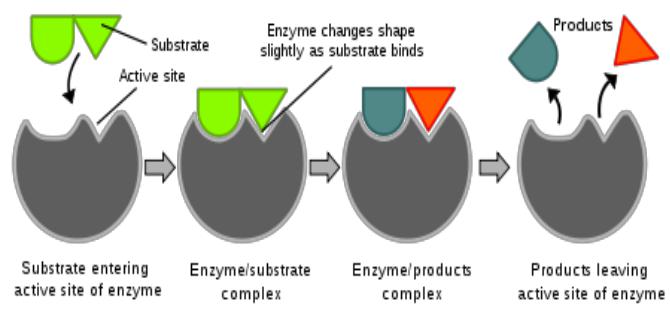
―Замок і ключ" модель за лауреатом Нобелівської премії, хіміком-органіком Еміль Фішером у 1894.
У 1958, Даніель Кошланд запропонував модифікацію до моделі замок-ключ.
Діаграми, що представляють дію ферменту

16
Як всі каталізатори, ензими працюють зі зниженням енергії активації (Ea) реакції, що таким чином сильно підвищує швидкість її.
Внаслідок цього продукти утворюються швидше і реакція швидше досягає відповідної рівноваги.
Реакції, каталізовані ензимами, відбуваються в мільйон раз швидше, за
реакції без них. Наприклад:
(у тканинах; висока CO2 концентрація)
(в легенях; низька CO2 концентрація)
17
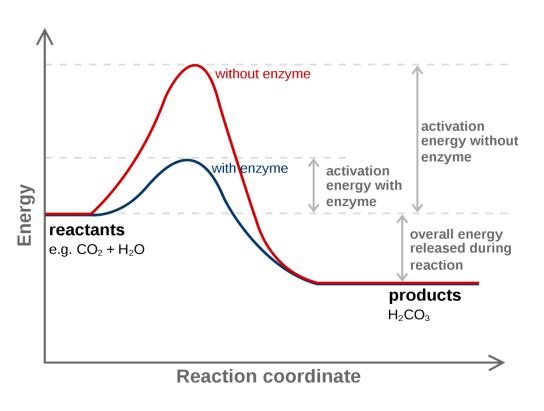
Енергетичні етапи хімічної реакції. Субстратам потрібно багато енергії, щоб досягнути переходу для перетворення в продукти. Ензим стабілізує стан переходу, знижуючи енергію, необхідну для утворення продуктів.
18
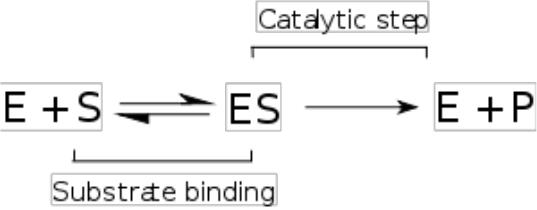
Механізм для односубстратної ензимної реакції. Ензим (E) зв'язує субстрат (S) внаслідок чого утворюється продукт (P).
19
Міжнародна спілка біохімії і молекулярної біології розробила номенклатура для ензимів, КФ; кожний ензим описується послідовністю 4-х чисел, представлених ―КФ".
Перше число представляє клас ензиму, який базується на механізмі реакції.

20
ЕС або КФ (класифікація ферментів)
КФ 1 Оксидоредуктази: каталізують реакції окислення/відновлення
CH3CH2OH + NAD+
(CH3)CHO + NADH + H+
оксидоредуктаза (алкогольдегідрогеназа)
КФ 2 Трансферази: переносять функціональні групи (наприклад, метильну чи фосфатну групу)
Глюкоза + ATФ
Глюкоза-6-фосфат + AДФ
трансфераза (гексокіназа)
21
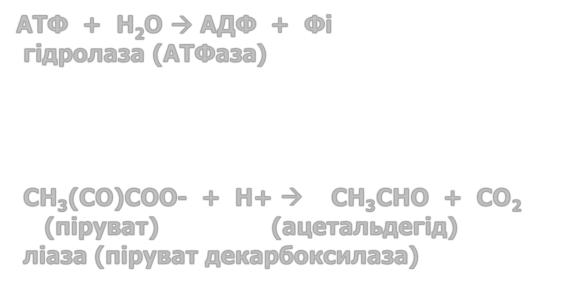
КФ 3 Гідролази: каталізують гідроліз різних зв'язків
ATФ + H2O AДФ + Фi
гідролаза (АТФаза)
КФ 4 Ліази: розрізають різні зв'язки, відмінні від таких як гідроліз і окислення
CH3(CO)COO- + H+ CH3CHO + CO2 |
|
(піруват) |
(ацетальдегід) |
ліаза (піруват декарбоксилаза)
22
КФ |
5 |
Ізомерази: |
каталізують |
|
ізомеризацію в межах однієї молекули |
||||
-OOC |
H |
|
H |
H |
| |
| |
|
| |
| |
C = C |
|
C = C |
||
| |
| |
|
| |
| |
H |
COO- |
|
-OOC |
COO- |
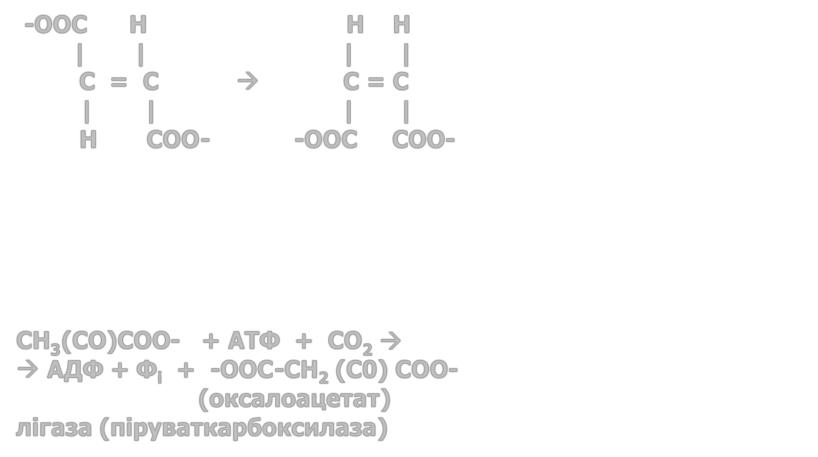
ізомераза (малеат ізомераза)
КФ 6 Лігази: об'єднують дві молекули з ковалентними зв'язками.
CH3(CO)COO- + ATФ + CO2
AДФ + Фi + -OOC-CH2 (C0) COO-
(оксалоацетат) лігаза (піруваткарбоксилаза)
