
- •История кафедры факультетской и госпитальной хирургии Кубанского государственного медицинского университета. Основные направления деятельности кафедры.
- •Николай Николаевич Петров – первый заведующий кафедрой факультетской и гос-питальной хирурги КубГму, академик рамн, Герой Социалистического Труда. Периоды жизненного и профессионального пути.
- •Видеолапароскопическая хирургия. Оборудование, обезболивание. Показания и противопоказания при ургентных заболеваниях органов брюшной полости.
- •Видеолапароскопическая хирургия. Преимущества и недостатки. Основные группы видеолапароскопических операций.
- •Значение видеолапароскопии в диагностике и лечении хирургической патологии. Техническое оснащение и основные этапы операции.
- •Эндоскопическая хирургия через естественные отверстия тела (notes). Преимуще-ства и недостатки.
- •Видеоторакоскопическая хирургия. Основные виды операций. Преимущества и не-достатки. Отличия от лапароскопической методики.
- •Использование робототехники в мини-инвазивной хирургии. Основные виды ис-пользуемых роботов.
- •Эндоваскулярная хирургия при ибс, митральных пороках, стенозах магистральных артерий.
- •Внесосудистая малоинвазивная хирургия в лечении заболеваний печени, желчевыводящих путей и поджелудочной железы.
- •Ретроградная холангиопанкреатография. Показания к исследованию, возможные ошибки и осложнения.
- •Эндоскопические методы диагностики и лечения внутрипротоковой патологии при заболеваниях желчевыводящих путей. Показания к эндоскопической папиллосфинк-теротомии.
- •Значение, виды и результаты лучевых методов обследования больных при острых заболеваниях органов брюшной полости.
- •Отграниченные жидкостные скопления (абсцессы, кисты, серомы, гематомы). При-чины их возникновения. Клиника, диагностика, современные методы лечение.
- •Синдром системной реакции организма на воспаление (sirs). Этиология, патогенез, клиника, диагностика, лечение.
- •Диффузный токсический зоб: этиология, патогенез, клиника, диагностика, лечение.
- •Эндемический и спорадический зоб: этиология, патогенез, клиника, диагностика, лечение.
- •Тиреоидиты (острый, подострый, аутоиммунный, фиброзный): этиология, патогенез, клиника, диагностика, лечение.
- •Рак щитовидной железы: этиология, патогенез, классификация по системе тnm, клиника, диагностика. Принципы хирургического лечения, заместительная терапия.
- •Абсцессы и флегмоны шеи: этиология, патогенез, клиника, диагностика, лечение.
- •Маститы (острый и хронический, специфический и неспецифический): этиология, патогенез, клиника диагностика, лечение.
- •Дисгормональные заболевания молочной железы (мастопатии): этиология, патогенез, клиника, диагностика, лечение.
- •Доброкачественные образования молочных желез (фиброаденома, аденома, папил-лома, липома, галактоцеле): этиология, патогенез, клиника, диагностика, лечение.
- •Рак молочной железы: классификация, клиника, диагностика, принципы лечения.
- •Химические ожоги и рубцовые сужения пищевода: этиология, патогенез, клиника, диагностика, лечение, профилактика.
- •Травматические повреждения пищевода. Этиология, клиника, диагностика, лечение.
- •Дивертикулы пищевода: классификация, этиология, патогенез, клиника, диагности-ка, лечение.
- •Рак пищевода: классификация, клиническое течение в зависимости от локализации, диагностика, методы оперативного лечения.
- •Травма груди. Определение, этиология, патогенез, классификация, методы диагно-стики. Симптомы повреждения груди (общие, местные, специфические). Основные принципы лечения.
- •Пневмоторакс. Определение, этиология, патогенез, классификация, диагностика, ле-чение.
- •Гемоторакс. Определение, этиология, патогенез, классификация, диагностика, лече-ние.
- •Травматические повреждения трахеи и бронхов: этиология, классификация, клиника диагностика, лечение.
- •Травматические повреждения легких: этиология, классификация, клиника, диагно-стика, лечение.
- •Травматические повреждения сердца: этиология, классификация, клиника, диагно-стика, лечение.
- •Бронхоэктатическая болезнь: этиология, патогенез, классификация, клиника, диа-гностика, лечение.
- •Абсцесс и гангрена легкого: классификация, этиология, патогенез, клиника, диффе-ренциальная диагностика, лечение.
- •Острая эмпиема плевры: классификация, патогенез, клиника, диагностика, принци-пы лечения.
- •Хроническая эмпиема плевры: этиология, клиника, диагностика, принципы лечения. Виды торакопластик.
- •Центральный рак легкого: классификация, клиника, диагностика, принципы лече-ния.
- •Периферический рак легкого: классификация, клиника, диагностика, принципы ле-чения.
- •Топография и функции диафрагмы. Травматические повреждения диафрагмы: этио-логия, классификация, клиника, диагностика, лечение.
- •Диафрагмальные грыжи: этиология, классификация, клиника, диагностика, лечение.
- •Травматические диафрагмальные грыжи: этиология, классификация, диагностика, лечение.
- •Грыжи пищеводного отверстия диафрагмы, клинико-рентгенологическая классифи-кация. Аксиальные грыжи: этиология, патогенез, клиника, диагностика, осложнения, принципы хирургического лечения.
- •Грыжи пищеводного отверстия диафрагмы, клинико-рентгенологическая классифи-кация. Параэзофагеальные грыжи: этиология, патогенез, клиника, диагностика, осложнения, принципы хирургического лечения.
- •Истинные грыжи слабых мест диафрагмы (грыжи Ларрея, Морганьи, Богдалека): этиология, патогенез, клиника, диагностика, лечение.
- •Релаксация диафрагмы: этиология, патогенез, клиника, диагностика, лечение.
- •«Острый живот»: определение, этиология, основные клинические симптомы, дифференциальная диагностика, принципы лечения.
- •Приобретенные паховые грыжи: этиология, патогенез, классификация, клиника, ди-агностика, методы хирургического лечения.
- •52. Скользящие наружные грыжи живота: этиология, патогенез, клиника, диагностика, особенности оперативного лечения.
- •53. Этиология и патогенез бедренных грыж. Клиника, диагностика, методы хирургиче-ского лечения.
- •54. Пупочные грыжи у взрослых: этиология, клиника, диагностика, методы хирургиче-ского лечения.
- •55. Грыжи белой линии живота. Анатомические предпосылки их образования. Клиника, диагностика, лечение.
- •56. Диастаз прямых мышц живота. Этиология, патогенез, клиника, диагностика, прин-ципы хирургического лечения.
- •57. Послеоперационные и рецидивные вентральные грыжи: классификация, этиология, патогенез, клиника, диагностика, методы хирургического лечения.
- •58. Осложнения грыж брюшной стенки: воспаление, невправимость, копростаз, ущем-ление. Определение понятий, клиника, диагностика, лечение.
- •60. Флегмона грыжевого мешка: клиника, диагностика, особенности хирургического лечения.
- •61. Травматические повреждения желудка и двенадцатиперстной кишки. Этиология, патогенез, классификация, клиника, диагностика, хирургическая тактика.
- •62. Синдром Меллори-Вейса: этиология, патогенез, клиника, диагностика, лечение.
- •Виды оперативных вмешательств при язвенной болезни желудка и дпк. Понятие об органосохраняющей хирургии язвенной болезни. Классификация оперативных вмешательств.
- •64. Ваготомия в хирургии язвенной болезни желудка и двенадцатиперстной кишки, ее виды. Дренирующие операции на желудке.
- •65. Язвенные гастродуоденальные кровотечения: патогенез, клиника, диагностика, классификация по степени тяжести кровопотери. Консервативное лечение и виды оперативных вмешательств.
- •67. Перфоративные гастродуоденальные язвы: классификация, клиника, диагностика, виды оперативных вмешательств.
- •68. Пенетрация язвы желудка и двенадцатиперстной кишки. Определение понятия. Этиология, патогенез, клиническая картина, диагностика, лечение.
- •69. Язвенный пилородуоденальный стеноз: патогенез, классификация, клиника, диагно-стика, лечение. Показания к операции и виды оперативных вмешательств.
- •70. Острые гастродуоденальные язвы и эрозии: этиология, патогенез, клиника, диагно-стика лечение.
- •71. Синдром Золингера-Эллисона: этиология, патогенез, классификация, клиника. Особенности хирургического лечения в зависимости от типа заболевания.
- •72. Демпинг-синдром: этиология, патогенез, классификация, клиника, диагностика, ле-чение, профилактика.
- •73. Синдром приводящей петли после операций на желудке: этиология, патогенез, клас-сификация, клиника, диагностика, лечение, профилактика.
- •74. Рецидив пептической язвы желудка и двенадцатиперстной кишки: этиология, пато-генез, клиника, диагностика, лечение, профилактика.
- •75. Постваготомические осложнения: этиология, патогенез, клиника, диагностика, лечение, профилактика.
- •76. Предраковые заболевания желудка. Гастрит, полипы и полипоз желудка, хрониче-ская язва желудка. Клиника, диагностика, роль гастроскопии и биопсии, лечение.
- •77. Рак желудка: этиология, патогенез, классификация, клиника, диагностика, лечение.
- •78. Абсцессы печени (бактериальные, паразитарные). Этиология, патогенез, клиника, диагностика, современные методы лечения.
- •2. Вскрытие и дренирование полости абсцесса.
- •79. Эхинококкоз печени. Этиология, патогенез, клиника, диагностика, осложнения, ле-чение.
- •80. Доброкачественные новообразования печени: этиология, патогенез, клиника, диа-гностика, лечение.
- •81. Злокачественные опухоли печени: этиология, патогенез, клиника, диагностика, лече-ние.
- •82. Синдром портальной гипертензии. Этиология, патогенез, клиника, диагностика. Ме-тоды консервативного и хирургического лечения.
- •Воздействие на источник кровотечения
- •Воздействие на свертывающую систему крови.
- •По распространенности:
- •По характеру повреждающего агента
- •86. Закрытая травма живота: Определение, этиология, классификация, клиника, методы диагностики, хирургическая тактика.
- •87. Открытая травма (ранения) живота: Определение, этиология, классификация, кли-ника, методы диагностики, хирургическая тактика.
- •1 Этап:
- •2 Этап:
- •3 Этап:
- •92. Местные послеоперационные осложнения. Определение, этиология, клиника, диа-гностика. Способы лечения и профилактики.
- •93. Общие послеоперационные осложнения. Определение, этиология, клиника, диагно-стика. Способы лечения и профилактики.
- •94. Травматические повреждения желчного пузыря и желчевыводящих путей. Этиоло-гия, патогенез, классификация, клиника, диагностика, хирургическая тактика.
- •95. Желчнокаменная болезнь. Этиология, патогенез камнеобразования, клиника, диа-гностика, лечение.
- •96. Осложнения желчнокаменной болезни (холедохолитиаз, рубцовый стеноз бдс, про-тяженные стриктуры протоков). Патогенез, клиника, диагностика, лечение.
- •97. Острый калькулезный холецистит. Этиология патогенез, классификация, клиника диагностика, лечение. Виды хирургических вмешательств.
- •98. Осложнения острого калькулезного холецистита (подпеченочный абсцесс, перито-нит, эмпиема желчного пузыря). Патогенез, клиника, диагностика, лечение.
- •99. Хронический калькулезный холецистит. Этиология патогенез, клиника диагностика, лечение. Виды хирургических вмешательств.
- •Показания и виды наружного дренирования желчных путей.
- •102. Механическая желтуха. Этиология, патогенез, клиника, дифференциальная диагно-стика. Принципы консервативного и хирургического лечения.
- •103. Постхолецистэктомический синдром. Определение понятия, классификация, клини-ка, диагностика, лечение.
- •104. Рак желчного пузыря и желчевыводящих путей. Факторы, способствующие разви-тию. Клиника, диагностика, дифференциальная диагностика, лечение.
- •105. Травматические повреждения поджелудочной железы. Этиология, патогенез, клас-сификация, клиника, диагностика, хирургическая тактика.
- •106. Острый панкреатит. Этиология, патогенез, классификация, клиника, диагностика, лечение. Хирургическая тактика при остром панкреатите на современном этапе.
- •107. Хронический панкреатит. Этиология, патогенез, классификация, клиника, диагно-стика, принципы лечения. Виды оперативных вмешательств.
- •108. Кисты поджелудочной железы. Этиология, патогенез, классификация, клиника, диа-гностика, лечение.
- •109. Свищи поджелудочной железы. Этиология, патогенез, классификация, клиника, ди-агностика, лечение.
- •110. Рак поджелудочной железы. Этиология, патогенез, классификация, клиника, диагно-стика. Виды радикальных и паллиативных хирургических вмешательств.
- •111. Травматические повреждения селезенки. Этиология, патогенез, классификация, клиника, диагностика, хирургическая тактика.
- •112. Инфаркты и абсцессы селезенки. Этиология, патогенез клиника, диагностика, лечение.
- •113. Кисты селезенки. Классификация, клиника, диагностика, лечение. Роль малоин-вазивных хирургических вмешательств на современном этапе в лечении кист селе-зенки.
- •114. Топография средостения. Острый медиастинит. Этиология, патогенез, классификация, клиника, диагностика, лечение.
- •115. Хронический медиастинит. Этиология, патогенез, классификация, клиника, диагно-стика, лечение.
- •116. Перикардиты: этиология, клиника, диагностика, лечение.
- •117. Аневризма брюшной аорты: этиология, патогенез, клиника, диагностика, хирургическая тактика.
- •118. Артериальные тромбозы и эмболии: этиология, клиника, диагностика, лечение.
- •119. Варикозная болезнь нижних конечностей: этиология, патогенез, классификация по системе сеар, клиника, диагностика. Методы консервативного и оперативного лечения.
- •120. Посттромбофлебитическая болезнь нижних конечностей: этиология, патогенез, классификация, клиника, диагностика. Методы консервативного и оперативного ле-чения.
- •121. Диабетическая ангиопатия нижних конечностей: этиология, патогенез, классификация, клиника, диагностика, принципы лечения.
- •122. Облитерирующие заболевания артерий нижних конечностей. Классификация забо-леваний, клиника, дифференциальная диагностика, лечение. Профилактика.
- •123. Облитерирующий атеросклероз нижних конечностей: клиника, диагностика, лече-ние. Профилактика.
- •124. Острые нарушения мезентериального кровообращения: этиология, патогенез, классификация, клиника диагностика, лечение.
- •125. Тромбофлебиты и флеботромбозы: классификация, клиника, диагностика, лечение. Профилактика венозных тромбозов в послеоперационном периоде.
- •126. Тромбоэмболические осложнения в послеоперационном периоде. Профилактика. Характеристика тромбоопасных больных.
- •1. Нефракционированный гепарин
- •2. Низкомолекулярные гепарины
- •1. Общехирургические операции
- •127. Тромбоэмболия легочной артерии у хирургических больных: этиология, диагностика, лечение, профилактика.
- •128. Острый аппендицит: этиология, патогенез, классификация, клиника, диагностика, лечение.
- •129. Аппендикулярный инфильтрат: классификация, особенности диагностики и хирургической тактики.
- •130. Осложнения острого аппендицита: этиология, патогенез, классификация, диагно-стика, лечение.
- •131. Внутрибрюшные осложнения после аппендэктомии: клиника, лечение, профилактика.
- •132. Острый аппендицит у стариков и беременных: особенности диагностики и хи-рургической тактики.
- •133. Хронический аппендицит: этиология, патогенез, классификация, диагностика, лечение.
- •134. Травматические повреждения тонкой и толстой кишки. Этиология, патогенез, классификация, клиника, диагностика, хирургическая тактика.
- •135. Травматические повреждения сосудов забрюшинного пространства. Этиология, патогенез, классификация, клиника, диагностика, хирургическая тактика.
- •136. Предраковые заболевания толстой кишки: клиника, диагностика, лечение.
- •137. Хронический колостаз: этиология, патогенез, клиника, диагностика, лечение.
- •138. Болезнь Крона: этиология, патогенез, классификация, клиника, диагностика, ле-чение.
- •139. Неспецифический язвенный колит: классификация, патогенез, клиника, диагно-стика, лечение.
- •140. Дивертикулы и дивертикулез толстой кишки: клиника, диагностика, осложнения. Показания к хирургическому лечению.
- •141. Полипы и полипоз ободочной кишки: классификация, диагностика, хирургическая тактика.
- •142. Рак правой половины ободочной кишки: осложнения, виды и выбор метода опера-тивного вмешательства.
- •143. Рак левой половины ободочной кишки: классификация, клиника, диагностика, лечение.
- •144. Геморрой: этиология, патогенез, классификация, клиника, диагностика, лечение. Профилактика заболевания.
- •145. Трещины прямой кишки: причины возникновения, классификация, клиника, диагно-стика, лечение. Профилактика заболевания.
- •146. Острые парапроктиты: классификация, этиология, клиника, диагностика, лечение. Профилактика.
- •147. Прямокишечные свищи: классификация, клиника, диагностика, лечение. Профи-лактика.
- •148. Рак прямой кишки: классификация, клиника, диагностика, виды хирургических вмешательств.
- •149. Кишечные свищи: классификация, клиника, лечение. Профилактика заболевания.
- •150. Панариций: этиология, классификация, клиника, диагностика, лечение. Профилак-тика заболевания.
- •151. Флегмоны кисти: этиология, патогенез, классификация, клиника, диагностика, лечение. Профилактика заболевания.
- •152. Рожистое воспаление: этиология, классификация, клиника, диагностика, лечение. Профилактика заболевания.
- •153. Сепсис: этиология, патогенез, классификация, клиника, диагностика, лечение.
- •154. Принципы предоперационной подготовки и послеоперационного ведения больных с сахарным диабетом.
- •155. Интракорпоральные и экстракорпоральные методы детоксикации организма у хирургических больных.
- •157. Странгуляционная кишечная непроходимость. Этиология, патогенез, классифика-ция, диагностика. Виды хирургического лечения. Показания к резекции кишки.
- •158. Обтурационная кишечная непроходимость. Этиология, патогенез, классификация, диагностика. Виды хирургического лечения.
- •159. Спаечная кишечная непроходимость. Этиология, патогенез, диагностика. Виды хирургического лечения.
- •160. Инвагинация кишечника. Определение понятия. Виды инвагинации. Этиология, патогенез, клиника, диагностика. Виды хирургического лечения.
- •161. Динамическая кишечная непроходимость (паралитическая, спастическая). Этиология, патогенез, клиника, диагностика, лечение.
- •165. Флегмоны забрюшинного пространства. Причины. Клинические проявления, диа-гностика, современный подход к лечению гнойных заболеваний тканей забрюшинного пространства.
- •167. Показания к трансплантации печени. Реабилитация больных в послеоперационном периоде.
- •168. Показания к трансплантации сердца. Иммунологические основы подбора донорских органов.
- •169. Приобретенный митральный стеноз. Этиология, патогенез, стадии заболевания, клиника, диагностика, лечение.
- •170. Приобретенная митральная недостаточность клапана. Этиология, патогенез, стадии заболевания, клиника, диагностика, лечение.
- •171. Приобретенный аортальный стеноз. Этиология, патогенез, стадии заболевания, кли-ника, диагностика, лечение.
- •172. Приобретенная аортальная недостаточность клапана. Этиология, патогенез, стадии заболевания, клиника, диагностика, лечение.
- •173. Хроническая ишемическая болезнь сердца. Этиология, патогенез, классификация по nyha, клиника, диагностика. Принципы хирургического лечения.
- •174. Аневризма сердца. Этиология, патогенез, клиника, диагностика. Принципы хирур-гического лечения.
- •175. Коарктация аорты. Этиология, патогенез, клиника, диагностика, лечение.
- •176. Кровезаменители: классификация по механизму действия, показания к применению в хирургической практике.
- •177. Переливание крови в хирургии: показания и противопоказания, компоненты и пре-параты крови. Методы определения групп крови и резус-фактора.
- •178. Правила переливания крови и ее компонентов. Оформление документации при ге-мотрансфузиях.
- •179. Реинфузия и аутогемотрансфузия в хирургии: показания, методика выполнения.
- •180. Гемотрансфузионные реакции и осложнения: классификация, клиника, лечение, профилактика.
161. Динамическая кишечная непроходимость (паралитическая, спастическая). Этиология, патогенез, клиника, диагностика, лечение.
Паралитическая непроходимость кишечника обусловлена значительным угнетением или даже полным прекращением перистальтической активности кишечника, ослаблением тонуса мышечного слоя кишечной стенки. Отсутствие пропульсивной перистальтической волны обусловливает застой содержимого в кишечнике. Наиболее часто паралитический илеус наблюдается у больных с перитонитом. Основной причиной является воспаление, ишемия стенки кишки, нарушение функции ауэрбахова и мейснерова нервных сплетений в стенке кишки.
Клиническая картина и диагностика. Основными симптомами являются тупые, распирающие боли, рвота, стойкая задержка стула и отхождения газов, вздутие живота. Боли, как правило, постоянные, не имеют четкой локализации и иррадиации, схваткообразный компонент обычно отсутствует.
По сравнению с механической кишечной непроходимостью рвота при динамической непроходимости наблюдается реже, хотя при развитии перитонита она может быть многократной.
Живот равномерно вздут, пальпаторно определяют резистентность брюшной стенки. При аускультации перистальтические шумы ослаблены или отсутствуют.
Если паралитическая непроходимость не сочетается с перитонитом, то в первые часы заболевания общее состояние больного остается удовлетворительным. В последующем, при отсутствии патогенетической терапии, состояние ухудшается, нарастают симптомы эндогенной интоксикации, гиповолемии, выраженных расстройств водно-электролитного баланса, кислотно-основного состояния, возникает полиорганная недостаточность жизненно важных органов.
Отдельную тяжелую группу составляют те виды паралитической непроходимости, которые возникают в связи с острыми нарушениями кровообращения в мезентериальных сосудах (тромбозы и эмболии верхнебрыжеечной артерии — см. "Заболевания периферических артерий").
При обзорной рентгеноскопии живота наблюдается равномерное вздутие всех отделов кишечника, преобладание в раздутой кишке газообразного содержимого над жидким, наличие горизонтальных уровней жидкости как в тонкой, так и в толстой кишке одновременно.
Лечение. В первую очередь необходимо устранить патологический процесс, приведший к развитию паралитической непроходимости кишечника. Для восстановления моторной функции кишечника и устранения его пареза применяют аминазин, снижающий угнетающее действие на перистальтику симпатической нервной системы, антихолинэстеразные препараты (прозерин, убретид), активирующие перистальтику путем усиления влияния парасимпатической нервной системы на контрактильную функцию кишечника, клизму через 30—40 мин после введения препаратов.
Необходима определенная последовательность в использовании этих препаратов. Вначале вводят аминазин или аналогичные ему лекарственные средства, через 45—50 мин — прозерин, затем назначают очистительную клизму. Эффективна также электростимуляция кишечника. В последние годы появились новые препараты — прокинетики (цисаприд и его производные), применяемые для стимуляции моторной деятельности кишечника.
Больным проводят постоянную декомпрессию желудка и кишечника путем аспирации с помощью назоеюнального зонда, устанавливаемого в просвет тощей кишки с помощью эндоскопа.
Нарушения гомеостаза корригируют по общим принципам лечения больных с выраженными метаболическими нарушениями при различных этиологических факторах (острая непроходимость кишечника, перитонит, деструктивный панкреатит и т. п.).
Хирургическое лечение при паралитической непроходимости кишечника показано лишь в случаях возникновения ее на фоне перитонита, тромбоза или эмболии брыжеечных сосудов.
Спастическая непроходимость кишечника — сравнительно редкий виддинамической непроходимости. Затруднение или полное прекращение продвижения кишечного содержимого обусловлено возникновением стойкого спазма мышечного слоя стенки кишки. Длительность спазма может быть различная — от нескольких минут до нескольких часов.
Клиническая картина и диагностика. Ведущим симптомом являются сильные схваткообразные висцеральные боли без определенной локализации. В период схваток больной мечется по кровати, кричит.
Диспепсические расстройства нехарактерны. Задержка стула и газов наблюдается не у всех больных, она редко бывает стойкой. Общее состояние больного нарушается незначительно. Живот имеет чаще обычную конфигурацию, если же брюшная стенка втянута, то он принимает ладьевидную форму.
При обзорной рентгеноскопии живота выявляют спастически атоническое состояние кишечника. Иногда по ходу тонкой кишки видны мелкие чаши Клойбера, расположенные цепочкой по ходу брыжейки тонкой кишки. При контрастном исследовании пищеварительного тракта с барием определяют замедленный пассаж бариевой взвеси по тонкой кишке, четкообразные участки вздутия кишечника.
Лечение. Обычно применяют только консервативное лечение. Больным назначают спазмолитические средства, физиотерапевтические процедуры, тепло на живот; проводят лечение основного заболевания.
162. Перитониты, определение понятия. Классификация перитонитов (по характеру развития, распространенности, виду экссудата). Патогенетические стадии, клиническая картина, диагностика. Принципы лечения.
Перитонит - локальная (источник), регионарная (брюшина), системная воспалительная реакция организма на развитие деструктивного и инфекционного процесса в органах живота, сопровождающаяся развитием абдоминального сепсиса с полиорганной дисфункцией.
КЛАССИФИКАЦИЯ
По этиологическому фактору:
первичный (спонтанный перитонит у детей и взрослых, тубер-кулёзный);
вторичный (вызванный перфорацией и деструкцией органов брюшной полости, послеоперационный, посттравматический);
третичный (персистирующий или вялотекущий).
По распространённости:
отграниченный (инфильтрат или абсцесс);
неотграниченный:
местный (занимает менее 3 из 9 анатомических областей брюшной полости)
распространённый (занимает 3 и более анатомические области брюшной полости).
По характеру патологического содержимого в полости брю-шины:
серозный;
серозно-фибринозный;
фибринозно-гнойный;
гнойный;
каловый;
геморрагический;
химический.
По микробиологическому фактору:
неспецифический, обусловлен микроорганизмами желудочно-кишечного тракта:
- аэробный грамотрицательный (кишечная или синегнойная палочка, протей, клебсиеллы, энтеробактер);
- аэробный грамположительный (стафилококк, стрептококк);
- анаэробный грамотрицательный (бактероиды, фузобактерии, вейлонеллы);
- анаэробный грамположительный (клостридии, эубактерии, лактобактерии, пептострептококки, пептококки);
специфический (гонококки, гемолитический стрептококк, микобактерии туберкулёза).
По тяжести общих клинических проявлений:
отсутствие признаков сепсиса;
сепсис;
тяжёлый сепсис (наличие полиорганной недостаточности с указанием объёма и степени полиорганной дисфункции);
инфекционно-токсический шок.
По наличию и характеру осложнений:
внутрибрюшные;
раневая инфекция;
инфекция верхних и нижних дыхательных путей (трахеоброн-хит, нозокомиальная пневмония);
ангиогенная инфекция;
инфекция мочевыводящих путей.
КЛИНИЧЕСКАЯ КАРТИНА
Клиническое обследование
Клинические проявления распространённого перитонита многообразны и складываются в большинстве случаев из симптомов основ-ного заболевания и «наслоения» на них признаков воспаления брюшины, абдоминального сепсиса или септического шока. Так же как симптомы местного перитонита являются составной частью клинических проявлений острых заболеваний органов брюшной полости.
Клинические проявления распространённого перитонита определены сочетанием 3 моментов.
Синдром, характерный для заболевания или травмы, вызвавших перитонит:
острое начало — «кинжальная» боль; перфорация полого органа, абсцессов или кист, нарушение мезентериального кровообращения, странгуляция кишечника, травма;
постепенное развитие — гнойно-деструктивные заболевания органов брюшной полости, первичный перитонит.
Синдром распространённого воспаления брюшины:
постоянные боли в животе;
напряжение брюшных мышц;
симптомы раздражения брюшины (Щёткина-Блюмберга, Воскресенского, Куленкампфа);
симптомы кишечной недостаточности (рвота, отсутствие перистальтики и дефекации, вздутие живота).
Синдром абдоминального сепсиса.
Клинические проявления перитонита во многом определены стадией процесса.
Первая стадия — отсутствие сепсиса. Длительность её составляет от нескольких часов до суток и более. На этой стадии воспалительный процесс в брюшной полости ещё только начинает развиваться, местный перитонит переходит в распространённый. Выпот в брюшной полости серозный или серозно-фибринозный. Если перитонит начинает развиваться в связи с перфорацией органа, то его клиническая картина складывается из симптомов, свойственных прободной язве, перфорации жёлчного пузыря или кишки, перфора-тивному аппендициту и так далее. Сначала боль локализуется в зоне источника перитонита и постепенно распространяется по всему животу, затем становится постоянной, без «светлых промежутков», плохо локализуется. Общими симптомами этой начальной фазы перитонита, развивающегося в связи с перфорацией, служат внезапные резкие боли в животе, сопровождающиеся картиной шока. Не-редко отмечается иррадиация болей в плечи или надключичные области, что связано с раздражением окончаний диафрагмальных не-рвов излившимся в брюшную полость желудочным или кишечным содержимым (симптом Мюсси-Георгиевского). Обычно с самого начала больной имеет вид тяжелострадающего человека, покрытого холодным потом, лежащего в вынужденном положении (нередко на спине или на боку с приведёнными к животу ногами), лишённого возможности глубоко дышать, но находящегося в полном созна-нии. Перитонит, осложняющий воспалительные заболевания органов брюшной полости, не имеет такого резкого начала: нет «ката-строфы», но есть более или менее быстрое прогрессирование локального процесса. Кроме боли, почти всегда бывает рефлекторная рвота и тошнота. Температура тела может быть нормальной, но чаще повышена. Пульс частый и малого наполнения, не соответствует температуре. АД в этот период нормальное или слегка понижено. Язык обложен белым налётом, суховат, но слизистая оболочка щёк ещё влажная. Брюшная стенка не принимает участия в акте дыхания, выявляется защитное напряжение мышц брюшной стенки.
Вторая стадия — стадия абдоминального сепсиса — наступает спустя 24-72 ч от начала заболевания. Продолжительность её — 2-3 сут. Она характеризуется нарастанием воспалительного процесса в брюшной полости. В выпоте появляются фибрин и гной, фагоцитоз ослаблен, резко нарушается мезентериальное кровообращение, что сопровождается развитием синдрома кишечной недостаточности с нарушением всех функций кишки и в первую очередь барьерной. Состояние больного становится тяжёлым. Его беспокоят слабость и жажда. Продолжается мучительная рвота, к концу она принимает характер срыгивания. Рвотные массы тёмные, бурые, с неприятным запахом (так называемая каловая рвота). Кожа влажная, лицо бледнеет, черты его заостряются, глаза западают. Выявляется цианоз кончика носа, ушных мочек, губ. Конечности становятся холодными, ногтевые ложа — цианотичны. Дыхание учащённое, поверхност-ное, иногда прерывистое, аритмичное. АД низкое. Тахикардия до 120-140 в мин, не соответствует температуре. Пульс мягкий, то едва ощутим, то более полный, сердечные тоны глухие. Язык сухой, обложен тёмным, плохо снимающимся налётом. Слизистая оболочка щёк также сухая, сухость во рту мешает больному говорить.
Живот вздут, умеренно напряжён и умеренно болезнен при пальпации, явно выражен симптом Щёткина-Блюмберга. Выраженность напряжения мышц брюшной стенки уменьшается. При перкуссии живота определяется равномерный высокий тимпанит, а в отлогих местах живота — притупление перкуторного звука, изменяющее свой уровень при поворотах больного, что свидетельствует о скопле-нии жидкости. Аускультация выявляет резкое ослабление, чаще полное отсутствие кишечных шумов. Газы не отходят, стул отсут-ствует. Моча становится тёмной, её мало (диурез менее 25 мл/ч). Из-за скопления выпота в полости малого таза мочеиспускание и исследование через прямую кишку могут быть болезнены. Больные в этот период обычно сохраняют сознание, хотя временами могут возникать возбуждение и бред.
Третья стадия — стадия тяжёлого сепсиса и септического шока, она наступает спустя 3 сут и более от начала болезни (иногда поз-же), характеризуется нарастающей полиорганной дисфункцией. Состояние больного крайне тяжёлое. Сознание спутанное, иногда наблюдается эйфория. Кожа бледна и желтушна, выражен цианоз. Боли в животе почти отсутствуют. Дыхание поверхностное, арит-мичное, частый, еле ощутимый пульс, АД низкое (менее 90 мм рт.ст.), олиго- или анурия. Больной то лежит неподвижно, то мечется, вздрагивает, «ловит мушек», глаза становятся тусклыми. Живот вздут, пальпация его практически безболезненна, напряжения мышц нет, при выслушивании — «гробовая тишина». (Проявления системной воспалительной реакции, абдоминального сепсиса и септиче-ского шока.)
Диагностика.
1) Клиника см выше
2) Лабораторная диагностика
Для перитонита характерны очевидные признаки нарастающей печёночно-почечной недостаточности, неконтролируемое снижение уровня белка, признаки азотемии, воспалительные изменения «белой крови», анемия, определение лейкоцитарного индекса интоксикации, при расчёте которого используют модифицированную формулу Я.Я. Кальф-Калифа:
ЛИИ = 32Пл + 8Ми + 4Ю + 2П + С/16Э + 2Б + Мо + Л,
где ЛИИ — лейкоцитарный индекс интоксикации; Пл — плазматические клетки;
Ми — миелоциты; Ю — юные нейтрофилы; П — палочкоядерные нейтрофилы;
С — сегментоядерные нейтрофилы; Э — эозинофилы; Б — базофилы; Л — лимфоциты; Мо — моноциты (норма = 1,08±0,45).
В качестве дополнительных лабораторных показателей диагностики абдоминального сепсиса и перитонита перспективно определение концентрации прокаль- цитонина или С-реактивного белка в плазме крови.
3) Инструментальные методы
Универсальными признаками, подтверждающими необходимость лапаротомии, служат:
наличие свободной или осумкованной жидкости в брюшной полости;
состояние желудочно-кишечного тракта, соответствующее кишечной непроходимости;
нарушение магистрального кровотока висцеральных органов;
признаки гематом или гнойно-деструктивного поражения забрюшинной клетчатки.
Ниже представлены прямые и косвенные признаки визуализационной диагностики распространённого и отграниченного воспаления брюшины.
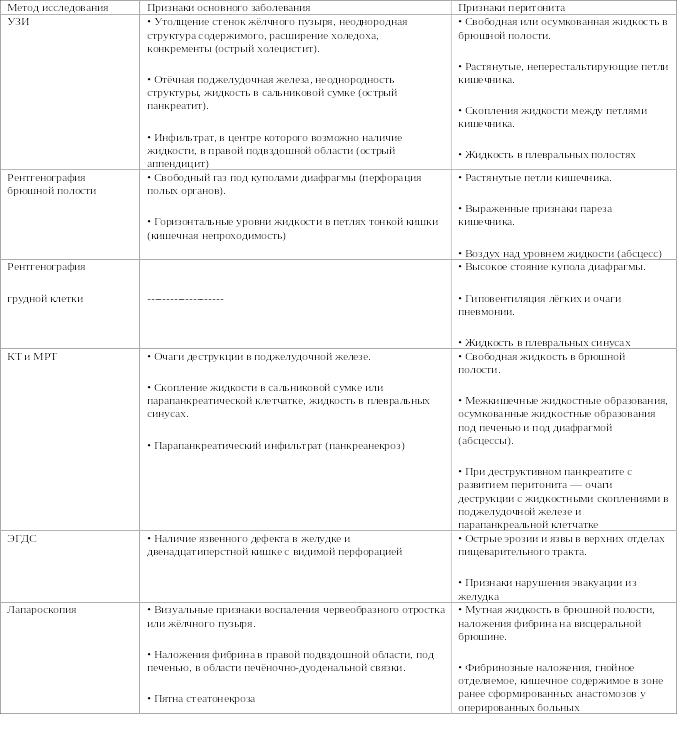
Лечение ниже.
163. Острый гнойный перитонит. Современные принципы комплексного лечения. Осо-бенности оперативного вмешательства. Борьба с нарушениями гемодинамики, микроциркуляции, гидроионными нарушениями, интоксикацией и парезом кишечника.
+ смотри в вопросах до и после.
Лечение. Распространенный гнойный перитонит является абсолютным показанием к экстренному оперативному вмешательству. Основные прин¬\ципы лечения перитонита предусматривают:
1. раннее удаление пораженного органа, послужившего причиной разви¬тия перитонита, или дренирование гнойников;
2. подавление резидуальной инфекции в брюшной полости разными способами: а) аспирацией экссудата и тщательным промыванием брюшной полости растворами (санация полости) во время операции; б) программи-рованным промыванием (повторной санацией) и ревизией брюшной полос¬ти после опрации; в) длительным промыванием брюшной полости через дренажи; г) дренированием 1—2 дренажами; д) созданием лапаростомы;
3. применение адекватной антибактериальной терапии до и после опе¬рации;
4. ликвидацию паралитической непроходимости кишечника (аспирация желудочного и кишечного содержимого через гастроинтестинальный зонд, промывание и стимуляция перистальтики кишечника);
5. интенсивную терапию, направленную на восполнение дефицита ОЦК, коррекцию нарушений водно-электролитного баланса, кислотно-основного состояния, белкового обмена с помощью массивной инфузионной терапии, парентерального питания, экстракорпоральной детоксикации;
6. поддержание на оптимальном уровне функционального состояния сердечно-сосудистой системы, легких (своевременное проведение искусст¬венной вентиляции), печени, почек (проведение гемодиализа).
В качестве операционного доступа используют срединную лапаротомию. Аспирируют экссудат, в тонкую кишку вводят длинный двухпросветный зонд для аспирации кишечного содержимого. Это создает благоприятные условия для ревизии всех отделов брюшной полости, включая ранее наложенные анастомозы. Если источником перитонита является орган, который может быть удален (аппендикс, желчный пузырь, некротический участок кишки), а условия позволяют это сделать, то его удаляют (аппендэктомия, холецистэктомия, резекция кишки и т. п.). В случае перфорации полого органа (язва желудка, двенадцатиперстная кишка) ушивают перфоративное отверстие или производят более радикальную органосохраняющую опера¬цию на желудке. Некротизированные участки кишки при механической ки¬шечной непроходимости или тромбозе мезентериальных сосудов резецируют. Если позволяют условия, то концы резецированной тонкой кишки со¬единяют анастомозом. После резекции толстой кишки концы ее выводят на переднюю брюшную стенку. Аборальный конец кишки иногда закрывают наглухо, т. е. накладывают одноствольную колостому. Через несколько недель после выздоровления восстанавливают непрерывность к и ш к и . Если орган, послуживший причиной перитонита, удалить или вывести на брюшную стенку нельзя, то приходится ограничиваться удалением гноя, подведением дренажей для аспирации гнойного или кишечного содержимого. Тампоны для отграничения очага инфекции от остальных отделов брюшной полости применяют редко, по специальным показаниям.
Брюшную полость в конце операции тщательно промывают 10—15 л изо¬тонического раствора натрия хлорида до чистой воды. К 1 л раствора натрия хлорида необходимо добавлять 100 мл 3% раствора перекиси водорода. Выделяющийся при контакте с воспаленными тканями активный кислород па¬губно действует на анаэробные возбудители. К последней порции жидкости для промывания добавляют раствор антисептического вещества (диоксидин, хлоргексидин, гипохлорид натрия, фурацилин). В процессе санации брюшной полости удаляют рыхлые налеты фибрина, содержащие, как правило, большое количество микроорганизмов.
Для декомпрессии кишечника в тонкую кишку через рот или носовой ход проводят длинный двухпросветный зонд с множественными отверстиями. Через зонд из просвета кишечника аспирируют жидкость и газы, периодически промывают кишечник, вводят энтеросорбенты и антибактериальные вещества. Зонд на некоторое время рекомендуется ввести в прямую кишку для удаления содержимого толстой кишки, в котором имеется наибольшая концентрация микроорганиз¬мов.
При невозможности проведения зонда в кишечник в некоторых хирургиче¬ских учреждениях накладывают илеостому. Выполнение илеостомии или энтеротомии для опорожнения кишечника при перитоните нежелательно, так как эта процедура часто дает опасные осложнения.
В корень брыжейки тонкой кишки в начале или в конце операции вводят 100—120 мл 0,25% раствора новокаина для предотвращения пареза кишки.
Для дренирования брюшной полости при распространенном гнойном или гнилостном перитоните дренажи вводят в полость малого таза (справа и слева), под диафрагму (с обеих сторон) и под печень. Все дренажи выво-дят через отдельные проколы брюшной стенки по передней аксиллярной линии. На операционном столе в брюшную полость вводят 1—2 л раствора, для того чтобы убедиться в полноценности оттока жидкости и экссудата по дренажам. Рану передней брюшной стенки зашивают наглухо или только до подкожной клетчатки, чтобы избежать раннего нагноения. Через 3 — 4 дня рану закрывают наглухо. Экссудат, накапливающийся после операции, будет оттекать пассивно по установленным дренажам.
Если во время операции выявлен распространенный гнойный перито¬нит, а источник инфекции удален, то для подавления резидуальной ин¬фекции через установленные дренажные трубки осуществляют постоян¬ное промывание (перитонеальный диализ/лаваж) брюшной полости. Предполагают, что этим достигается дальнейшее механическое очищение брюшной полости от резидуальной инфекции. В первые же сутки в верхние дренажи капельно вводят изотонический раствор хлорида натрия с добавлением к нему калия, натрия, хлора, кальция, учитывая их содержание в крови.
Отток раствора происходит через нижние дренажи. Необходимо следить за тем, чтобы жидкость не накапливалась в брюшной полости, а количество введенной и выделенной жидкости было одинаковым. Такой способ промывания (диализа) называют проточным. Если количество оттекающей жидко¬сти значительно меньше количества вводимой, то для предотвращения за¬держки жидкости в животе переходят на фракционное промывание. В этом случае вводят раствор в тот или иной дренаж и на несколько часов перекры¬вают его, а затем аспирируют жидкость и экссудат. Фракционное промыва¬ние уступает по эффективности проточному. При проточном промывании в течение суток капельно в брюшную полость вводят 8—10 л раствора, при фракционном — 2—3 л. Проточное промывание проводят в течение 2—3 дней. За это время, как правило, удается более или менее хорошо отмыть брюшную полость, удалить накапливающийся экссудат и пленки фибрина. Несмотря на промывание в брюшной полости образуются рыхлые спайки, отграничивающие дренажи от свободной брюшной полости, препятствующие ирригации всех отделов ее. Дальнейшее проведение промывания становится нецелесообразным.
Недостатками проточного и фракционного промывания является боль¬шая частота (до 20%) формирования межкишечных, поддиафрагмальных и тазовых абсцессов вследствие слипания петель кишечника и отграничения экссудата в образовавшемся пространстве. Примерно так же часто возника¬ют абсцессы при дренировании без промывания.
В настоящее время для лечения распространенного гнойного перитонита с успехом применяют программированное, т. е. заранее запланированное, промывание (повторную ревизию и санацию) брюшной полости. В этом случае после операции края раны брюшной стенки лишь сближают швами на специальных прокладках. Иногда к краям апоневроза прямых мышц жи¬вота подшивают застежку "молния" или нейлоновую сетку, для того чтобы быстро, без дополнительной травмы тканей можно открывать и закрывать рану передней брюшной стенки при повторных ревизиях и санации. Через не полностью закрытую рану (лапаростому) происходит отток экссудата из брюшной полости. В зависимости от общего состояния пациента через 24— 48 ч проводят повторную ревизию брюшной полости, промывая ее, как во время операции. У больных с запущенными формами гнойного перитонита в среднем требуется 3-5 сеансов этапного промывания. Повторные ревизии прекращают, когда брюшная полость становится чистой, а экссудат про¬зрачным. Данная методика позволяет более радикально справляться с резидуальной инфекцией, предотвращать формирование абсцессов, существен¬но улучшить результаты лечения.
Не следует рассматривать программированное промывание как лапаростому. При лапаростомии повторные ревизии и санации брюшной полости не производятся. При перевязках лишь меняют тампоны, закрывающие ра¬ну, а иногда тупым путем в пределах видимости разделяют рыхлые спайки между петлями кишечника и с краями брюшины. Если же источник пери¬тонита во время первой операции не был ликвидирован (например, при не¬состоятельности пищеводно- или желудочно-кишечного анастомозов), то применение данного способа лечения нецелесообразно.
При местном серозном перитоните после удаления органа, послуживше¬го причиной перитонита, достаточно провести локальное промывание, вве¬сти дренаж и закрыть рану. При серозно-гнойном перитоните, распростра-нившемся на нижнюю или верхнюю часть брюшной полости, необходима тщательная санация и дренирование 1—2 двухпросветными трубками. При местном диффузном перитоните с серозным выпотом вблизи воспаленного органа после удаления последнего рану промывают, вводят дренаж и заши¬вают.
Лечение паралитической непроходимости кишечника начинают уже на операционном столе. В корень брыжейки тонкой кишки вводят 0,25% раствор новокаина, в просвет — назоинтестинальный двухпросветный зонд для аспирации содержимого и декомпрессии кишечника. Декомпрессия позволяет улучшить микроциркуляцию стенок кишечника, удалить эндотоксины и микроорганизмы, уменьшить интоксикацию. Зонд целесообразно провести возможно дальше от трейтцевой связки. В послеоперационном периоде производят постоянную аспирацию содержимого кишечника и желудка. Че¬рез зонд можно вводить энтеросорбенты, не всасывающиеся в кишечнике антибактериальные препараты. Периодически зонд и кишечник необходимо промывать. Указанные мероприятия позволяют уменьшить интоксикацию и транслокацию эндотоксинов и бактерий. Для стимуляции кишечника используют антихолинэстеразные препараты, накожную электростимуля¬цию кишечника, клизмы.
Перед операцией и после нее необходимо проводить адекватную интен¬сивную терапию для коррекции нарушений гомеостаза. Это является важнейшим компонентом лечения перитонита! При проведении инфузионной терапии количество внутривенно вводимой жидкости определяют, исходя из рассчета 40—45 мл жидкости на 1 кг массы тела пациента (в среднем 3—4 л/сут). При этом необходимо учитывать и восполнять ощутимые потери воды и электролитов (потери жидкости с мочой, рвотой, выделениями по дренажам и кишечному зонду), а также неощутимые потери (выделение жидкости с потом и выдыхаемым воздухом) — приблизительно 1 — 1 , 5 л/сут.
Для проведения инфузионной терапии и контроля за ее полноценностью сразу после поступления тяжело больного в стационар ему необходимо ввести зонд в желудок для предотвращения аспирации содержимого желудка в дыхательные пути при индукции наркоза, подключичный катетер для быстрого восполнения ОЦК и измерения центрального венозного давления с целью контроля за адекватностью введения растворов. В мочевой пузырь вводится катетер для измерения почасового диуреза. Инфузионная терапия считается адекватной, если центральное венозное давление удается довести и поддерживать на нормальных цифрах и восстановить диурез до 40—50 мл/ч.
С учетом содержания электролитов в крови и кислотно-основного состояния, сначала внутривенно вводят кристаллоидные растворы для быст¬рого восполнения дефицита ОЦК (0,9% раствор натрия хлорида, трисамин, 5% и 10% растворы глюкозы, раствор Дарроу и др.), затем коллоидные растворы для поддержания онкотического давления плазмы и удержания жидкости в сосудистом русле (полиглюкин, реополиглюкин, гемодез, плаз¬му крови, альбумин и другие инфузионные препараты). По строгим показаниям производят переливание эритроцитной массы.
Для парентерального питания используют 10—20% растворы глюкозы, легкоусвояемые растворы аминокислот, жировые эмульсии и другие специально приготовленные растворы. Потребности пациента в питании (в кало¬риях) следует мониторировать так же, как частоту пульса и артериального давления. Многоцентровые исследования метаболизма показали, что более 30% пациентов в отделениях интенсивной терапии голодают. Дефицит в калориях за время пребывания в отделении интенсивной терапии у 30% больных достигает 10000 калорий. Это эквивалентно голоданию здорового человека в течение 5 дней. Позднее, когда восстановится перистальтика ки¬шечника, приступают к энтеральному зондовому, а затем и пероральному питанию.
Для устранения синдрома диссеминированного внутрисосудистого свер¬тывания применяют препараты, улучшающие реологические свойства крови (реополиглюкин, дезагреганты, гепарин).
Для дезинтоксикации организма используют методику гемодилюции с форсированным диурезом (введение фуросемида), в более тяжелых случаях -— экстракорпоральные методы очищения организма от продуктов метаболиз¬ма и токсичных веществ (плазмаферез — более эффективный метод, а также плазмо- и гемосорбцию). Заслуживает осуждения подключение селезенки свиньи. Это равнозначно ксенотрансплантации. В течение 40—60 мин в се¬лезенке развивается сверхострая реакция отторжения, сосуды ее тромбируются, кровь реципиента перестает поступать в подключенную селезенку. В ответ на поступление в кровь реципиента чужеродных белков стимулирует¬ся тот же механизм защиты против антигенной агрессии, который организм использует от агрессии эндотоксинов микроорганизмов. Гиперстимуляция макрофагов и других цитокин продуцирующих клеток, как упоминалось вы¬ше, может быть опасной. Эффективность метода в рандомизированном сравнительном исследовании не доказана. Вместе с тем жизнь пациента подвергается дополнительному риску заражения вирусами животных, избыточной стимуляции иммунной системы антигенами и белками животных.
Для устранения дыхательной недостаточности широко применяют ис¬кусственную вентиляцию легких.
При острой почечной недостаточности осуществляют гемодиализ — для выведения азотистых шлаков и гемофильтрацию — для удаления избытка воды. Изменяя содержание электролитов в диализирующей жидкости, можно во время диализа удалить избыток калия из плазмы. Эти способы помогают эффективно лечить полиорганную недостаточность.
164. Современные принципы комплексного лечения острого гнойного перитонита. Особенности оперативного вмешательства, способы дренирования брюшной полости. Показания к программированной санации брюшной полости. Роль антибиотиков в комплексном лечении.
Лечение распространённого перитонита
Основные направления:
Оптимальная хирургическая тактика;
Рациональная антибактериальная терапия;
Адекватная интенсивная терапия.
Факторы, определяющие успех лечения перитонита:
80% - оптимальная хирургическая тактика (адекватная санация);
20% - антибактериальная и интенсивная терапия.
Задачи оперативного вмешательства:
Устранение источника перитонита;
Интраоперационная санация;
Декомпрессия ЖКТ;
Создание условий для пролонгированной санации брюшной полости в послеоперационном периоде.
Устранение источника перитонита:
Источник перитонита должен быть надёжно ликвидирован с помощью наименее травматичного и технически легко выполнимого способа.
Общепринятый доступ – срединная лапаротомия, позволяющая обеспечить полноценную ревизию и санацию всех отделов брюшной полости.
Объём операции соизмеряется с функциональными возможностями больного.
Обширные резекции и экстирпации органов у тяжелобольных с перитонитом являются вынужденными и выполняются в исключительных случаях.
При невозможности радикального удаления источника перитонита необходима его экстраперитонезация или использование марлевых тампонов, способствующих отграничению инфекционного процесса от остальных отделов брюшной полости.
При перитоните повышается риск несостоятельности кишечных анастомозов.
Вопрос о формировании анастомоза после резекции тонкой и правой половины толстой кишки решается индивидуально в зависимости от сроков перитонита. В большинстве случаев показан первичный анастомоз, так как риск несостоятельности конкурирует с опасными последствиями тонкокишечного свища.
Резекцию левой половины толстой кишки при перитоните следует завершать одноствольной колостомой с ушиванием дистального отрезка кишки по типу обструктивной резекции Гартмана.
Интраоперационная санация:
Адекватность санации брюшной полости определяется следующими факторами:
Высокой степенью бактериальной контаминации перитонеального содержимого;
Ассоциативным характером микрофлоры с широким представительством анаэробов;
Быстрой сменой приоритетных возбудителей;
Быстрым развитием резистентности микрофлоры к антибиотикам.
Санация брюшной полости – важнейший этап оперативного вмешательства, который должен выполняться с особой тщательностью.
Многократное промывание брюшной полости антисептическими растворами проводится до «чистой воды». Во время промывания максимально удаляются фибринозные наложения с брюшины, так как плёнки фибрина содержат такое же количество микробов, что и перитонеальный экссудат. Для промывания брюшной полости используют:
раствор натрия хлорида (с добавлением антибиотиков);
раствор фурацилина 1:5000;
5% раствор глюкозы;
смесь, состоящая из равных количеств раствора фурацилина и 5% раствора глюкозы. При этом конечная концентрация глюкозы не должна превышать 2-2,5%, что важно для предупреждения возможной десквамации мезотелия брюшины;
0,25% раствор новокаина;
при каловых перитонитах – 50 мл 3% раствора перекиси водорода (перекись водорода способствует более эффективной механической обработке поверхности брюшины и воздействует на анаэробную микрофлору, которая при каловых перитонитах всегда имеется в брюшном экссудате). В заключительную порцию санирующего раствора перед закрытием брюшной полости добавляется 1-2 г канамицина или мономицина в сочетании с протеолитическим ферментом химотрипсином (50 г/л), так как протеолитический фермент улучшает бактерицидный эффект антибиотика даже при минимальных экспозициях;
10% раствора тиосульфата натрия;
0,2% раствор хлоргексидина биглюконата;
изотонический раствор Рингера с антибиотиками;
"Дезмистин" (в соотношении 1:10 с раствором натрия хлорида 0,9%);
поливинилпирридолом;
полиионным изотоническим раствором (аппарат «Гейзер»);
раствор "Бализ-2".
Адекватная санация позволяет добиться максимальной деконтаминации брюшины и способствует снижению уровня эндогенной интоксикации. Неполноценная санация не может быть восполнена ни антибактериальной терапией, ни интенсивной терапией.
Способы завершения операции:
Дренирование брюшной полости;
Перитонеальный диализ;
Повторные ревизии и санации брюшной полости («этапный лаваж», программируемая релапаротомия и др.);
Лапаростомия.
Дренирование брюшной полости:
Дренирование брюшной полости не всегда способствует адекватной санации независимо от количества дренажных трубок.
При перитоните у 80% больных через 12-24 часа дренажные трубки теряют свою проходимость. В связи с этим дренажи не могут обеспечить полноценный отток экссудата из брюшной полости, следовательно, её полноценную санацию в послеоперационном периоде.
Перитонеальный диализ:
Метод широко использовался в 70-х – 80-х годах прошлого столетия, как метод пролонгированной санации брюшной полости у больных с распространённым перитонитом и сыграл положительную роль в снижении летальности.
Преимуществаметода:
непрерывное промывание брюшной полости;
не требуется наркоз.
Недостатки метода:
водно-электролитные и белковые нарушения;
местные инфекционные осложнения;
пролежни от длительно стоящих дренажей;
невозможность адекватной санации.
В последние годы метод практически не используется при лечении распространённого перитонита.
Стремление активно воздействовать на инфекционный процесс при распространённом перитоните как во время операции, так и после неё побудило хирургов к разработке активных хирургических методов пролонгированной санации брюшной полости. К ним относятся лапаростомия и программируемые ревизии и санации брюшной полости.
Лапаростомия:
Преимущества метода:
визуальный контроль за течением инфекционного процесса в брюшной полости;
самопроизвольный отток экссудата из брюшной полости;
коррекция симптомов повышенного внутрибрюшного давления;
упрощение повторных вмешательств.
Недостатки метода:
водно-электролитные и белковые нарушения;
травматизация петель кишечника и формирование свищей;
эвентрация органов;
длительные сроки лечения;
ретракция брюшной стенки с последующим формированием вентральной грыжи.
При формировании истинной лапаростомы брюшную стенку не ушивают, кишечные петли покрывают марлевыми тампонами или синтетическими сетчатыми материалами. Возможно открытое лечение перитонита в камере с абактериальной средой. В настоящее время метод применяется в исключительных случаях в связи с представленными недостатками.
Показания:
Послеоперационный гнойный перитонит с флегмоной передней брюшной стенки;
Гнойный перитонит с множественными межпетлевыми абсцессами;
Гнойный перитонит с несформированными кишечными свищами;
Синдром полиорганной недостаточности с поражением трёх и более органов, развитием глубоких гемодинамических нарушений, не позволяющих использовать этапные ревизии.
Плановые санации брюшной полости:
Широкое использование получили модифицированные варианты открытого лечения перитонита, заключающиеся в частичном или полном сближении краёв лапаротомной раны с последующими ревизиями и санациями брюшной полости.
Способы закрытия лапаротомной раны:
Провизорные швы;
Вентрофилы;
Металлические пластины;
Застёжка «молния»;
«Специальные» устройства.
По своему значению программированные санации очень близки к лапаростомии, но не тождественны ей.
В настоящее время плановые санации считаются наиболее эффективным хирургическим методом воздействия на инфекционный процесс при распространённом перитоните.
Суть метода:первичные операции с ликвидацией источника перитонита, ряд повторных ревизий и санаций брюшной полости.
Принципы метода:
1. Адекватная санация брюшной полости с максимальным удалением бактериального субстрата, создание условий, противодействующих дальнейшему прогрессированию инфекционного процесса.
2. Интраоперационная оценка динамики и прогнозирование течения перитонита, ранняя диагностика осложнений.
Преимущества метода:
Эффективное воздействие на внутрибрюшинный инфекционный процесс;
Ранняя диагностика внутрибрюшных и раневых осложнений;
Отсутствие дренажей;
Предупреждение внутрибрюшных абсцессов;
Пагубное воздействие аэрации на анаэробную микрофлору.
Недостатки метода:
Длительная назоинтестинальная интубация;
Повторные наркозы;
Повторные повреждения брюшной стенки;
Агрессивность метода.
Показания:
Распространённый гнойный перитонит с клиническими проявлениями высокой бактериальной контаминации;
Послеоперационный прогрессирующий перитонит;
Множественные межкишечные абсцессы (формирующиеся или имеющиеся);
Распространённый гнойный перитонит, осложнённый ПОН (три и более системы);__
Неуверенность в состоятельности кишечных швов и анастомозов.
Повторная ревизия планируется во время первой операции. Оптимальные сроки 24-48 часов после первичной операции.
При планировании повторной ревизии нужно ориентироваться на:
клинические признаки перитонита;
выраженность синдрома эндогенной интоксикации;
динамику СПОН;
данные предшествующей интраоперационной ревизии.
После устранения источника перитонита и санации брюшной полости проводиться назоинтестинальная интубация, которая является строго обязательным этапом операции при использовании метода плановых санаций.
Назоинтестинальная интубация обеспечивает:
декомпрессию ЖКТ;
облегчает манипуляции в брюшной полости, уменьшает травматичность операций, снижает внутрибрюшное давление;
способствует восстановлению перистальтики, улучшает кровообращение и микроциркуляцию в стенке кишки;
снижает уровень эндогенной интоксикации;
предупреждает несостоятельность кишечных анастомозов и эвентраций;
обеспечивает возможность выполнения кишечного лаважа, селективной декантаменации кишечника и энтерального питания.
Назоинтестинальный зонд удаляют на следующий день после последней ревизии при условии восстановления перистальтики кишечника.
Агрессивность и высокая травматичность метода плановых санаций заставили хирургов искать альтернативные варианты. Использование современных технологий расширило возможности лапароскопии.
Этот метод стал широко применяться не только для верификации перитонита, но и как метод пролонгированной санации брюшной полости.
Лапароскопическая санация:
Преимущества метода:
Малая травматичность;
Сокращение раневых осложнений;
Ранняя диагностика внутрибрюшных абсцессов;
Ранняя реабилитация пациента;
Возможность избежать напрасных релапаротомий.
Недостатки метода:
Невозможность адекватной санации при высокой степени бактериальной контаминации брюшной полости и множественных плотных фибринозных наложениях;
Плохая визуализация при паралитической дилатации кишечника;
Невозможность назоинтестинальной интубации.
Оптимальные сроки выполнения санационных лапароскопий 12 – 24 часа после операционного вмешательства.
Лапароскопическая санация не является альтернативой методу программированных санаций.
Видеолапароскопия позволяет обеспечить адекватную санацию брюшной полости только в случае низкой бактериальной контаминации бактериального экссудата.
Каждый из методов пролонгированной санации брюшной полости, обладая целым рядом преимуществ, в то же время имеет недостатки.
Оптимально сочетающим преимущества и недостатки является метод повторных ревизий и санаций брюшной полости, который эффективно воздействует на внутрибрюшной инфекционный процесс.
Лапаростомия рассматривается как вынужденная операция, при невозможности использования других методов.
Видеолапароскопия должна использоваться по ограниченным показаниям в виду технической невозможности обеспечения адекватной санации при тяжёлых формах перитонита.
АНТИБИОТИКОТЕРАПИЯ.
Пути введения антимикробных препаратов:
1. местный (внутрибрюшной) – через ирригаторы и дренажи;
2. общий:
Внутривенный;
Внутриартериальный (внутриаортальный, в чревный ствол, в брыжеечные или сальниковую артерии);
Внутримышечный (только после восстановлении микроциркуляции);
Внутрипортальный – через реканализированную пупочную вену в круглой
связке печени;
Эндолимфатический:
Антероградный – через микрохирургически катетеризированный периферический лимфатический сосуд на тыле стопы или депульпированный паховый лимфатический узел.
Ретроградный - через грудной лимфатический проток.
Лимфотропный внутритканевой – через лимфатическую сеть голени, забрюшинного пространства.
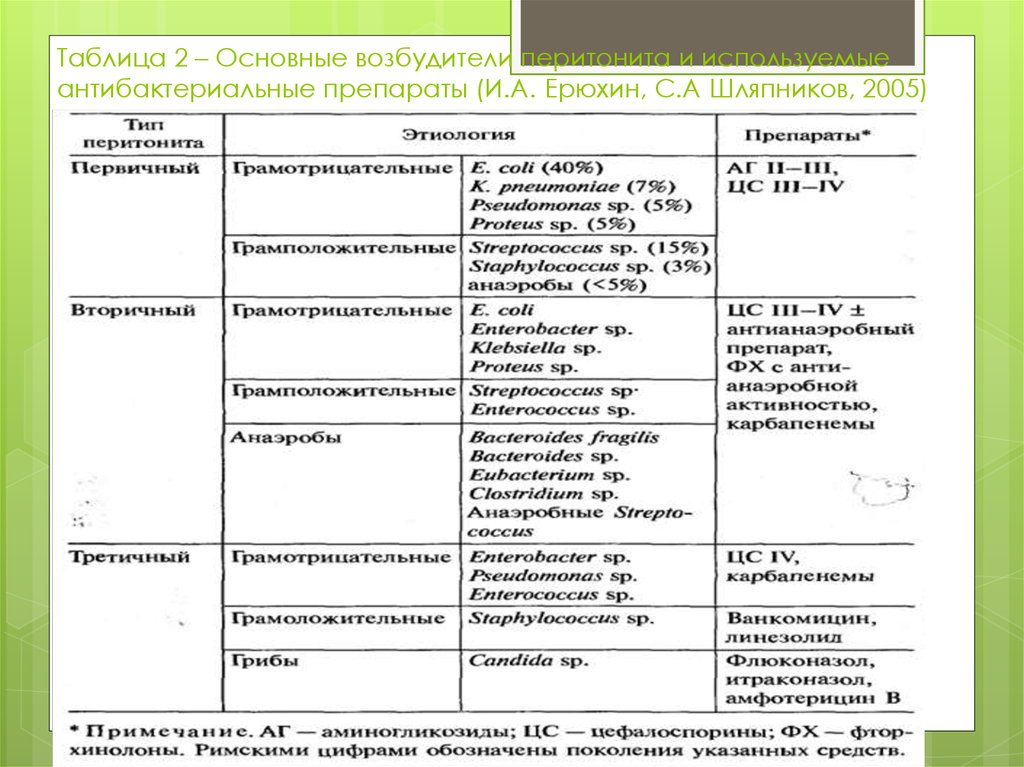
Первичный перитонит составляет примерно 1 % от всех клинических случаев перитонита. Он развивается у больных, страдающих тяжелыми фоновыми заболеваниями, и основными возбудителями являются пневмококки (Strept.Pneumoniae) и грамотрицательные палочки (Esherichia coli, Klebsiella spp.). Как правило, среди возбудителей отсутствуют анаэробные микроорганизмы, и инфекционный процесс вызывается одним возбудителем. Возбудители попадают гематогенным путем или за счет транслокации через стенку кишечника.
Наиболее часто используемые препараты: аминогликозиды (гентамицин, амикацин, нетромицин), цефалоспорины III – IV (цефтриаксон, цефтазидим, цефепим)
Вторичный перитонит, наиболее часто встречающийся в клинической практике, вызывается энтеральными грамотрицательными возбудителями и облигатными анаэробами. На выбор антибиотика существенное влияние оказывают следующие факторы. Во-первых, локализация первичного очага. В зависимости от того, является ли источником верхний отдел желудочнокишечного тракта или нижний, желчевыводящие и мочевыводящие пути, определяется преимущественная микрофлора, вегетирующая в этой зоне. Вовторых, важнейшим фактором является тяжесть состояния больного и степень органной недостаточности. Оценку этих параметров проводят по широко распространенным шкалам: SAPS (наиболее распространена в Европейских странах) или APACHE II (используется в США и Канаде) и SOFA. Общий принцип заключается в том, что чем тяжелее состояние больного, тем более мощные и менее токсичные антибиотики должны применяться.
Использование антибиотиков резерва (цефалоспорины IV поколения, карбапенемы) сразу с момента начала антибактериальной терапии у тяжелой и крайне тяжелой категории22 больных не только обеспечивает лучший прогноз за счет широкого спектра и меньшей токсичности, но и является экономически более выгодным.

При лечении третичного перитонита надо всегда помнить о риске развития системного кандидоза. Использование противогрибковых препаратов в качестве профилактического средства остается до настоящего времени вопросом, не имеющим однозначного решения. Большинство исследователей склоняются к мысли о нецелесообразности приема флюконазола или итраконазола с профилактической целью. Чрезвычайно широко распространенное мнение о профилактической эффективности нистатина также не соответствует действительности, в связи с его низкой биодоступностью. Он эффективен лишь при кандидозах слизистых оболочек полости рта и верхних отделов желудочно-кишечного тракта.
