
bkh_dlya_tebya
.pdf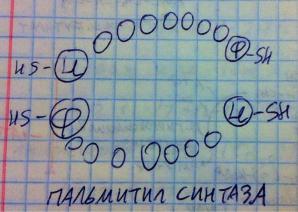
углеводорода надо было отщепить водороды (получив энергию от них), а на их место поставить кислород – режем углеводород на ацетилы, к которым присоединяем КоА. А в синтезе жирных кислот мы соединяем ацетилы (малонил – тот же ацетил, просто с аксексуаром), отсоединяем от них кислороды, а на их место ставим водороды – получается длинный углеводород. Надеюсь, вы уловили сходство. Вот только кое-что для вас будет новым – все реакции выполняет один полифункциональный фермент, вместо множества монофункциональных. Фермент называется пальмитилсинтаза, он состоит из 2-х субъединиц, в каждой по 7 доменов, в качестве закрепителей ацилов выступают цистеин и 4-фосфопантетеин, имеется ацилпереносящий белок, фермент одновременно синтезирует по две кислоты, субъединицы антипараллельны. Предлагаю самую простую схему фермента на рисунке.
Фермент получил своё название неслучайно – он синтезирует только пальмитиновую кислоту, остальные кислоты получаются из этой путём дополнительных превращений другими ферментами. Данный фермент не регулируется, хотя полагают, что инсулин может вызывать увеличение количества этого фермента. Благодаря тому, что это один фермент и продукты одной реакции мгновенно переходят участвовать в другую, синтез жирных кислот протекает крайне быстро (это один из путей утилизации глюкозы, он должен работать быстро). Теперь разберёмся с самими реакциями. Фермент для удобства обозначаем прямоугольником с двумя буквами (цистеин и 4-фосфопантетеин) с сульфгидрильными группами. Первым делом на цистеин переносится ацетил из ацетила-КоА, дальше на 4- фосфопантетеин переносится малонил из малонила-КоА. Теперь начинается цикл. Первым делом малонил теряет карбоксильную группу, на место которой становится ацетил – получается ацетоацетил. Дальше ко второму кислороду и соответствующему углероду присоединяют водород с помощью НАДФН2, образуется гидроксильная группа, затем отщепляется вода через эту группу – образуется двойная связь. К двойной связи добавляют водород с помощью НАДФН2 – образуется полноценный насыщенный углеводородный радикал. Далее образованный бутирил (4-х углеродный ацил) переносят
201
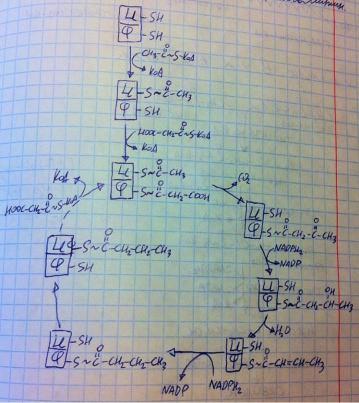
обратно на цистеин, чтобы в следующем цикле он делал всё то же самое, что делал ацетил, только с уже более длинным радикалом. К 4-фосфопантетеину присоединяется новый малонил – цикл повторяется. Циклы повторяются до тех пор, пока не будет синтезирован пальмитил, который гидролитически отщепляется, превращаясь в пальмитиновую кислоту.
Посчитаем затраты на синтез пальмитиновой кислоты. Она строится из двухуглеродных компонентов, первым является ацетил-КоА, а дальше только малонилы-КоА (считаем за двухуглеродный компонент, ибо карбоксильную группу он теряет и становится двухуглеродным), т.е. в пальмитиновой кислоте 16 углеродов – 1 ацетил-КоА и 7 малонил-КоА. На транспорт каждого ацетил-КоА тратится 1 АТФ, а таких 8 (7 из них были превращены в малонилКоА), а на синтез каждого малонила-КоА тратится по 1 АТФ, в сумме 15 АТФ.
А в каждый цикл (как и малонилов, их 7) тратится по 2 НАДФН2. Тогда в сумме на синтез пальмитиновой кислоты потрачено 1 ацетил-КоА, 7 малонил-КоА, 15 АТФ, 14 НАДФН2.
Если же вам нужна кислота подлиннее (мозг у нас такие просто обожает, особенно с нечётным числом углеродов), вы можете использовать ферменты «элонгации» (удлиннения), которые с помощью того же малонилКоА наращивают радикал аналогичными реакциями (вот прям точь-в-точь). А если вы хотите синтезировать ненасыщенную кислоту, то в положениях 9-10 можно сделать двойную связь в микросомах (особые участки ЭПР) с помощью цитохрома—b5, который получает электроны от НАДН2 с помощью соответствующей редуктазы (подробно всё разберём на теме печени), затем
202

этот цитохром берёт электроны, присоединяет их к молекуле кислорода, потом суёт в него протоны – образуется вода, но только одна, а второй атом кислорода остаётся свободным, он-то забирает водород от углеродов жирной кислоты и тоже превращается в воду, так жирная кислота приобретает двойную связь. Но мы умеем делать только одну двойную связь, поэтому полиненасыщенные жирные кислоты мы получаем только с пищей.
Синтез глицерофосфолипидов
Теперь обсудим синтез глицерофосфолипидов или как их ещё называют фосфатидами в честь фосфатидной кислоты, которая лежит в их основе. Синтез фосфатидов сопряжён с синтезом ТАГ. Всё так же начинается с синтеза глицерол-3-фосфата, который можно получить фосфорилированием глицерола глицеролкиназой, либо можно присоединить водород к диоксиацетонфосфату ДАФ (из гликолиза), последний вариант используется чаще.
203
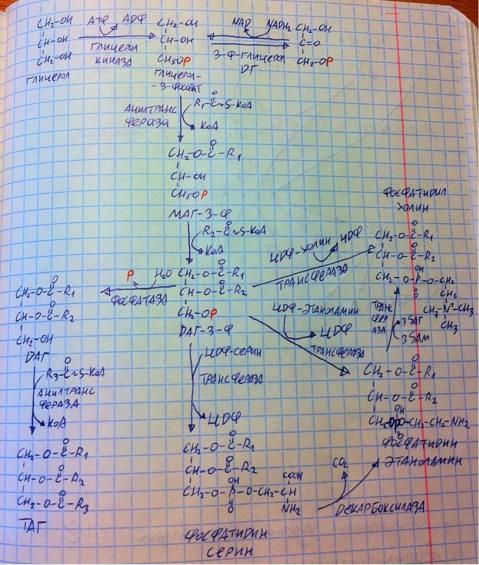
Дальше к глицерол-3-фосфату ацилтрансферазы последовательно присоединяют по одному ацилу от ацил-КоА, образуя сначала МАГ-3-фосфат, затем ДАГ-3-фосфат (фосфатидная кислота), который по сути является узловым метаболитом, из него можно сделать ТАГ, а можно и глицерофосфолипиды. Если подействовать фосфатазой, получится ДАГ, на него действуем ацилтрансферазой, получаем ТАГ. Но также с помощью специальных трансфераз мы можем взять ЦДФ-серин, перенести серин с ЦДФ на фосфатидную кислоту – получим серин, та же история с этаноламином и холином. Примечательно то, что данные глицерофосфолипиды могут превращаться друг в друга, ведь если декарбоксилаза отщепит углекислый газ от серина, то тот превратится в этаноламин, а если метилтрансфераза с помощью 3-х SАМ подействует на этаноламин, то тот превратится в холин. Ну ещё, конечно, есть другие глицерофосфолипиды, например, дифосфатид и фосфатидилинозитол. Дифосфатид создаётся трансферазой с использованием фосфатидной кислоты и ЦДФ-ДАГ (получится как бы два ДАГ, соединённые фосфорной
204
кислотой), а фосфатидилинозитол из фосфатидной кислоты и ЦДФ-инозитола тоже трансферазой.
Липотропные вещества
Теперь очень важная и интересная подтема – липотропные вещества. Ими называют те самые полярные «головки» для синтеза глицерофосфолипидов (серин, этаноламин, холин, инозитол) и вещества, необходимые для синтеза этих «головок» (метионин в качестве SАМ, витамины B9 и B12 выступают донорами метильной группы для синтеза холина) – эти вещества необходимы для синтеза глицерофосфолипидов. Заметьте, что ТАГ и глицероФЛ имеют общего предшественника – фосфатидную кислоту, поэтому они конкурируют между собой. Что это значит? Если в печени очень много жирных кислот, а липотропных веществ мало, тогда большая часть фосфатидной кислоты уйдёт на синтез ТАГ, а чем больше липотропных веществ, тем больше фосфатидной кислоты уходит на синтез глицероФЛ. Схема довольно простая. Насколько это важно с клинической точки зрения? Ну смотрите. По какой-то причине жирных кислот образуется явно больше, чем липотропных факторов, тогда ТАГ в печени становится много (ЛПОНП не успевают уносить ТАГ из печени), а глицероФЛ становится очень мало, в результате чего печень почти перестаёт синтезировать ЛП, ибо тем позарест нужны глицероФЛ для формирования внешней оболочки. Получается, что в печени очень много ТАГ, который некому уносить (ЛП не синтезируются без глицероФЛ). И вот тогда проиходит патологический процесс – печень депонирует ТАГ. Насколько это плохо? Единственное, что должна депонировать печень, это гликоген, который и так много места занимает, а оставшееся пространство в клетках занято кучей метаболических процессов (у печени центральная роль в метаболизме белков, углеводов и липидов), а когда в печени депонируется ТАГ в форме здоровенных липидных капель, гепатоциты не могут выполнять свои функции, за этим следует нарушение функции печени и всего обмена веществ (в дальнейшем может повлечь дисфункцию многих органов). Вот это называется жировым перерождением печени. Само по себе оно не пройдёт,
а если это затянется, то может начаться некроз гепатоцитов, в общем это тяжёлое заболевание с множеством последствий. Как лечить? К счастью, это просто, если не затягивать – необходимо давать пациенту в большом количестве липотропные вещества, что склонит равновесие в сторону синтеза глицероФЛ, тогда, во-первых, печень начнёт получать глицероФЛ и синтезировать ЛПОНП, что поможет ей избавиться от уже имеющегося ТАГ, а во-вторых, увеличение синтеза глицероФЛ конкурентно вызывает снижение синтеза ТАГ, т.е. печень одновременно избавляется от имеющегося ТАГ и предохраняется от образования нового ТАГ. В итоге, печень очищается и всё
205
становится на свои места. Но есть и вторая логичная сопутствующая мера – жировое перерождение печени редко провоцируется дефицитом липотропных веществ, чаще её провоцирует избыток образования жирных кислот (липотропные вещества в норме, а жирные кислоты в переизбытке, поэтому равновесие сдвигается в сторону синтеза ТАГ), поэтому мера будет заключаться в том, чтобы остановить это избыточное образование жирных кислот. Так что приводит к избыточному синтезу (или просто их избытку) жирных кислот и, соответственно, жировому перерождению печени? Вопервых, сахарный диабет 2-го типа. Как я и говорил, жировая ткань и, возможно, мшцы не утилизируют глюкозу, поэтому вся работа падает на печень, большую часть глюкозу ей приходится превращать в жирные кислоты (гликолиз, ПДК, ПФП) и, соответственно, ТАГ, которых образуется в 2 раза больше обычного, а то и больше – вот вам и явный перевес ТАГ над глицероФЛ. Во-вторых, злоупотребление алкоголем. У этого явления много патологических аспектов, но я обращу внимание на то, что в результате обезвреживания в печени этанола образуется много ацетил-КоА и НАДН2, НАДН2 смещает равновесие реакции превращения ДАФ в глицерол-3-фосфат
в сторону глицерол-3-фосфата, который используется для синтеза ТАГ, а из лишнего ацетил-КоА синтезируются жирные кислоты, они оказываются в избытке, синтез ТАГ снова превалирует над глицероФЛ. В-третьих, ожирение и просто калорийное питание. Если вы едите много быстрых углеводов, то они в большинстве превратятся в ТАГ, а если вы сверху будите заедать жирной пищей, то вы к жирным кислотам, синтезированным из глюкозы, добавите жирные кислоты пищи – комбо. Вот это основное, касательно синтеза фосфатидов и жирового перерождения печени. Главное, запомните, что синтезы ТАГ и глицероФЛ конкурируют друг с другом, а равновесие между их синтезом меняется с помощью жирных кислот (в сторону ТАГ) и липотропных веществ (в сторону глицероФЛ). Кстати вещества, вызывающие излишний синтез жирных кислот, ТАГ и жировое перерождение печени, типа алкоголя, называются антилипотропными.
Холестерол
Теперь перейдм к такой важной молекуле, как холестерол. Это важная и нужная молекула, хотя в последнее время говорят только о его негативной стороне. В чём польза холестерола? Во-первых, это незаменимый компонент клетоных мембран – он придаёт им жёсткость и стабильность (без него они бы были никакие, проверено экспериментально). Во-вторых, холестерол выделяется с секретом сальных желёз, которые поддерживают функциональное состояние кожи и волос. В-третьих, из холестерола синтезируются гормоны коры надпочечников и половые гормоны. В- четвёртых, из холестерола синтезируется витамин D3, без которого у нас наступил бы остеопароз, а у детей рахит. В-пятых, из
206

холестерола синтезируются желчные кислоты, без которых невозможно переваривание липидов (вспомните, чем чревата стеаторея и поймёте, насколько важны желчные кислоты и, соответственно, холестерол). Так что холестерол – важная молекула, но его избыток в крови (как общий уровень, так и отдельно в атерогенных фракциях ЛП) приводит к развитию атеросклероза. Но вообще так практически со всеми молекулами в нашем организме – для их концентраций в различных состояниях организма существуют пределы верхние и нижние, выход за которые чреват патологическим состоянием. Очень часто болезнь это не что-то новое, а просто отклонение от нормальных параметров того, что в нас и так было.
Теперь перейдём к самому синтезу холестерола.
Синтез холестерола можно условно разделить на 4 этапа: синтез мевалоновой кислоты, синтез сквалена, ланостерола и холестерола. В рамках программы обычно разбирают только синтез мевалоновой кислоты, так как там вполне адекватные реакции, на следующих стадиях сплошной мрак. Синтез мевалоновой кислоты очень похож на синтез кетоновых тел –
207
разница в последней реакции. Сначала тиолаза сочетает 2 ацетил-КоА, убирая один КоА и создавая ацетоацетил-КоА, к которому ГМГ-КоА-синтаза присоединяет уксусную кислоту, образованную путём гидролиза ещё одного ацетил-КоА – получается 3-гидрокси-3-метил-глутармл-КоА ГМГ-КоА. На ГМГКоА действует ГМГ-КоА-редуктаза, она берёт 4 водорода от 2-х НАДФН2, к сере от КоА присоединяет один водород, чтобы восстановить сульфгидрильную группу, а другие три водорода присоединяет к углероду и кислороду, чтобы получился как бы спирт – вот вам и мевалоновая кислота. ГМГ-КоА-редуктаза – ключевой фермент синтеза холестерола, он активируется посредством дефосфорилирования по инициативе инсулина и ингибируется посредством фосфорилирования по инициативе глюкагона. Помимо этого, если в клетке достаточно холестерола, тот воздействует на цитозольный рецептор, который прекращает синтез ключевого фермента (точнее транскрипцию и в последствие трансляцию), чтобы клетки не синтезировали холестерола больше, чем надо, также синтез холестерола ингибируется, если его в достатке поступает из крови в ЛПНП. Ну и как я говорил в теме атеросклероза, существуют препараты-статины, которые ингибируют ГМГ-КоА-редуктазу, чтобы организм не синтезировал свой холестерол, а брал тот, который в крови в избытке, вот только у этих препаратов есть побочные эффекты в виде неработающей печени.
Синтез сфинголипидов
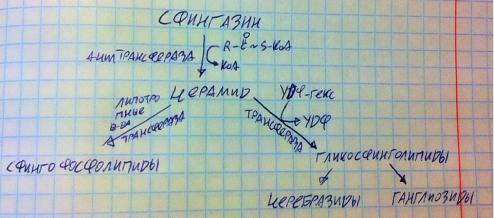
Ацилтрансфераза присоединяет ацил к сфингазину – образуется церамид. Если другая трансфераза присоединит к церамиду липотропные вещества (да-да, у глицеро- и сфингофосфолипидов есть общие липотропы) тоже через ЦДФ, то образуются сфингофосфолипиды – сфингомиелин. А если же специальные трансферазы присоединят к церамиду углеводы (через УДФ-гексозу, в синтезе гликогена похожий механизм был – вспоминайте), то получиатся гликосфинголипиды (если одна гексоза, то церебразид, если целый олигосахарид, то гангиозид). Эти липиды, как и все, катаболизируются, если с их катаболизмом случаются проблемы, то развиваются так называемые болезни накопления. Сейчас коротко скажем о
208
них пару слов. Если у вас сломана сфингомиелиназа (разрушает сфингомиелин, т.е. сфингофосфолипиды), то эти липиды откладываются в лизосомах, особенно в нервной ткани, что приводит к умственной отсталости
и ранней смертности – болезнь Нимана-Пика. Если сломана церебразидаза (разрушает церебразиды), то наступает болезнь Фарбера, при которой также умственная отсталость, но ещё и увеличение в размерах печени и селезёнки. Для ганглиозидов, так как у них олигосахарид присоединён к церамиду, придуманы гликозидазы, которые откусывают по одной глюкозе, если эти ферменты не работают, то эти липиды, оказавшись в лизосоме (они очень широкие) разрывают её, тогда лизосомальные ферменты выходят в цитоплазму и разрушают всё на своём пути – болезни Гоше и Тея-Сакса.
Раз уж я снова заикнулся о катаболизме, должен уделить отдельное внимание катаболизму некоторых глицерофосфолипидов, ибо они могут разрушаться, но не по энергетической нужде, а по регуляторной. Нужно знать два примера. Во-первых, фосфолипаза-C, которая разрушает фосфатидилинозитолдифосфат ФИФ2 на ДАГ и инозитол-трифосфат (ИФ3), которые нужны для прямой и опосредованной активации протеинкиназы-C, данная фосфолипаза, так как является передатчиком гормонального сигнала, активируется альфа-субъединицей G-белка. Вторая фосфолипаза – фосфолипаза-А2, которая прилагает гидролиз к разным глицероФЛ, но в другое место – она отщепляет из 2-го положения арахидоновую кислоту, чтобы из той могли синтезироваться эйкозаноиды, ибо это основное хранилище этой кислоты (цитоплазматическая мембрана, её глицероФЛ). Данная фосфолипаза также активируется через альфа-субъединицу G-белка. Один из методов борьбы с воспалением – ингибирование фосфолипазы-А2, чтобы та не освобождала арахидоновую кислоту, из которой синтезируются простогландины, которые являются медиаторами воспаления.
Ацетил-КоА
Теперь обсудим получение и применение такого ключевого метаболита, как ацетил-КоА (в белковом, липидном и углеводном обмене). Универсальная схема. Откуда получается ацетил-КоА? Во-первых, из жирных кислот, которые есть в любом сложном липиде, путём бета-окисления можно получить ацетил-КоА. Во-вторых, всех углеводы (на основе гексоз в основном) превращаются в глюкозу, та идёт в гликолиз, даёт ПВК, ПВК в ПДК даёт ацетил-КоА. Помимо этого, ТАГ распадается на жирные кислоты и глицерол, а глицерол после пары реакций тоже включается в гликолиз. В- третьих, белки распадаются на аминокислоты, гликогенные дают пируват, или что-то около, или то, что может включаться в ЦТК, кетогенные дают кетоновые тела, которые через бета-окисление превращаются в ацетил-КоА, кетогликогенные делают и то, и другое. В итоге, все аминокислоты приходят к ацетил-КоА. Ну и в-четвёртых, кетоновые тела в бета-окислении
209
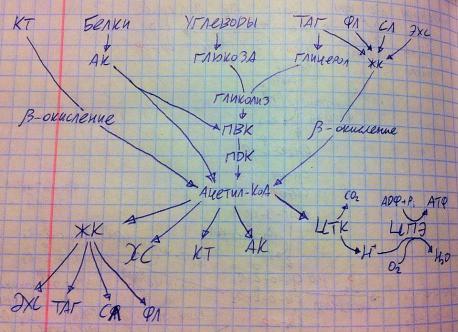
распадаются на ацетил-КоА. Есть, конечно, пятый источник – этиловый спирт, но это уже на ваши страх и совесть.
На что расходуется ацетил-КоА? Из него синтезируются жирные кислоты, а из них все сложные липиды, синтезируется холестерол, кетоновые тела, аминокислоты (кетогенные и кетоглюкогенные), но также ацетил-КоА обильно поступает в общий конечный путь катаболизма, т.е. уходит в ЦТК, в котором уходит углекислый газ, образуются протоны (с электронами, конечно, без них ничего бы не получилось, недаром же цепь переноса электронов, можете по желанию их даже себе на схемку подрисовать), которые поступают в ЦПЭ, туда же кислород – образуется вода, одновременно синтезируется АТФ. Это в общем-то всё, что нужно знать.
Строение мембран
Последняя тема в липидном обмене – клеточные/метаболические мембраны как особые структуры, основанные на липидах, а потому и разбирающиеся в теме липидного обмена. Разберём основные вопросы, связанные с ними.
А начнём мы со строения мембран, его общий план. Все клеточные мембраны состоят из липидов и белков (некоторые выделяют ещё углеводный компонент, но углеводы в мембране есть только как часть липидов и белков, поэтому правильнее всё же выделять только липидный и белковый компоненты). Доля липидов в зависимости от мембраны колеблится от 30% до 70%, то же касается и белков – от 30% до 70%. Все липиды амфифильные, т.е. имеют гидрофильную (контактирует с цитоплазмой и внеклеточной жидкостью) и гидрофобную (контактируют друг
210
