
Полезные материалы за все 6 курсов / Учебники, методички, pdf / методичка онкология лекции
.pdfстояния резко усугубляется повторяющимися желудочно-пищеводными кровотечениями, асцит перестает купироваться лекарственной терапией.
В ряде случаев наблюдается осложненное течение ПРП, когда осложнения проявляются после определенного бессимптомного периода. Тромбоз воротной вены и ее ветвей, печеночных артерий, тромбоз печеночных вен и НПВ (синдром Бадда – Киари) с развитием острой печеночной недостаточности, распад опухоли с разрывом печени и внутрибрюшинным кровотечением, формирование артерио – портальных шунтов, развитие механи- ческой желтухи, желчных свищей, гемобилии, формирование внутрипече- ночных абсцессов.
Бессимптомное или скрытое течение ПРП наблюдается при небольших размерах опухолей печени, которые выявляются, как правило, случайно при лапаротомии или аутопсии.
Средняя продолжительность жизни после начала клинических проявлений заболевания без лечения 5 – 6 месяцев.
Диагностика ПРП
В настоящее время скрининг первичного рака печени несовершенен. Основан на определении в крови обследуемых лиц групп риска один раз в 4-6 мес., уровня АФП крови и, в случае повышения его концентрации, применение УЗИ печени.
АФП – гликопротеид, у большинства больных ПРП с опухолью больше 3 см концентрация маркера в сыворотке крови выше 20 нг/мл (20 мкг/л). Концентрация маркера прямо пропорциональна массе опухоли. Данный иммунохимический маркер имеет диагностическое значение при гепатоцеллюлярном, гепатохолангиоцеллюлярном раке и гепатобластоме. Холангиокарцинома, цистаденокарцинома, недифференцированный рак печени не сопровождаются повышением концентрации АФП в сыворотке крови.
Определение АФП пригодно для скрининга гепатоцеллюлярной карциномы в указанных группах риска, особенно на фоне постоянно возрастающей активности ферментов – ЩФ, гамма-ГТ, АСТ, АЛТ. Более специфич- ным, чем АФП является дес-гамма-карбоксипротромбин (дес-гамма-КПТ) – витамин К-зависимый предшественник протромбина, синтезируемый нормальными гепатоцитами и клетками гепатоцеллюлярного рака. Повышение уровня этого фактора до 100 нг/мл и более свидетельствует о возможном гепатоцеллюлярном раке.
РЭА и СА 19-9 имеют большое значение в диагностике и мониторировании больных холангиоцеллюлярным раком, а также выявлении больных метастатическим раком печени.
329
Для решения диагностических задач, которые должны ответить на вопросы, имеется ли в печени опухоль, требующая хирургического лечения и удалима ли опухоль печени, если опухоль удалима, каково функциональное состояние непораженной опухолью паренхимы печени и других жизненно важных систем организма: кардио-респираторной и мочевыделительной систем, свертывающей системы крови.
На сегодняшний день предлагается высокоинформативный комплекс диагностики, включающий ряд сложных инструментальных методов:
•ультрасонографиясприцельнойаспирационнойтонкоигольнойбиопсией
Метод позволяет лоцировать опухоли печени диаметром 1,5-2см и получить правильный диагноз в 87,5% случаев.Метод высокоинформативен в определении пораженной доли и сегментов печени, позволяет судить о состоянии ворот печени, инвазии опухоли в прилежащие к печени органы. Легко выявляются увеличенные лимфоузлы в гепатодуоденальной связке, панкреатодуоденальной зоне, асцит. Метод информативен в выявлении изменений внутрипеч¸ночных трубчатых структур. Информативность метода возрастает, если применяется ЦДК. Для каждого из сосудов печени свойственен характерный доплеровский сигнал. Имеется возможность выявить аномалии сосудов, выявить опухолевую деформацию, обструкцию сосудов, определить скорость кровотока в сосуде, что важно при прорастании опухолью воротной вены и артериовенозных шунтах. Методика тр¸х- мерного УЗИ позволяет получить объ¸мное изображение печени и расположенной в ней опухоли, а также дать объ¸мные характеристики не пора- ж¸нной опухолью части печени, что чрезвычайно важно при планировании хирургического лечения больного ПРП. Тр¸хмерная ультразвуковая реконструкция опухоли печени облегчает восприятие УЗ-изображений клиницистам. На современном этапе наиболее информативным методом в диагностике опухолей печени является эхоконтрастное исследование с волюметрической реконструкцией и оценкой изображения в отсроченную фазу.
• рентгеновская компьютерная томография
Информативным методом в диагностике опухолей печени является РКТ. Исследование следует проводить с контрастированием и без него (нативная РКТ). Для получения необходимого градиента концентрации рентгеноконтрастного препарата осуществляется его быстрое введение с помощью автоматического шприца, контрастное средство при этом перемещается по сосудистому руслу, длительно не смешиваясь с кровью (болюсное контрастирование). Стандартная РКТ точно указывает локализацию пораженных сегментов печени. При выполнении РКТ со спиральным сканированием визуализируются гиперваскулярные опухоли печени, к которым относится
330

гепатоцеллюлярная карцинома, гепатобластома, ангиосаркома и другие первичные злокачественные опухоли печени. Визуализируются и сосуды пече- ни. При нативной РКТ можно выявлять опухоли печени не менее 1см в диаметре. При спиральной КТ с болюсным контрастированием возможно выявлять 50% очагов в печени размерами менее 1см. Спиральная динами- ческая РКТ с контрастированием используется сразу при затруднениях в выявлении тромбоза воротной вены и ее ветвей, печеночных вен при ПРП с помощью УЗИ. При этом можно получить трехмерное изображение и оценить взаимосвязь сосудов с опухолью печени.
• ангиография печени
Выполняется после введения контрастного вещества в чревной ствол и(или) селективно в печеночную артерию для обнаружения патогномонич- ных для опухоли печени ангиографических симптомов – «ампутации сосуда», патологического сосудистого «клубка», экстравазальных «озер». Рентгенэндоваскулярное исследование позволяет определить характер опухоли и установить показания и границы резекции печени. Четкая визуализация печеночных артерий во время целиакографии, воротной вены и ее основных ветвей при возвратной сплено-мезентерикопортографии, НПВ при нижней каваграфии дают пока незаменимую информацию о сосудистой анатомии печени, об интактности или вовлеченности ворот печени в опухолевый процесс. Метод позволяет достоверно судить о резектабельности опухолевого процесса в печени. В случае выявления признаков нерезектабельности, может быть оставлен катетер в правом стволе или печеночной артерии для проведения регионарного лекарственного лечения.
• магнитно – резонансная томография (МРТ)
В диагностике первичных злокачественных опухолей печени и внутрипеченочных желчных протоков включает:
-динамическую МРТ с внутривенным контрастированием;
-бесконтрастную магнитно – резонансную ангиографию (МРА);
-трехмерные изображения.
Ядерно – магнитный резонанс имеет преимущества перед КТ при определении внутренней структуры опухоли и установлении взаимоотношения с магистральными сосудами и структурами. МРТ информативна в обнаружении внутрипеченочных отсевов опухоли, распространении опухоли на ворота печени, дифференциальной диагностике рака и хорошо васкуляризованных доброкачественных образований печени (узловая гиперплазия, аденома, гемангиома).
Томография с меченными 99mТс эритроцитами. При опухолях печени сосудистой природы однофазная эмиссионная КТ с меченными 99mТс эритро-
331
цитами выявляет длительное сохранение радиоактивности над опухолью, обусловленное задержкой в ней крови. Необходимость в однофазной эмиссионной компьютерной томографии с меченными 99mТс эритроцитами возникает при дифференциальной диагностике между образованием сосудистой природы и хорошо кровоснабжаемой опухолью не сосудистого происхождения.
ПЭТ (позитронная эмиссионная томография – диагностические возможности метода в гепатологии активно изучаются. Считается, что ПЭТ – высокоинформативный метод дифференциальной диагностики образований печени опухолевой и неопухолевой природы, определения распространенности злокачественного процесса.
• пункционная биопсия с визуализацией
Оуществляется под контролем УЗИ, РКТ, лапароскопии. Может выполняться неоднократно, в т.ч. в амбулаторных условиях. Осложнениями практически не сопровождается. Используются иглы длиной 10-15 см с наружным диаметром 0,7-1,2 мм (калибр 22-18 G). Значение пункции возрастает при нерезектабельности процесса. Проводить ее надо осторожно, поскольку опухоль обычно хорошо васкуляризована. При цитологическом исследовании асцитической жидкости опухолевые клетки, как правило, выявить не удается. Иногда для биопсии печени прибегают к лапароскопии или минилапаротомии. Такой подход позволяет заодно выявить больных с локализованной опухолью которым можно выполнить резекцию печени.
Выполнение базового диагностического комплекса, включающего методы неинвазивной визуализации, исследование крови на маркеры и пункционную цитобиопсию, почти всегда позволяет достоверно судить о морфологической структуре опухоли, ее размерах, долевой и сегментарной локализации, наличии асцита, распространенности на ворота печени, отсевах внутри печени, наличии опухолевых тромбов в ветвях воротной вены или печеночных венах, поражении лимфоузлов ворот печени и гепатодуоденальной связки, распространении опухоли на прилежащие к печени органы или отдаленных метастазах.
Методы оценки функционального состояния печени
Исследование функций печени необходимо для диагностики заболеваний и оценки тяжести поражения печени, для определения прогноза заболевания и возможности компенсации функций печени в период лечения и после него, в т.ч. после резекции печени и трансплантации органа, для осуществления контроля за эффективностью лечения.
332
Основные биохимические показатели крови, характеризующие функциональное состояние печени:
•билирубин
•щелочная фосфатаза (ЩФ)
Повышается при холестазе и в меньшей степени при первичном поражении гепатоцитов.
• гамма-глутамилтранспептидаза (гамма-ГТ)
Активность возрастает при холестатическом и паренхиматозном поражении печени. При холестазе гамма-ГТ повышается параллельно с щелоч- ной фосфатазой. При метастатическом поражении печени гамма-ГТ повышается чаще, чем щелочная фосфатаза.
• трансаминазы - аспартатаминотрансфераза (митохонадриальный фермент АсАТ)
Активность АсАТ повышается при любом остром повреждении паренхимы печени и других тканей и органов (скелетная мускулатура, миокард, почки).
- аланинаминотрансфераза (цитоплазматический фермент АлАТ) Поскольку АлАТ в гепатоцитах значительно больше, чем в клетках дру-
гих органов, его повышение более специфично для заболеваний печени.
• лактатдегидрогеназа (ЛДГ)
Малочувствительный показатель поражения печени. Значительное повышение активности ЛДГ отмечается при опухолевой поражении печени.
• альбумин (37-52 г/л)
Снижение концентрации может свидетельствовать о снижении белковосинтетической функции печени.
• фибриноген (2-6 г /л)
Белок острой фазы. Концентрация возрастает при остром поражении печени. При хронических заболеваниях печени различной этиологиии снижается.
• протромбиновое время (11-15 с)
Возрастает при диффузных поражениях печени различной этиологии.
•альфа-глобулин (6-10 г/л), бета-глобулин (7-11 г/л), гамма-глобулин (8-16 г/л)
Концентрация возрастает при различных поражениях печени, в т.ч. холестазе. Кореллируют с липопротеинами крови.
•мочевина (2,5-7,5 ммоль/л)
Снижение концентрации свидетельствует об угнетении образования мочевины в гепатоцитах из аминокислот.
333
• аминокислоты
Концентрация возрастает при всех заболеваниях печени, особенно характерно повышение концентрации метионина (>50 мкмоль/л) фенилаланина (>109 мкмоль/л), тирозина (>72 мкмоль/л).
• желчные кислоты (суммарно - 2,5-6,8 мкмоль/л).
Концентрация возрастает после приема пищи при различных поражениях печени. Высокочувствительный метод подтверждает поражение пе- чени, позволяет оценить ее выделительную функцию и наличие порто-си- стемного шунтирования крови.
• глюкоза (3,8-5,8 ммоль/ л)
При фульминантном некрозе печени содержание глюкозы снижается. При хронических диффузных заболеваниях печени нарушается толерантность к глюкозе.
• галактоза (2,2–3,3 ммоль/ л)
Тест толерантности – определение через 60 мин в сыворотке после приема 40 г в 250 мл воды. При хронических диффузных заболеваниях печени концентрация возрастает.
Иммуногистохимические тесты сыворотки крови
• ÀÔÏ (  10 ìêã/ë)
10 ìêã/ë)
Повышение в крови может свидетельствовать о гепатоцеллюлярном раке, хроническом гепатите и циррозе печени.
Иммуноглобулины классов G, М, А
Концентрация повышается из-за угнетения секвестрации антигенов в звездчатых клетках печени и нарушения катаболизма иммунных комплексов в печени. Уровень существенно возрастает при гепатитах и циррозах разной этиологии.
По показаниям, наряду с оценкой функционального состояния паренхимы печени, проводится изучение функционального состояния миокарда (ЭКГ, ЭхоКГ, велоэргометрия), функции внешнего дыхания (спирометрия, оценка эффективности альвеолярной вентиляции и диффузионной способности легких, КОС крови), почек и мочевыводящих путей (изучение клиренса креатинина, радиоизотопное исследование секреторно-экскретор- ной функции почек, экскреторная урография), свертывающей системы крови (коагулограмма) а также исследование крови на вирусы гепатитов В, С и др.
В результате решения указанных выше диагностических задач с высокой степенью вероятности можно судить о резектабельности опухоли и переносимости лечения.
Дифференциальная диагностика проводится со следующими заболеваниями:
•Доброкачественные опухоли печени
•Паразитарные заболевания
334
•Цирроз и гепатиты
•Кисты и абсцессы печени
•Метастатические опухоли
Лечение и прогноз у больных первичными злокачественными опухолями печени и внутрипеченочных желчных протоков
Для печеночноклеточного рака характерно быстро прогрессирующее течение. Без лечения большинство больных умирают через 3-6 мес после постановки диагноза. При раннем выявлении опухоли (путем регулярного определения уровня АФП и УЗИ) продолжительность жизни больных можно увеличить до 1-2 лет, а некоторым выполнить резекцию печени. Единственный шанс на излечение дает резекция печени, однако из-за цирроза печени, поражения обеих долей и отдаленных метастазов (в головной мозг, кости, надпочечники) она возможна лишь у немногих больных.
Для выбора лечебной тактики необходимо учитывать: 1. Характер опухоли:
-первичная;
-вторичная (метастатическая). 2. Распространенность опухоли:
-краевое расположение без связи с магистральными сосудами;
-расположение в глубине печени, связь с магистральными сосудами, наличие не менее 2 непораженных сегментов печени;
-тотальное поражение печени.
3. наличие осложнений:
-разрыв опухоли с внутрибрюшным кровотечением и/или истечением желчи;
-обтурация воротной и/или нижней полой вены;
-обтурационная желтуха.
Оценка операбельности опухоли печени имеет первоочередное значе- ние. Признаки неоперабельности могут быть обнаружены, как при лапаротомии или лапароскопии, так и с помощью КТ, МРТ и ангиографии. К ним относятся вовлечение обеих долей или четырех секторов печени, тромбоз воротной вены, инвазия или опухолевый тромб нижней полой вены, а также метастазы, в том числе регионарные лимфоузлы (их поражение подтверждают путем открытой биопсии).
335
Прогностические факторы
Если опухоль ограничена печенью, основное прогностическое значение имеют число опухолевых узлов и инвазия крупных сосудов. Выживаемость при операбельном печеночноклеточном раке зависит от следующих факторов:
1. Количество, размеры и локализация узлов.
-при одиночной опухоли 5-летняя выживаемость составляет 45%;
-при множественных – 15-25%;
-для опухоли размерами 2-5 см пятилетняя выживаемость составляет 40-45%, для более крупных – 10%;
-прогноз лучше у больных без цирроза печени и при локализации опухоли в левой доле или нижних (V и VI) сегментах правой доли.
2. Вовлечение вен. Все больные с опухолевыми тромбами в воротной или печеночных венах умирают в течении 3 лет, без поражения крупных сосудов 5-летняя выживаемость составляет 30%.
3. Объем и вид операции. При радикальной резекции печени 5-летняя выживаемость составляет 55% по сравнению с 5% при наличии остаточ- ной опухоли. После гемигепатэктомии пятилетняя выживаемость достигает 85%, после сегментэктомии – 50%, после краевой резекции – у оперированных больных 90% рецидивов возникают в печени.
4. Функциональные резервы печени также влияют на выживаемость. Их оценивают количественным методом исследования функции печени.
Практически значимыми являются две функциональные печеночные пробы.
Проба с индоцианином зеленым
Индоцианин зеленый удаляется из сосудистого русла только печенью в неконьюгированном виде. Клиренс индоцианина зеленого менее 0,4 мг/кг/ мин даже после экономных резекций печени ассоциируется с достоверно более высокой частотой острой печеночной недостаточности в послеоперационном периоде. Для больных, которым планируются обширные резекции печени, этот показатель должен быть не менее 1,0 мг/кг/мин. При удалении значительного объема непораженной опухолью печени этот показатель умножается на числовое (в %) выражение этого объема. Метод эффективный, безопасный, но дорогостоящий.
Исследование поглотительно – выделительной функции печени с помощью меченного радиоактивным технецием Brom Mesida. Функциональное состояние печени оценивается в цифровом выражении. Каждому цифровому уровню соответствует процент сохраненного функционального резер-
336
ва печени. Помимо вышеуказанных в практике применяются и другие методы количественного исследования функции печени: дыхательная проба с аминопирином, проба с лидокаином, проба с антипирином, бромсульфалеиновая проба.
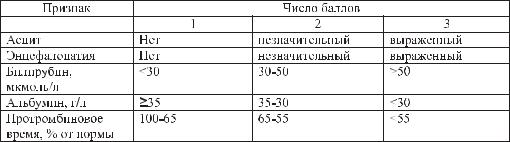
Существует система критериев оценки печеночноклеточной функции по Child-Pugh подразумевает три класса: А, В, С, определяемые по числу баллов.
Оценка печеночноклеточной функции
Класс А - 5-6 баллов; класс В – 7-9 баллов; класс С - 10 и более баллов.
Функциональные тесты при ПРП столь существенны, что преимущественно на их основе разработана классификация гепатоцеллюлярного рака (Okuda К. et al., 1984). Рассматриваемые в классификации признаки: асцит, объем опухоли более 50% печени, альбумин сыворотки крови меньше 30 г/л, общий билирубин сыворотки крови больше 30 мкмоль/л.
Классификация гепатоцеллюлярного рака по К. Okuda:
I стадия – указанные признаки отсутствуют; II стадия – не более 2 признаков;
III стадия – имеются все 4 признака.
Абсолютно точных функциональных тестов переносимости резекции печени нет. В практике является достаточным сочетание:
1)базовые биохимические показатели + система критериев Child-Pugh;
2)базовые биохимические показатели + один из методов количественной оценки функции печени (например, проба с индоцианином зеленым).
Для выбора лечебной тактики необходима следующая клиническая классификация:
1. Характер опухоли:
-первичная;
-вторичная (метастатическая).
337
2. Распространенность опухоли:
- краевое расположение без связи с магистральными сосудами; - расположение в глубине печени, связь с магистральными сосудами,
наличие не менее 2 непораженных сегментов печени; - тотальное поражение печени.
3. Наличие осложнений:
-разрыв опухоли с внутрибрюшным кровотечением и/или истечением желчи;
-обтурация воротной и/или нижней полой вены;
-обтурационная желтуха.
ÂРоссийском онкологическом научном центре им. Н.Н. Блохина РАМН
âотдельную классификацию выделены методы и виды лечения больных опухолями печени.
Классификация методов и видов лечения больных опухолями печени
I.Хирургическое лечение:
1)резекция печени;
2)гепатэктомия с ортотопической алло (ауто-) трансплантацией печени. II. Локальное аблативное и циторедуктивное лечение:
1)радиочастотная термодеструкция опухоли;
2)криодеструкция опухоли;
3)микроволновая фокусная деструкция опухоли;
4)ультразвуковая фокусная деструкция опухоли;
5)лазерная фокусная деструкция опухоли;
6)деструкция опухоли печени путем введения в опухоль этанола, уксусной кислоты, цистостатиков, радиоактивных изотопов;
7)другие виды локального циторедуктивного лечения;
8)сочетанное локальное циторедуктивное лечение.
III.Внутрисосудистое чрескатетерное (рентгеноэндоваскулярное) лечение:
1)эмболизация печеночной артерии (ЭПА);
2)химиоэмболизация печеночной артерии (ХЭПА);
3)масляная химиоэмболизация печеночной артерии (МХЭПА);
4)артерио – портальная химиоэмболизация;
5)химиоинфузия в печеночную артерию;
6)химиотерапия в воротную вену;
7)регионарная радиотерапия;
8)сочетанное внутрисосудистое чрескатетерное лечение.
338
