
- •15.03.04 «Автоматизация технологических процессов и производств» и
- •27.03.02 «Управление качеством» подготовки бакалавров Составитель г.Ю. Вострикова
- •Рецензенты:
- •Оглавление
- •Введение
- •Раздел 1. Основные химические понятия и стехиометрические законы Содержание материала для самостоятельного изучения
- •Основные теоретические положения
- •Решение типовых задач
- •Задачи для самостоятельного решения
- •Раздел 2. Квантово-механические представления
- •Основные теоретические положения
- •47 Ag 1s22s22p63s23p64s23d104p65s24d9 - неправильно,
- •47 Ag 1s22s22p63s23p64s23d104p65s14d10- правильно,
- •2.2. Химическая связь и строение молекул Содержание материала для самостоятельного изучения
- •Основные теоретические положения
- •Способы образования ковалентной связи
- •Решение типовых задач
- •Вопросы для семинарского занятия
- •2.3. Окислительно-восстановительные реакции Содержание материала для самостоятельного изучения
- •Основные теоретические положения
- •Решение типовых задач
- •Задачи для самостоятельного решения
- •Примерный вариант самостоятельной работы
- •Раздел 3. Общие закономерности химических процессов
- •3.1. Энергетика химических процессов
- •Содержание материала для самостоятельного изучения
- •Основные теоретические положения
- •Решение типовых задач
- •Задачи для самостоятельного решения
- •3.2. Химическая кинетика и равновесие Содержание материала для самостоятельного изучения
- •Литература: [1 – гл. 5, § 5.5; гл. 6, § 6.1; гл. 7, §§ 7.1 – 7.3]; [2 – гл.VI, §§ 57 – 61, 63]. Основные теоретические положения
- •Решение типовых задач
- •Задачи для самостоятельного решения
- •Вопросы для семинарского занятия
- •Раздел 4. Растворы. Дисперсные системы
- •4.1. Способы выражения количественного состава растворов Содержание материала для самостоятельного изучения
- •Литература: [1 – гл. 4, § 4.1]; [2 – гл. VII, §§ 73, 74]. Основные теоретические положения
- •Основные способы выражения концентрации
- •Решение типовых задач
- •0,5 Моль/л.
- •4.2. Общие свойства растворов Содержание материала для самостоятельного изучения
- •Основные теоретические положения
- •Решение типовых задач
- •Задачи для самостоятельного решения
- •Решение типовых задач
- •4.4. Водородный показатель рН. Гидролиз солей Содержание материала для самостоятельного изучения
- •Литература: [1 – гл. 8, §§ 8.5, 8.6]; [2 – гл.VII, §§ 90 – 92]. Основные теоретические положения
- •Решение типовых задач Задача 1. Вычислите рН раствора гидроксида кальция с молярной концентрацией 0,005 моль/л, считая диссоциацию Са(он)2 полной.
- •Из уравнения диссоциации следует, что
- •Задачи для самостоятельного решения
- •Объясните, написав уравнения реакций в молекулярной и ионно-молекулярной форме.
- •Вопросы для семинарского занятия
- •4.5. Гетерогенные дисперсные системы Содержание материала для самостоятельного изучения
- •Основные теоретические положения
- •Молекулы пав обозначают следующим символом:
- •Решение типовых задач
- •Задачи для самостоятельного решения
- •Тема 5. Электрохимические системы
- •5.1. Электродные потенциалы и электродвижущие силы Содержание материала для самостоятельного изучения
- •Основные теоретические положения
- •Стандартные электродные потенциалы в водных растворах при 298 к
- •Решение типовых задач
- •5.2. Электролиз Содержание материала для самостоятельного изучения
- •Основные теоретические положения
- •Решение типовых задач
- •5.3. Коррозия и защита металлов от коррозии Содержание материала для самостоятельного изучения
- •Основные теоретические положения
- •Решение типовых задач
- •Задачи для самостоятельного решения
- •Вопросы для семинарского занятия
- •Раздел 6. Технология и переработка полимеров
- •6.1. Методы получения, строение и свойства полимеров Содержание материала для самостоятельного изучения
- •Основные теоретические положения
- •Решение типовых задач
- •6.2. Переработка полимерных материалов Содержание материала для самостоятельного изучения
- •Некоторые представители композиционных материалов, применяемых в строительстве
- •Задачи для самостоятельного решения
- •Заключение
- •Библиографический список Основной
- •Дополнительный
- •15.03.04 «Автоматизация технологических процессов и производств»
- •3 94006 Воронеж, ул. 20-летия Октября, 84
Решение типовых задач
Задача 1. Составьте уравнение электролитической диссоциации веществ: KOH, HCl, H2CO3, Zn(OH)2, CuOHCl, Mg(HCO3)2. Для слабых электролитов напишите выражение констант диссоциации и укажите более слабый электролит.
Решение. В данном ряду KOH (щелочь), HCl (кислота), CuOHCl (основная соль), Mg(HCO3)2 (кислая соль) являются сильными электролитами. Для них уравнения электролитической диссоциации выглядят соответственно следующим образом:
KOH → K+ + OH‾ , HCl → H+ + Cl‾,
CuOHCl → CuOH+ + Cl‾,
Mg(HCO3)2 → Mg2+ + 2HCO3‾.
Угольная кислота и гидроксид магния – слабые электролиты, диссоциируют в две ступени. Каждая ступень диссоциации характеризуется своей константой (табл. 4.2).
Уравнения электролитической диссоциации слабых электролитов:
I
ступень:
H2CO3
H+
+ HCO3‾,
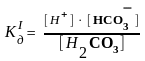 = 4,5 · 10–7
;
= 4,5 · 10–7
;
II
ступень:
HCO3‾
H+
+ CO32‾,
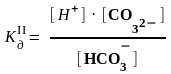 =
4,8 · 10–11
.
=
4,8 · 10–11
.
I
ступень:
Zn(OH)2
Zn OH+
+
OH‾
,
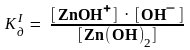 = 4,4
· 10–5
;
= 4,4
· 10–5
;
II
ступень:
ZnOH+
Zn
2+
+ OH‾,
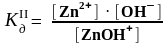 =
1,5 · 10–9
.
=
1,5 · 10–9
.
Так как величина константы диссоциации угольной кислоты меньше, чем гидроксида цинка, то H2CO3 является более слабым электролитом, чем Zn(OH)2.
Задача 2. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия между растворами BaCl2 и Na2SO4, Na2CO3 и H2SO4, CH3COONa и HCl, Fe(OH)3 и HNO3.
Решение. В растворах электролитов реакции происходят между ионами только в том случае, если в результате взаимодействия образуются слабые электролиты (табл. 4.2), труднорастворимые (табл. 4.3) или газообразные соединения
При составлении ионно-молекулярных уравнений эти соединения записывают в молекулярной форме, сильные растворимые электролиты – в виде ионов.
Для реакции:
BaCl2 + Na2SO4 →BaSO4↓+ 2NaCl (молекулярное уравнение),
р р н р
сильн.эл. сильн.эл. сильн.эл. сильн.эл.
Ba2+ + 2Cl‾ + 2Na+ + SO42‾ → BaSO4↓ + 2Na+ + 2Cl‾ (полное ионно- молекулярное уравнение),
Ba2+ + SO42‾ → BaSO4↓ (сокращенное ионно-молекулярное уравнение).
Реакция возможна, так как она сопровождается образованием труднорастворимого соединения BaSO4.
Na2CO3 + H2SO4 → Na2SO4 + H2O + CO2↑
р р р слаб.эл. газ
сильн.эл. сильн.эл. сильн.эл.
2Na+ + CO32‾+ 2H+ + SO42‾ → 2Na+ + SO42‾ + H2O + CO2↑
2H+ + CO32‾ → H2O + CO2↑.
Реакция протекает, так как сопровождается образованием газообразного соединения CO2 и слабого электролита H2O .
CH3COONa + HCl → CH3COOH + NaCl,
р р р р
сильн.эл. сильн.эл. слаб.эл. сильн.эл.
CH3COO‾ + Na+ + H+ + Cl‾ → CH3COOH + Na+ + Cl‾,
CH3COO‾ + H+ → CH3COOH.
В результате этой реакции образуется слабый электролит CH3COOH.
Fe(OH)3 + 3HNO3 Fe(NO3)3 + 3H2O
н р р слаб.эл.
слаб.эл. сильн.эл. сильн.эл.
Fe(OH)3 + 3H+ + 3NO3‾ Fe3+ + 3NO3‾+ 3H2O
Fe(OH)3 + 3H+ Fe3+ + 3H2O.
Реакция обратима, так как среди исходных веществ и среди продуктов реакции есть слабые электролиты.
