
- •Часть 1
- •Часть 1
- •Введение
- •Кинематика.
- •Динамика.
- •Динамика вращательного движения.
- •Элементы механики сплошных сред.
- •Релятивистская механика.
- •Термодинамика и статистическая физика.
- •Электричество и магнетизм.
- •Диэлектрики в электрическом поле.
- •Методические указания
- •Контрольная работа по физике №1
- •Студента группы рк-001
- •Шифр 257320
- •Иванова Петра Ивановича
- •1. Механика
- •Кинематика материальной точки
- •1.2.Кинематика поступательного и вращательного движения абсолютно твёрдого тела
- •Примеры решения задач по кинематике
- •Решение
- •Решение
- •Решение
- •1.3. Динамика материальной точки и поступательного движения абсолютно твердого тела
- •1.4. Динамика вращательного движения твердого тела
- •1.4.1. Момент инерции и момент импульса твердого тела
- •1.4.2. Момент силы. Основной закон динамики вращательного движения твердого тела
- •Примеры решения задач по динамике поступательного и вращательного движения тел
- •Решение
- •Решение
- •Решение
- •Решение
- •1.5. Механическая энергия, работа и мощность
- •1.5.1 Механическая работа и мощность при поступательном движении
- •1.5.2. Кинетическая и потенциальная энергия
- •1.5.3. Работа и мощность при вращательном движении
- •Примеры решения задач на работу и мощность
- •Решение
- •Решение
- •Решение
- •Решение
- •1.6. Законы сохранения
- •1.6.1. Закон сохранения импульса
- •1.6.2. Закон сохранения момента импульса
- •1.6.3. Закон сохранения механической энергии
- •Примеры решения задач на законы сохранения
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •1.7. Механика упругодеформируемых тел
- •1.7.1 Одноосное растяжение и сжатие
- •1.7.2. Сдвиг
- •Примеры решения задач на деформацию твердых тел
- •Решение
- •Решение
- •Решение
- •1.8. Механика жидкостей и газов
- •1.8.1. Идеальная жидкость. Уравнение неразрывности. Уравнение Бернулли
- •1.8.2. Вязкость. Ламинарный и турбулентный режимы течения жидкостей
- •Примеры решения задач на механику жидкостей
- •Решение
- •Решение
- •1.9. Основы релятивистской механики
- •1. 9.1. Преобразования координат и принцип относительности Галилея
- •1.9.2. Постулаты специальной теории относительности
- •1.9.3. Преобразования Лоренца. Следствия из преобразований Лоренца
- •1.9.4. Импульс и энергия в релятивистской механике
- •2. Молекулярная физика
- •2.1. Идеальный газ. Уравнение состояния идеального газа
- •2.2. Основное уравнение молекулярно-кинетической теории
- •2.3. Распределение молекул по скоростям
- •2.4. Барометрическая формула. Распределение Больцмана
- •2.5. Эффективный диаметр и средняя длина свободного пробега молекул
- •2.6. Явления переноса
- •Примеры решения задач по мкт
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •3. Термодинамика
- •3.1. Внутренняя энергия идеального газа. Равномерное распределение энергии по степеням свободы молекул
- •3.2. Теплота и работа. Первое начало термодинамики
- •3.3. Применение первого начала термодинамики к изопроцессам. Молярная теплоемкость идеального газа
- •3.4. Адиабатный процесс. Уравнение Пуассона
- •3.5. Круговые процессы. Цикл Карно. Второе начало термодинамики
- •3.6. Энтропия
- •Примеры решения задач по термодинамике
- •Решение
- •Решение
- •Решение
- •Решение
- •Р ешение
- •Решение
- •4. Электростатика
- •4.1. Электрический заряд. Закон сохранения электрического заряда. Закон Кулона
- •4.2. Электростатическое поле. Напряженность электростатического поля. Принцип суперпозиции полей
- •4.3. Линии напряжённости. Поток вектора напряжённости. Теорема Гаусса
- •4.4. Работа сил электрического поля. Потенциал
- •4.5. Эквипотенциальные поверхности. Связь между напряженностью и потенциалом
- •4.6. Проводники в электрическом поле
- •4.7. Диэлектрики в электрическом поле
- •4.8. Электроемкость уединенного проводника. Конденсаторы
- •4.9. Энергия электрического поля
- •Примеры решения задач по электростатике
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •5. Законы постоянного тока
- •5.1. Сила и плотность тока. Сторонние силы, эдс и напряжение
- •5.2 Обобщённый закон Ома. Дифференциальная форма закона Ома
- •5.3. Работа тока. Закон Джоуля - Ленца
- •5.4. Правила Кирхгофа и их применение к расчёту электрических цепей
- •Решение
- •Подставляя это выражение в (1), получим
- •Решение Из условия равномерности возрастания тока следует
- •Решение
- •Задачи для контрольных заданий
- •86. Азот находится при нормальных условиях. Найти:
- •Варианты контрольных заданий
- •Заключение
- •Приложения
- •1. Вычитание векторов
- •1. Скалярное произведение двух векторов
- •1. Векторное произведение двух векторов
- •2. Производная и дифференциал
- •2. Таблица простейших производных
- •2. Правила вычисления дифференциалов
- •3. Элементы интегрального исчисления Интегрирование– действие обратное дифференцированию
- •Неопределенный интеграл
- •4. Понятие градиента физической величины
- •5. Основные физические постоянные
- •6. Некоторые астрономические величины
- •7. Плотности ρ твёрдых тел, жидкостей и газов
- •8. Диэлектрическая проницаемость ε
- •9. Удельное сопротивление ρ и температурный коэффициент α проводимости
- •Библиографический список
- •Оглавление
- •1.1. Кинематика материальной точки………..………….………....8
- •1.4.1. Момент инерции и момент импульса твердого
- •1.5.1 Механическая работа и мощность при поступа-
- •2.5. Эффективный диаметр и средняя длина свободного
- •4.1. Электрический заряд. Закон сохранения электрического
- •Учебное издание
- •Краткий курс физики
- •Часть 1
- •3 94026 Воронеж, Московский просп., 14
Примеры решения задач по термодинамике
Пример
1. Найти среднюю кинетическую энергию
![]() вращательного движения одной молекулы
кислорода при температуре Т=350К,
а также кинетическую энергию Ек
враща- тельного движения всех молекул
кислорода массой
m = 4г.
вращательного движения одной молекулы
кислорода при температуре Т=350К,
а также кинетическую энергию Ек
враща- тельного движения всех молекул
кислорода массой
m = 4г.
Решение
На каждую
степень свободы молекулы газа приходится
одинаковая средняя энергия
![]() ,
где k
– постоянная Больцмана, Т
– термодинамическая температура газа.
Так как вращательному движению двухатомной
молекулы соответ- ствуют две степени
свободы, то средняя энергия вращатель-
ного движения молекулы кислорода равна
,
где k
– постоянная Больцмана, Т
– термодинамическая температура газа.
Так как вращательному движению двухатомной
молекулы соответ- ствуют две степени
свободы, то средняя энергия вращатель-
ного движения молекулы кислорода равна
![]() .
(1)
.
(1)
Кинетическая энергия вращательного движения всех молекул газа
![]() (2)
(2)
Число всех молекул газа
![]() ,
(3)
,
(3)
где NA – постоянная Авогадро; ν – количество вещества.
Если учесть, что количество вещества , где m – масса вещества; М – молярная масса газа, то формула (3) примет вид
![]() .
.
Подставив выражение для N в выражение (2), получим
![]() .
(4)
.
(4)
Учитывая, что для кислорода М = 32·10-3кг/моль, после подстановки числовых значений, получим:
![]() ;
;
![]() .
.
Пример 2. Определить отношение удельных теплоём- костей для смеси газов, содержащей гелий массой m1=8 г и водород массой m2 = 2 г.
Решение
Для
нагревания смеси газов массой
![]() на T при
постоянном объёме ей необходимо сообщить
количество теплоты
на T при
постоянном объёме ей необходимо сообщить
количество теплоты
![]() где
где
![]() -
удельная теплоёмкость смеси.
-
удельная теплоёмкость смеси.
Часть этого
количества теплоты,
![]() пойдёт на нагревание гелия, другая часть
пойдёт на нагревание гелия, другая часть
![]() - на нагревание водорода.
Тогда
- на нагревание водорода.
Тогда
![]() ,
,
![]()
Отсюда
![]() .
.
Аналогично находим ср смеси:
![]() .
.
Здесь
![]() ,
,![]() и
и
![]() ,
,![]() -
удельные теплоёмкости гелия и водорода
соответственно:
-
удельные теплоёмкости гелия и водорода
соответственно:
![]()
Так как гелий – газ одноатомный, то i1=3, водород – газ двухатомный, следовательно, i2=5.
Отношение удельных теплоёмкостей:

Подставляя выражение для удельных теплоёмкостей, получим:
 .
.
Пример
3. Кислород массой m
=2кг занимает объём V1=1м3
и находится под давлением P1
= 0,2 МПа. Газ был нагрет сначала
при постоянном давлении до объёма V2
= 3 м3, а затем при
постоянном объёме до давления P3
= 0,5 МПа. Найти изменение![]() внутренней
энергии газа, совершённую им работу и
теплоту Q, переданную
газу. Построить график процесса.
внутренней
энергии газа, совершённую им работу и
теплоту Q, переданную
газу. Построить график процесса.
Решение
Изменение внутренней энергии газа
![]() ,
(1)
,
(1)
где i
– число степеней свободы молекул
газа (для двухатомных молекул кислорода
i
=5);
![]() - разность температур газа в конечном
(третьем) и начальном состояниях.
- разность температур газа в конечном
(третьем) и начальном состояниях.
Начальную и
конечную температуру газа найдём из
уравнения Менделеева – Клапейрона
![]() ,
откуда
,
откуда
![]() ,
,
![]() ,
,
![]() .
.
Работа расширения газа при постоянном давлении выражается формулой
![]() .
.
Работа газа, нагреваемого при постоянном объеме равна нулю:
A2 = 0.
Следовательно полная работа , совершаемая газом равна
А = А1+А2 = А1.
Согласно первому началу термодинамики, теплота Q передаваемая газу, равна сумме изменения внутренней энергии и работы А:
![]()
Произведём вычисления, учтя, что для кислорода
M=32·10-3кг/моль, получим
![]() ;
;
![]() ;
;
![]() .
.
![]() ;
;
![]()
![]()
График процесса представлен на рисунке.
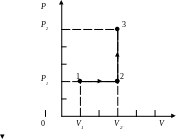
Пример 4. В цилиндре под поршнем находится водород массой m = 0,02 кг при температуре Т1 = 300К. Водород сначала расширялся адиабатно, увеличив свой объём в n1=5 раз, а затем был сжат изотермически, причём объём газа уменьшился в n2 =5 раз. Найти температуру в конце адиабати- ческого расширения и работу, совершаемую газом при этих процессах. Изобразить процесс графически.
