
- •1. Введение
- •2. Химическая коррозия
- •2.1 Показатели химической коррозии
- •2.2 Пленки продуктов коррозии и их свойства
- •2.3 Кинетика роста пленок
- •2 .4 Оксидные пленки и их свойства
- •2.5 Теория жаростойкого легирования
- •2.6 Факторы газовой коррозии
- •Внутренние
- •Внешние факторы
- •2.7 Защита от газовой коррозии
- •3. Электрохимическая коррозия
- •3.1 Термодинамика электрохимической коррозии
- •3.2 Схема электрохимической коррозии
- •А нодный
- •3.3 Местные гальванические элементы и причины их появления
- •3.4 Катодные процессы
- •3.5 Внутренние и внешние факторы электрохимической коррозии Внутренние факторы
- •Термодинамическая устойчивость и положение в периодической системе Менделеева
- •Состав и структура сплава
- •Внешние факторы
- •3 . Температура, давление и перемешивание
- •С увеличением давления скорость коррозии увеличивается, т.К. Увеличивается растворимость кислорода.
- •3.6 Понятие пассивности и ее значение для защиты металлов
- •4. Коррозия металлов в естественных условиях
- •4.1 Атмосферная коррозия
- •4.1.1 Типы атмосферной коррозии
- •Толщина пленки меняет течение катодных и анодных процессов. В зависимости от толщины возможен различный контроль:
- •4.1.2 Причины появления пленки влаги
- •4.1.3 Факторы атмосферной коррозии
- •4.1.4 Способы защиты
- •4.2 Подземная коррозия
- •4.2.1 Особенности подземной коррозии
- •4.2.2 Механизм
- •4.2.3 Вторичные продукты коррозии
- •4.2.4 Факторы подземной коррозии
- •4.2.5 Блуждающие токи
- •4.2.6 Методы защиты
- •4.3 Морская коррозия
- •4.3.1 Особенности морской коррозии
- •4.3.2 Характер разрушения
- •4.3.3 Механизм морской коррозии
- •4.3.4 Контроль
- •4.3.5 Факторы морской коррозии
- •4.3.6 Методы защиты
- •4.4 Коррозия металлов на металлургических предприятиях
- •5. Коррозия металлов в условиях эксплуатации
- •5.1 Межкристаллитная коррозия (мкк)
- •5.1.1Факторы мкк
- •5.1.2 Защита от мкк
- •5.2 Контактная коррозия
- •5.3 Щелевая коррозия
- •5.3.1 Способы защиты от щелевой коррозии
- •5.4.1 Типы питтинговой коррозии
- •5.4.2 Условия питтингообразования
- •5.4.3 Этапы питтингообразования
- •5.4.4 Факторы
- •5.4.5 Защита от питтингообразования
- •6. Защита металлов от коррозии
- •6.1 Защитные покрытия
- •Травление:
- •6.1.1 Металлические
- •Гальванический метод
- •Горячий метод
- •Плакирование.
- •Металлизация распылением
- •Диффузионные
- •6.1.2 Неметаллические покрытия
- •1.Лакокрасочные покрытия
- •6.2.1 Катодная защита
- •6.2.2 Анодная защита
- •6.3 Замедлители коррозии
- •Приложение
3.4 Катодные процессы
В подавляющем большинстве случаев, с которыми приходится иметь дело в практике, окисление металла в процессе коррозии осуществляется вследствие восстановления ионов водорода (водородная деполяризация) или растворенного в электролите кислорода воздуха (кислородная деполяризация). Водородная деполяризация характерна для коррозии электроотрицательных металлов преимущественно в кислых средах, а кислородная - для коррозии всех металлов, в том числе и электроотрицательных, как правило в нейтральных и щелочных средах .
Водородная деполяризация
Н+ + е → ½ Н2 φ ≈ 0,0 В
Характерна для металлов в кислых или нейтральных средах, имеющих большое отрицательное значение потенциала ( например : Mg φ = -2,37 В ).
φ ( Н+ / Н2) = -0,059 рН.
Сдвиг потенциала равновесного электрода в отрицательную сторону, зависящий от протекания тока, называют перенапряжением, которое характеризует трудность протекания катодной реакции. Перенапряжение описывается уравнением Тафеля.
η = a + b ∙ lg i ,
где b – коэффициент, который почти для всех металлов при восстановлении ионов из кислых растворов ≈ 0,12 ,
а – коэффициент, зависящий от природы металла.
аCd = 1,40 аZn = 1,24 аCu = 0,87 аFe = 0,70 аPt = 0,1
Водородная деполяризация существенно зависит от природы металла. Она не имеет диффузионных ограничений, перемешивание не ускоряет этот процесс. Повышение температуры снижает перенапряжение водорода.
Кислородная деполяризация
О2 + 4е + 2Н2О → 4ОН-
О2 + 4е + 4Н+ → 2Н2О
Равновесный потенциал реакции зависит от рН.
φ ( О2 / ОН- ) = 1,23 – 0,059 рН
Т.к. О2 имеет очень низкую растворимость (≈ 0,008 г/л), то при этой реакции возникают диффузионные ограничения. Концентрация О2 в растворе вблизи поверхности металла в слое Прандтля δ (толщиной δ = 10-3 10-2 см) - Сs.
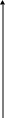 С
С


 С0
С0
1

СS 2



0 δ х
Рисунок 3.3 Изменение концентрации кислорода в слое Прандтля
В результате реакции разряда концентрация О2 в слое δ снижается со СS (кривая 1). При возрастании коррозионного тока концентрация О2 вблизи поверхности приближается к 0 (кривая 2) в этом случае достигается предельный диффузионный ток iд:
iд = 4FКд ∙Со/
С помощью уравнения Нернста сдвиг ∆ φ можно определить по следующей формуле:
∆ φ = RT/4F∙ ln (1 – i/iд),
где iд – предельный диффузионный ток.
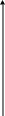 φ
φ
 3
3

 φ0
(Н+/
Н2)
φ0
(Н+/
Н2)

1
φ0 (О2 / ОН-)


iд i
Рис. 3.4 Полная кривая катодной деполяризации
УЧАСТОК 1. Определяется только скоростью разряда молекул О2 .
УЧАСТОК 2. С ростом скорости СS → 0 и достигается предельный диффузионный ток.
УЧАСТОК 3. При больших ∆ φ (когда φ достигает φ разряда Н2) определяется разрядом О2 и Н2 .
Положение участка 2 зависит от перемешивания и температуры. При перемешивании уменьшается толщина диффузионного слоя, а величина iд увеличивается.
При температуре t = 100 0С О2 полностью удаляется из раствора. Увеличение концентрации солей уменьшает растворимость О2 .
Наличие пузырьков Н2 вызывает перемешивание и ускорение процесса деполяризации.
При наличии в металле катодных включений скорость кислородной деполяризации зависит от их размера. При размере более 1-2 см - скорость коррозии пропорциональна площади включений.
i = k′ ∙ Sк -
Если Sк > δ, а размеры катодов менее 0,01 см, то скорость процесса пропорциональна линейному размеру катодов i = α∙Sk= к2 ∙r
где r – линейный размер.
