
- •Часть I
- •Содержание
- •Введение
- •Алканы, алкены, алкины. Способы получения, свойства
- •Получение алканов
- •2. Прямой синтез из элементов
- •Каталитическое гидрирование монооксида углерода
- •Синтезы индивидуальных парафинов
- •Химические свойства алканов
- •Г) Изомеризация, дегидрирование, ароматизация алканов
- •Получение алкенов
- •Химические свойства алкенов
- •Д) Реакции присоединения, протекающие против правила Марковникова
- •E) Окисление алкенов
- •З) Реакции полимеризации алкенов
- •Синтез ацетилена в промышленности, способы введения тройной связи
- •Химические свойства алкинов a) Реакции электрофильного присоединения
- •Б ) Присоединение галогенводородов по тройной связи идет по правилу Марковникова, труднее, чем к алкенам:
- •Д) Реакции с участием подвижного атома водорода в ацетилене
- •Е) Окисление ацетилена
- •В избытке окислителя может происходить полное разрушение молекулы алкина:
- •Ж) Димеризация и полимеризация ацетилена проходят каталитически.
- •Практическая работа № 1 получение и свойства метана, алкенов и ацетилена
- •2. Получение и исследование некоторых свойств алкенов
- •3. Получение ацетилена и исследование его свойств
- •Контрольные вопросы и задания
- •Реакции электрофильного замещения в ароматических соединениях
- •Типы электрофильных реагентов. Пути их образования
- •Эффекты замещения. Ориентанты I и II рода. Индуктивное и мезомерное влияние заместителей
- •Согласованная и несогласованная ориентация заместителей
- •Практическая работа № 2 свойства ароматических соединений получение мета-динитробензола
- •1. Окисление ароматических углеводородов
- •2. Качественная реакция на ароматические углеводороды
- •3. Синтез мета-динитробензола
- •Контрольные вопросы и задания
- •Реакции аренов, приводящие к неароматическим системам. Окислительные превращения
- •Практическая работа № 3 получение бензойной кислоты окислением арена
- •Контрольные вопросы и задания
- •Способы очистки твердых органических соединеий
- •Практическая работа № 4 очистка бензойной кислоты методом перекристаллизации, определение температуры плавления
- •1. Перекристаллизация
- •2. Определение температуры плавления
- •Контрольные вопросы и задания
- •Способы получения галогенпроизводных предельных углеводородов. Реакции нуклеофильного замещения
- •Практическая работа № 5 синтез бромистого алкила
- •1. Синтез бромистого алкила
- •2. Очистка вещества перегонкой при атмосферном давлении
- •Контрольные вопросы и задания
- •Правила техники безопасности при выполнении работ
- •Литература
- •Часть I
- •603950, Нижний Новгород, пр. Гагарина, 23
3. Получение ацетилена и исследование его свойств
Прежде чем непосредственно получать ацетилен, необходимо приготовить пробирки с бромной водой и разбавленным раствором перманганата калия, а также полоску фильтровальной бумаги, смоченную аммиачным раствором CuCl.
В сухую пробирку помещают небольшой кусочек карбида кальция, добавляют 3-4 капли воды, быстро закрывают отверстие пробирки газоотводной трубкой. Выделяющийся газ немедленно пропускают в раствор перманганата калия до изменения окраски раствора.
После этого также быстро пропускают выделяющийся газ в пробирку с бромной водой до обесцвечивания последней.
В конце реакции вводят полоску фильтровальной бумаги, смоченную аммиачным раствором CuCl, в отверстие реакционной пробирки.
Н-СС-Н + 2 CuCl Cu-СС-Cu + 2 НCl
Наблюдают, как фильтровальная бумага изменяет свою окраску вследствие образования ацетиленида меди.
Контрольные вопросы и задания
Объясните на конкретном примере, почему синтез Вюрца пригоден
только для получения симметрично-построенных алканов.
Могут ли существовать алкан, алкен или алкин с соотношением масс
углерода и водорода в молекуле, равным 7? Ответ аргументируйте.
Исходя из метана, не используя других органических соединений,
получите дифенилацетилен. Что получится в результате его
тримеризации? Приведите уравнения и условия реакций.
Содержание предельного углеводорода в смеси, состоящей из всех
углеводородов, содержащих по два атома углерода, составляет 32.8 %
по объему. 1 л такой смеси (н.у.) может присоединить 6.4 г Br2.
Найдите плотность смеси углеводородов (г/л).
5*. Смесь водорода и этиленового углеводорода общим объемом 13.44 л
(н.у.) пропустили над платиновым катализатором при 200 С, в
результате чего общий объем смеси уменьшился до 10.08 л (н.у.). При
пропускании исходной смеси через склянку с избытком бромной воды
масса склянки увеличилась на 11.2 г. Определите качественный и
количественный (в % по объему) состав исходной смеси, если
известно, что реакция на поверхности платинового катализатора
ротекала с выходом 75 % от теоретически возможного, а с бромной
водой – количественно.
Реакции электрофильного замещения в ароматических соединениях
Ароматические углеводороды (арены) представляют собой группу углеводородов, содержащих бензольное кольцо. Общая формула CnH2n-6. Бензольное кольцо обуславливает определенные физические и химические свойства, так называемый ароматический характер.
Характерными реакциями для ароматических углеводородов являются реакции замещения атома водорода бензольного кольца, называемые реакциями электрофильного замещения.
Примеры подобных реакций:
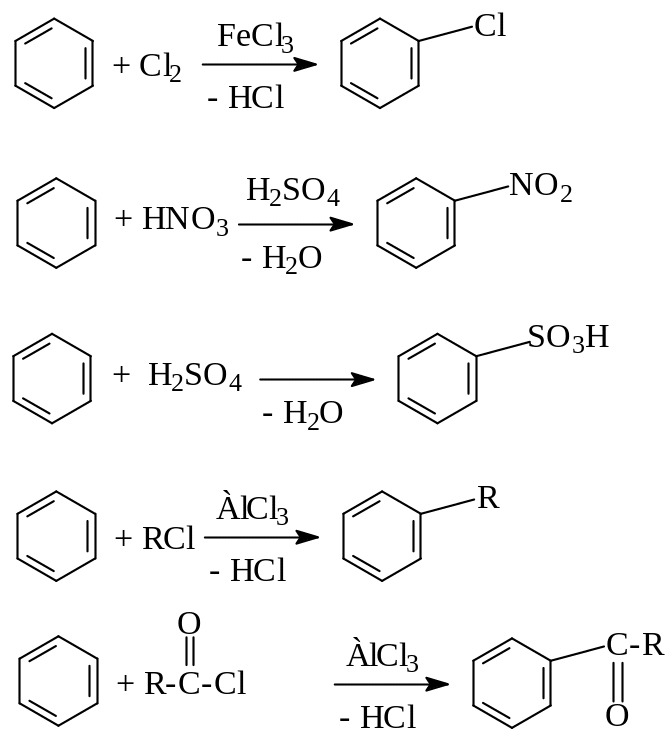
а) галогенирование
б) нитрование
в) сульфирование
г) алкилирование
д) ацилирование
Механизм электрофильного замещения двухстадиен:
Первой стадией атаки электрофильного реагента является образование -комплекса, в котором электрофильная частица, в наших примерах Cl+, NO2+, SO3H+, R+, RC(O)+, связывается с молекулой бензола за счет всех его -электронов:

быстро медленно
-комплекс -комплекс
Е+ вытягивает пару электронов на себя, образуя -комплекс.
На второй стадии -комплекс выбрасывает протон, восстанавливая ароматическую систему.
Самой медленной стадией реакции, определяющей ее скорость, является переход -комплекса в -комплекс.
