
- •Часть I
- •Содержание
- •Введение
- •Алканы, алкены, алкины. Способы получения, свойства
- •Получение алканов
- •2. Прямой синтез из элементов
- •Каталитическое гидрирование монооксида углерода
- •Синтезы индивидуальных парафинов
- •Химические свойства алканов
- •Г) Изомеризация, дегидрирование, ароматизация алканов
- •Получение алкенов
- •Химические свойства алкенов
- •Д) Реакции присоединения, протекающие против правила Марковникова
- •E) Окисление алкенов
- •З) Реакции полимеризации алкенов
- •Синтез ацетилена в промышленности, способы введения тройной связи
- •Химические свойства алкинов a) Реакции электрофильного присоединения
- •Б ) Присоединение галогенводородов по тройной связи идет по правилу Марковникова, труднее, чем к алкенам:
- •Д) Реакции с участием подвижного атома водорода в ацетилене
- •Е) Окисление ацетилена
- •В избытке окислителя может происходить полное разрушение молекулы алкина:
- •Ж) Димеризация и полимеризация ацетилена проходят каталитически.
- •Практическая работа № 1 получение и свойства метана, алкенов и ацетилена
- •2. Получение и исследование некоторых свойств алкенов
- •3. Получение ацетилена и исследование его свойств
- •Контрольные вопросы и задания
- •Реакции электрофильного замещения в ароматических соединениях
- •Типы электрофильных реагентов. Пути их образования
- •Эффекты замещения. Ориентанты I и II рода. Индуктивное и мезомерное влияние заместителей
- •Согласованная и несогласованная ориентация заместителей
- •Практическая работа № 2 свойства ароматических соединений получение мета-динитробензола
- •1. Окисление ароматических углеводородов
- •2. Качественная реакция на ароматические углеводороды
- •3. Синтез мета-динитробензола
- •Контрольные вопросы и задания
- •Реакции аренов, приводящие к неароматическим системам. Окислительные превращения
- •Практическая работа № 3 получение бензойной кислоты окислением арена
- •Контрольные вопросы и задания
- •Способы очистки твердых органических соединеий
- •Практическая работа № 4 очистка бензойной кислоты методом перекристаллизации, определение температуры плавления
- •1. Перекристаллизация
- •2. Определение температуры плавления
- •Контрольные вопросы и задания
- •Способы получения галогенпроизводных предельных углеводородов. Реакции нуклеофильного замещения
- •Практическая работа № 5 синтез бромистого алкила
- •1. Синтез бромистого алкила
- •2. Очистка вещества перегонкой при атмосферном давлении
- •Контрольные вопросы и задания
- •Правила техники безопасности при выполнении работ
- •Литература
- •Часть I
- •603950, Нижний Новгород, пр. Гагарина, 23
Типы электрофильных реагентов. Пути их образования
В любой реакции электрофильного замещения предварительной является стадия образования электрофильной частицы. Катализаторами данного процесса служат минеральные кислоты, кислоты Льюиса.
а) Нитрование
Используют нитрующую смесь – смесь азотной и серной кислот в соотношении 1 : 2:
H![]() O-NO2
+ 2 H2SO4
H3O+
+ 2 HSO4-
+ NO2+
или
O-NO2
+ 2 H2SO4
H3O+
+ 2 HSO4-
+ NO2+
или
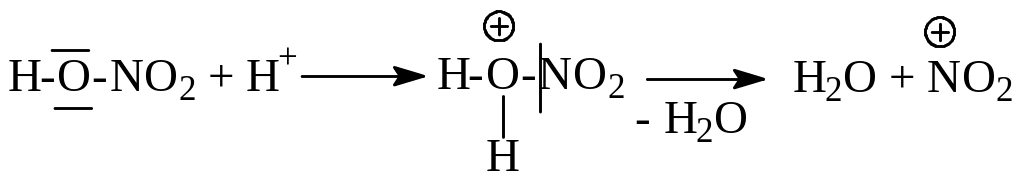
ион нитрония

нитробензол
б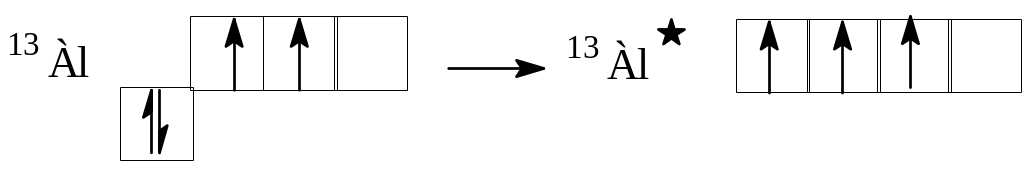 )
Галогенирование
проводят галогенами в
присутствии катализаторов
– кислот
Льюиса:
АlCl3,
АlBr3,
FeBr3
и т.д. – галогенидов металлов, центральный
атом которых имеет недостаток электронов
)
Галогенирование
проводят галогенами в
присутствии катализаторов
– кислот
Льюиса:
АlCl3,
АlBr3,
FeBr3
и т.д. – галогенидов металлов, центральный
атом которых имеет недостаток электронов

В полне
вероятно, что свободный Cl+
не образуется, а АlCl3
служит лишь для поляризации хлора:
полне
вероятно, что свободный Cl+
не образуется, а АlCl3
служит лишь для поляризации хлора:
+ -
-комплекс с участием хлорбензол
катализатора
В отсутствии катализатора при нагревании или освещении гомологов бензола идет гомолитическое замещение в боковую цепь:
Cl2, hv Cl2, hv Cl2, hv
C6H5-CH3 C6H5-CH2Cl C6H5-CHCl2 C6H5-CCl3
- HCl бензил- - HCl хлористый - HCl бензотри-
хлорид бензилиден хлорид
в) Ацилирование по Фриделю-Крафтсу:
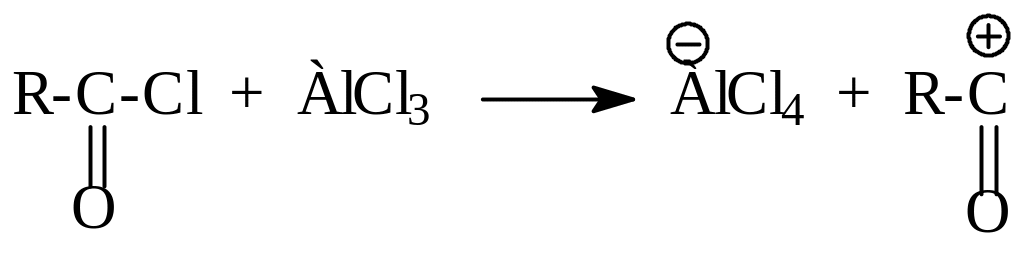
г) Алкилирование ароматических соединений можно провести галогеналкилами, спиртами или алкенами. При алкилировании спиртами или алкенами для получения карбкатионов используют кислотные катализаторы:

+ -
д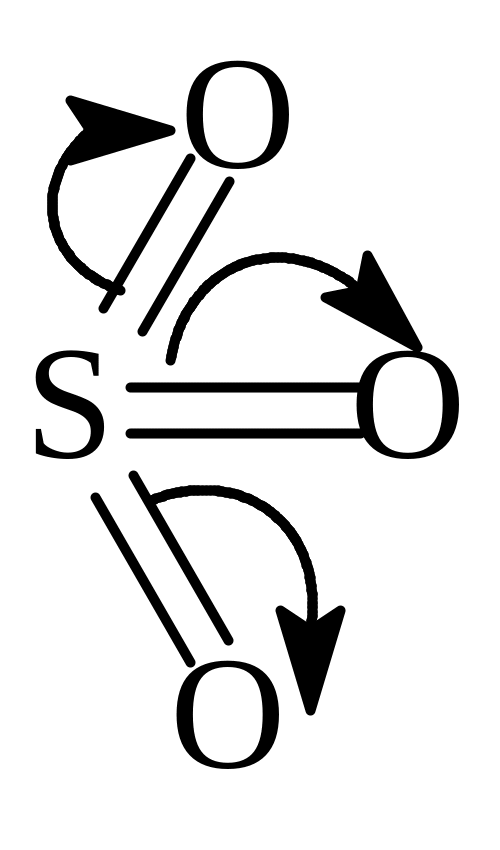 )
Сульфирование
проводят обычно серной кислотой,
содержащей избыток SO3.
Атом серы в оксиде серы(VI)
имеет дефицит электронной
)
Сульфирование
проводят обычно серной кислотой,
содержащей избыток SO3.
Атом серы в оксиде серы(VI)
имеет дефицит электронной
-
плотности: + -
-

бензолсульфо-
кислота
Сульфирование – необычная реакция, она обратима, причем равновесие сильно сдвинуто влево.
Эффекты замещения. Ориентанты I и II рода. Индуктивное и мезомерное влияние заместителей
Любая группа, связанная с ароматическим кольцом, влияет на его реакционную способность и определяет ориентацию замещения. Присутствие заместителя нарушает симметрию -системы, деформируя ее электронное облако, и связи С-Н в цикле становятся неравноценными. При этом в молекуле возникают три различных положения по отношению к уже существующему заместителю: орто-, пара и мета. Соответственно заместители в бензольном кольце делятся на 2 группы:
Заместители I рода – группировки атомов, способные отдавать электронную плотность (электронодонорные), под влиянием которых ядро становится более активным и которые направляют вхождение электрофильных агентов преимущественно в орто- и(или) пара-положение. Это – орто-, пара-ориентанты: -ОН, -OR, -NH2, -NR2, -R, галогены.
Р ассмотрим
влияние заместителей I
рода на примере
нитрования алкилбензолов:
ассмотрим
влияние заместителей I
рода на примере
нитрования алкилбензолов:
При R = CH3 61.4 % 37.0 %
При R = CH3CH2 45.9 % 50.8 %
Если ориентант I рода имеет на ключевом атоме свободную (неподеленную) пару электронов, то он передает ее в совместное пользование связанному с ним бензольному кольцу за счет +М-эффекта:

Заместители I рода, как правило, ускоряют реакции электрофильного замещения, то есть они являются активирующими заместителями. Исключением являются галогены, у которых –I-эффект превалирует над +М, поэтому галогены – дезактивирующие заместители. Однако, благодаря +М-эффекту, они орто-, пара-ориентанты.
Заместители II рода – группы, способные оттягивать электронную плотность бензольного кольца (электроноакцепторные) и направляющие входящий заместитель преимущественно в мета-положение. Это – дезактивирующие заместители: NO2, CN, SO3H, CF3, COOH, C(O)H.
Мета-ориентанты взаимодействуют с кольцом либо за счет индукционного, либо мезомерного эффектов:
- -
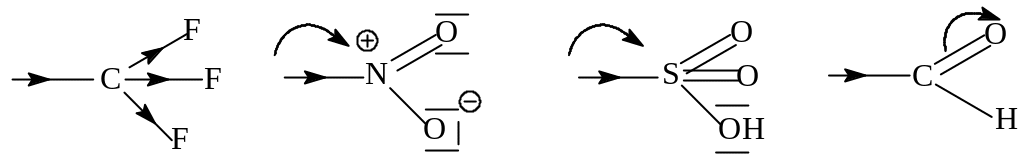 +
+
+
+
+
+
Следовательно, мета-ориентанты создают небольшой избыток электронной плотности в мета-положениях, но в целом являются дезактивирующими.
