
- •Часть I
- •Содержание
- •Введение
- •Алканы, алкены, алкины. Способы получения, свойства
- •Получение алканов
- •2. Прямой синтез из элементов
- •Каталитическое гидрирование монооксида углерода
- •Синтезы индивидуальных парафинов
- •Химические свойства алканов
- •Г) Изомеризация, дегидрирование, ароматизация алканов
- •Получение алкенов
- •Химические свойства алкенов
- •Д) Реакции присоединения, протекающие против правила Марковникова
- •E) Окисление алкенов
- •З) Реакции полимеризации алкенов
- •Синтез ацетилена в промышленности, способы введения тройной связи
- •Химические свойства алкинов a) Реакции электрофильного присоединения
- •Б ) Присоединение галогенводородов по тройной связи идет по правилу Марковникова, труднее, чем к алкенам:
- •Д) Реакции с участием подвижного атома водорода в ацетилене
- •Е) Окисление ацетилена
- •В избытке окислителя может происходить полное разрушение молекулы алкина:
- •Ж) Димеризация и полимеризация ацетилена проходят каталитически.
- •Практическая работа № 1 получение и свойства метана, алкенов и ацетилена
- •2. Получение и исследование некоторых свойств алкенов
- •3. Получение ацетилена и исследование его свойств
- •Контрольные вопросы и задания
- •Реакции электрофильного замещения в ароматических соединениях
- •Типы электрофильных реагентов. Пути их образования
- •Эффекты замещения. Ориентанты I и II рода. Индуктивное и мезомерное влияние заместителей
- •Согласованная и несогласованная ориентация заместителей
- •Практическая работа № 2 свойства ароматических соединений получение мета-динитробензола
- •1. Окисление ароматических углеводородов
- •2. Качественная реакция на ароматические углеводороды
- •3. Синтез мета-динитробензола
- •Контрольные вопросы и задания
- •Реакции аренов, приводящие к неароматическим системам. Окислительные превращения
- •Практическая работа № 3 получение бензойной кислоты окислением арена
- •Контрольные вопросы и задания
- •Способы очистки твердых органических соединеий
- •Практическая работа № 4 очистка бензойной кислоты методом перекристаллизации, определение температуры плавления
- •1. Перекристаллизация
- •2. Определение температуры плавления
- •Контрольные вопросы и задания
- •Способы получения галогенпроизводных предельных углеводородов. Реакции нуклеофильного замещения
- •Практическая работа № 5 синтез бромистого алкила
- •1. Синтез бромистого алкила
- •2. Очистка вещества перегонкой при атмосферном давлении
- •Контрольные вопросы и задания
- •Правила техники безопасности при выполнении работ
- •Литература
- •Часть I
- •603950, Нижний Новгород, пр. Гагарина, 23
Практическая работа № 5 синтез бромистого алкила
Как уже отмечалось, oдним из наиболее распространенных способов получения алкилгалогенпроизводных углеводородов в лабораторных условиях является взаимодействие спиртов с галогенводородами.
Цель работы:
синтезировать бромистый изопропил или бромистый этил
очистить полученное соединение перегонкой при атмосферном давлении
Оборудование: круглодонная колба на 250 мл, изогнутая стеклянная трубка, нисходящий холодильник Либиха, стаканы или колбы, делительная воронка, колба Вюрца, термометр, аллонж, кипелки.
1. Синтез бромистого алкила
KBr + H2SO4 HBr + KHSO4
R-OH + HBr R-Br + H2O
R = i-C3H7, C2H5
В круглодонную колбу на 250 мл осторожно наливают 37.5 мл концентрированной серной кислоты и при перемешивании добавляют 20 мл изопропилового ( = 0.785 г/мл) (или этилового, = 0.78 г/мл) спирта, охлаждая содержимое колбы под струей холодной воды. К охлажденной смеси, не прекращая перемешивания и охлаждения, добавляют 15 мл холодной воды и вновь охлаждают реакционную смесь до комнатной температуры. Затем вносят в колбу 30 г мелко измельченного бромистого калия.
С помощью изогнутой стеклянной трубки колбу c реакционной смесью присоединяют к холодильнику Либиха. Кончик аллонжа погружают в холодную воду, налитую в приемник. Колбу со смесью нагревают на газовой горелке, используя рассекатель. При этом выделяющийся бромистый алкил скапливается в приемнике под слоем воды в виде мутной жидкости. Реакцию считают законченной, когда под воду в приемник перестанут опускаться капельки галогеналкила.
Смесь из приемника переливают в делительную воронку, отделяют нижний слой галогеналкила в сухую чистую колбу и добавляют осушитель – безводный CaCl2. Вещество оставляют над осушителем на несколько часов.
2. Очистка вещества перегонкой при атмосферном давлении
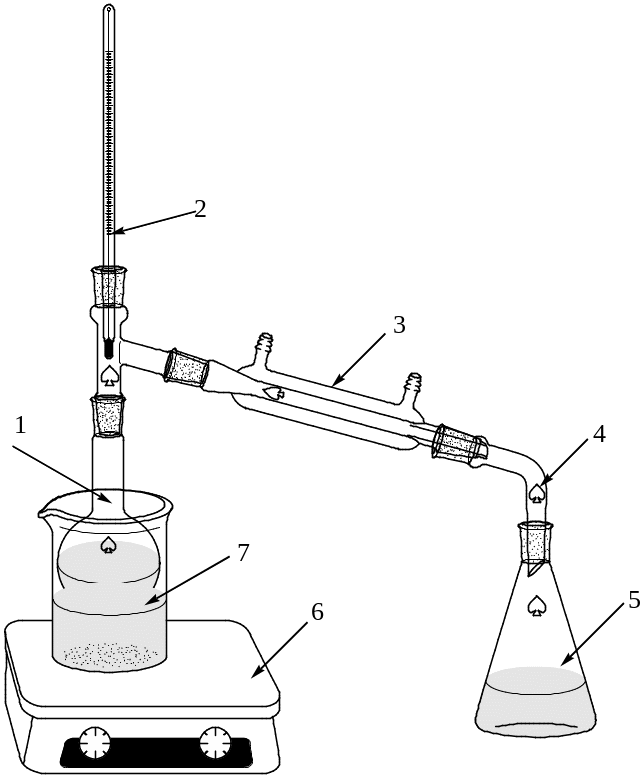
Высушенный бромистый изопропил (или бромистый этил) отфильтровывают в колбу Вюрца (1), помещают туда же несколько кипелок. Вставляют в верхнее отверстие термометр (2) на уровне бокового отвода таким образом, чтобы ртутный столбик полностью омывался парами кипящей жидкости.
Колбу нагревают (6) на водяной бане (7). Пары вещества попадают в отводную трубку колбы Вюрца и конденсируются в холодильнике Либиха (3). Как правило, в начале перегонки
температура кипения вещества несколько
ниже ее истинного значения, что может быть связано с наличием примесей, которые собирают в отдельную колбу. Как только значение температуры на термометре достигает нужного значения (57-60 С в случае бромистого изопропила и 35-39 С для бромистого этила), под аллонж (4) ставят в качестве приемника (5) сухую взвешенную колбу.
Перегонку ведут со скоростью 40-50 капель в минуту. Перегонять вещество из колбы Вюрца досуха нельзя.
По окончании перегонки взвешивают приемник с веществом.
Контрольные вопросы и задания
1. Запишите реакции, проходящие при действии на 3-бром-3,4-диметилпентан а) водного раствора КОН, б) NaNH2, в) спиртового раствора NaOH, г) (СН3)2СН-ОН.
2. Приведите еще, как минимум, две реакции получения бромистого изопропила, исходя из алкана и алкена. Запишите механизмы реакций.
3. Газ, выделившийся при получении бромбензола из 22.17 мл бензола (плотность 0.8 г/мл), ввели в реакцию с 4.48 л (н.у.) изобутилена. Какие соединения образовались и какова их масса, если учесть, что выход бромбензола составляет 80 % от теоретического, а реакция с изобутиленом идет количественно?
4. Алкен присоединяет 6.72 л (н.у.) хлороводорода. В результате гидролиза продукта реакции водным раствором гидроксида натрия при нагревании образовалось 22.2 г предельного одноатомного спирта. Определите возможное строение исходных и конечных соединений, удовлетворяющих условию задачи.
5*. Смесь изомерных дихлорэтанов нагрели со спиртовым раствором щелочи. Выделившийся газ пропустили в аммиачный раствор оксида серебра, при этом выпало 9.60 г осадка. При обработке такого же количества исходной смеси водным раствором щелочи получена смесь, при действии на которую аммиачного раствора оксида серебра выпало 6.48 г осадка. Определите массу исходной смеси и мольную долю каждого компонента в ней.
