
- •Часть I
- •Содержание
- •Введение
- •Алканы, алкены, алкины. Способы получения, свойства
- •Получение алканов
- •2. Прямой синтез из элементов
- •Каталитическое гидрирование монооксида углерода
- •Синтезы индивидуальных парафинов
- •Химические свойства алканов
- •Г) Изомеризация, дегидрирование, ароматизация алканов
- •Получение алкенов
- •Химические свойства алкенов
- •Д) Реакции присоединения, протекающие против правила Марковникова
- •E) Окисление алкенов
- •З) Реакции полимеризации алкенов
- •Синтез ацетилена в промышленности, способы введения тройной связи
- •Химические свойства алкинов a) Реакции электрофильного присоединения
- •Б ) Присоединение галогенводородов по тройной связи идет по правилу Марковникова, труднее, чем к алкенам:
- •Д) Реакции с участием подвижного атома водорода в ацетилене
- •Е) Окисление ацетилена
- •В избытке окислителя может происходить полное разрушение молекулы алкина:
- •Ж) Димеризация и полимеризация ацетилена проходят каталитически.
- •Практическая работа № 1 получение и свойства метана, алкенов и ацетилена
- •2. Получение и исследование некоторых свойств алкенов
- •3. Получение ацетилена и исследование его свойств
- •Контрольные вопросы и задания
- •Реакции электрофильного замещения в ароматических соединениях
- •Типы электрофильных реагентов. Пути их образования
- •Эффекты замещения. Ориентанты I и II рода. Индуктивное и мезомерное влияние заместителей
- •Согласованная и несогласованная ориентация заместителей
- •Практическая работа № 2 свойства ароматических соединений получение мета-динитробензола
- •1. Окисление ароматических углеводородов
- •2. Качественная реакция на ароматические углеводороды
- •3. Синтез мета-динитробензола
- •Контрольные вопросы и задания
- •Реакции аренов, приводящие к неароматическим системам. Окислительные превращения
- •Практическая работа № 3 получение бензойной кислоты окислением арена
- •Контрольные вопросы и задания
- •Способы очистки твердых органических соединеий
- •Практическая работа № 4 очистка бензойной кислоты методом перекристаллизации, определение температуры плавления
- •1. Перекристаллизация
- •2. Определение температуры плавления
- •Контрольные вопросы и задания
- •Способы получения галогенпроизводных предельных углеводородов. Реакции нуклеофильного замещения
- •Практическая работа № 5 синтез бромистого алкила
- •1. Синтез бромистого алкила
- •2. Очистка вещества перегонкой при атмосферном давлении
- •Контрольные вопросы и задания
- •Правила техники безопасности при выполнении работ
- •Литература
- •Часть I
- •603950, Нижний Новгород, пр. Гагарина, 23
З) Реакции полимеризации алкенов
Одним из наиболее важных для современной промышленности превращений алкенов является реакция полимеризации, открытая А.М. Бутлеровым.
Полимеризация – это процесс образования высокомолекулярного вещества (полимера) путем соединения молекул алкена (мономера) вследствие разрыва двойных связей:

Полимеризация может быть вызвана нагреванием, сверхвысоким давлением, облучением, действием катализаторов.
Реакция полимеризации включает 3 стадии: инициирование, cтадию роста, cтадию обрыва цепи.
Полимеризация алкенов в зависимости от механизма может быть двух видов: радикальная или инициированная и ионная или каталитическая (катионная или анионная).
Полиэтилен имеет n = 100 – 1000 звеньев этилена (полиэтилен высокого давления, ПЭВД), используется для производства труб, пленки и т.п. Пропилен и изобутилен с трудом полимеризуются по свбодно-радикальному механизму.
В 1953 г. К. Циглер (Институт Макса Планка, ФРГ) осуществил полимеризацию этилена при комнатной температуре и обычном давлении в растворе предельного углеводорода. В качестве катализатора он использовал триэтилалюминий (C2H5)3Аl c добавками TiCl4.
(C2H5)3АlTiCl4 – катализатор Циглера
(C2H5)3АlTiCl3 – катализатор Дж. Натта (Миланский политехнический институт, Италия)
(C2H5)3Аl TiClх – катализатор Циглера-Натта (x = 3, 4)
Молекулярная масса 3 000 000 - 5 000 000 ед. – более высокомолекулярный полимер (полиэтилен низкого давления, ПЭНД).
За открытие этих катализаторов К. Циглер и Дж. Натта в 1963 г. были удостоены Нобелевской премии по химии.
Алкины – углеводороды общей формулы СnH2n-2, содержащие в своем составе тройную связь.
Синтез ацетилена в промышленности, способы введения тройной связи
Основным сырьем для получения ацетилена в промышленности являются уголь, нефть и природный газ.
а) Синтез из карбида кальция:
Карбид кальция в промышленности получают сплавлением негашеной извести с углем в электрических печах при температуре 2500-3000 С:
СаО + 3 С СаС2 + СО
Карбид кальция бурно реагирует с водой с выделением ацетилена:
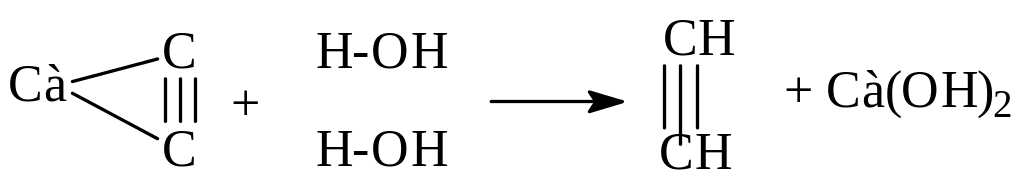
Метод освоен еще в прошлом веке и используется как в лабораторных условиях, так и в промышленности. Однако, получаемый таким способом ацетилен очень дорогой, поскольку получение СаС2 требует больших затрат электроэнергии.
б) Пиролиз метана до ацетилена осуществляют путем нагревания очищенного метана до 1500 С. При этом происходит образование ацетиленоводородной смеси:
1400 - 1500 С
2 СН4 СНСН + 3 Н2
Реакция эндотермична, поэтому метод тоже дорогой.
Из гомологов метана ацетилен получается при более низкой температуре:
1200 С
С2Н6 СНСН + 2 Н2
1200 С
2 С3Н8 3 СНСН + 5 Н2
в) Синтез ацетиленовых углеводородов из алкенов
Дигалогеналканы, содержащие оба атома галогена у соседних атомов углерода, отщепляют 2 молекулы галогенводорода при обработке спиртовым раствором гидроксида калия:
KOH KOH
CH3-CH=CH2 + Br2 CH3-CHBr-CH2Br CH3-CH=CHBr
спирт. спирт.
CH3-CCH + KBr + H2O
пропин
Можно получить алкины из галогенпроизводных, содержащих 2 атома галогена у одного атома углерода:
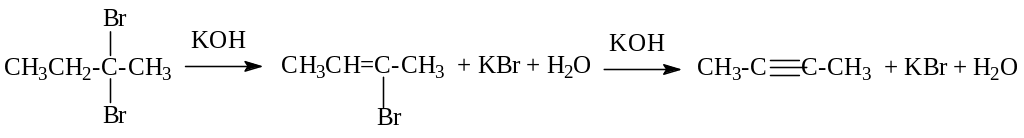
бутин-2
г) Алкилирование металлических производных ацетилена
Ацетилен и моноалкилацетилены R-CCH имеют достаточно кислые атомы водорода, способные замещаться на металлы:
C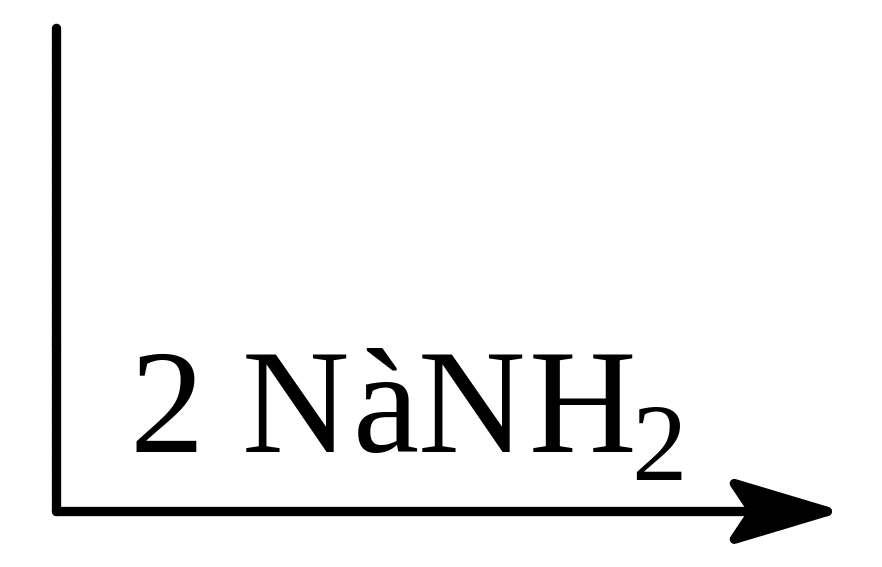 HCH
+ NаNH2
2 HCC-Nа
+ NH3
HCH
+ NаNH2
2 HCC-Nа
+ NH3
ацетиленид натрия
Nа-CC-Nа + 2 NH3
динатрийацетиленид
Если на ацетилениды действовать галогеналкилами, можно получить гомологи ацетилена:
HCC-Nа + С3Н7Br HCC-С3Н7 + NаBr
пентин-1
Nа-CC-Nа + 2 С2Н5Br С2Н5-CC-С2Н5 + 2 NаBr
гексин-3
