
- •А. С. Сіньковський
- •Теорія та методи
- •Напилення
- •Курс лекцій
- •Затверджено
- •Isbn 966-8335-02-3 © Наука і техніка, 2010 лекція 1
- •Вакуумні методи напилювання покриттів
- •Лекція 2 Умови та технологія процесу вакуумного напилення
- •Лекція 3 Підвищення технологічних параметрів процесу нанесення вакуумних покриттів
- •Лекція 4 Способи та технологічні особливості конденсаційного напилювання покриттів вибухом розпилюваного матеріалу
- •Лекція 5 Вакуумне конденсаційне напилювання покриттів іонним розпиленням
- •Лекція 6 Обладнання для вакуумного напилювання покриттів
- •2. Газотермічні методи напилювання покриттів лекція 7 Плазма. Процеси, що відбуваються в плазмі
- •Лекція 8 Потік плазми. Плазмово–дугове та плазмово–струменеве напилення
- •Лекція 9 Плазмотрони, їхні конструктивні відмінності та властивості
- •Лекція 10 Джерела плазмової дуги деяких промислових установок
- •Лекція 11 Методи забезпечення газотермічних установок газами
- •Лекція 12 Порошкові живильники-дозатори
- •Лекція 13 Установки для плазмового напилення
- •При наближенні до галтелі швидкість переміщення розпилювача
- •Лекція 14 Газополуменеве напилювання
- •Лекція 15 Обладнання для газополуменевого напилювання покриттів
- •Лекція 16 Електродугова металізація
- •Лекція 17 Способи та технологічні особливості електродугової металізації
- •Лекція 18 Умови електродугової металізації
- •Лекція 19 Вплив зовнішніх факторів на електродугову металізацію
- •Лекція 20 Детонаційне нанесення покриттів
- •Лекція 21 Основні енергетичні та зовнішні параметри процесу детонаційного напилення покриттів
- •Лекція 22 Високочастотна металізація
- •3. Двофазні потоки, що утворюються при газотермічних методах напилення лекція 23 Характеристика двофазних потоків при газотермічному напиленні. Теорія подібності
- •Лекція 24 Надзвукові струмені
- •Лекція 25 Порівняння різних типів струменів
- •Лекція 26 Металургійні процеси при газотермічному напиленні (гтн) покриттів
- •Лекція 27 Взаємодія частинок розпилюваного матеріалу з газовою фазою
- •Лекція 28 Взаємодія газової фази з вологою і воднем та азотом
- •Лекція 29 Взаємодія твердої фази з воднем та азотом
- •Лекція 30 Газодинамічний метод нанесення покриттів
- •25.2. Струмені плазми
- •30.3 Метод газодинамічного напилення
- •Запитання
- •4. Процеси, що протікають при утворенні покриттів, та їхня структура
- •Лекція 31
- •Вплив зовнішніх факторів на міцність
- •Зчеплення покриття з основою
- •Лекція 32 Механізм та кінетика фізико-хімічних процесів, що ведуть до міцного зчеплення напилюваних частинок
- •Лекція 33 Структурна будова покриттів
- •5. Технологія нанесення, обробки та контролю газотермічних покриттів лекція 34 Технологія нанесення газотермічних покриттів
- •Лекція 38. Контроль якості напилених покриттів
- •38.1. Загальна характеристика методів контролю
- •Існуючі методи контролю якості напилених покриттів можна розділити на неруйнувальні та руйнувальні.
- •Лекція 39. Техніка безпеки і охорона праці при газотермічному напиленні покриттів
- •Лекція 40 Області використання газотермічних покриттів та економічна доцільність їхнього нанесення
- •Штучний супутник землі
- •Сопла реактивних двигунів і ракет
- •Список літератури
- •Анатолій Степанович Сіньковський Теорія та методи напилення курс лекцій
- •Одеський національний політехнічний університет
- •65044, Одеса, пр. Шевченка, 1
- •65044, Одеса, пр. Шевченка, 1, корп. 5.
2. Газотермічні методи напилювання покриттів лекція 7 Плазма. Процеси, що відбуваються в плазмі
7.1. Плазма та її основні характеристики.
Плазма в перекладі з грецької – plasma – виліплення, оформлення. Плазмою називають іонізований квазінейтральний газ.
Термін “плазма” введений в 1929 р. Ленглюром.
Якщо газ, молекули якого складаються із кількох атомів, нагріти (наприклад в електричній дузі), до температури >1000 оС, то відбудеться процес руйнування молекулярних зв`язків і газ переходитиме в атомний стан.
Кількість молекул які розпалися зростатиме зі збільшенням температури і тиску . Наприклад , для азоту можна записати:
![]() ,
,
де
![]() – енергія дисоціації , яку виражають
еВ
– енергія дисоціації , яку виражають
еВ
![]()
Ступінь дисоціації визначається коефіцієнтом , який являє собою відношення числа дисоційованих молекул до загального числа молекул в одиниці об`єму.
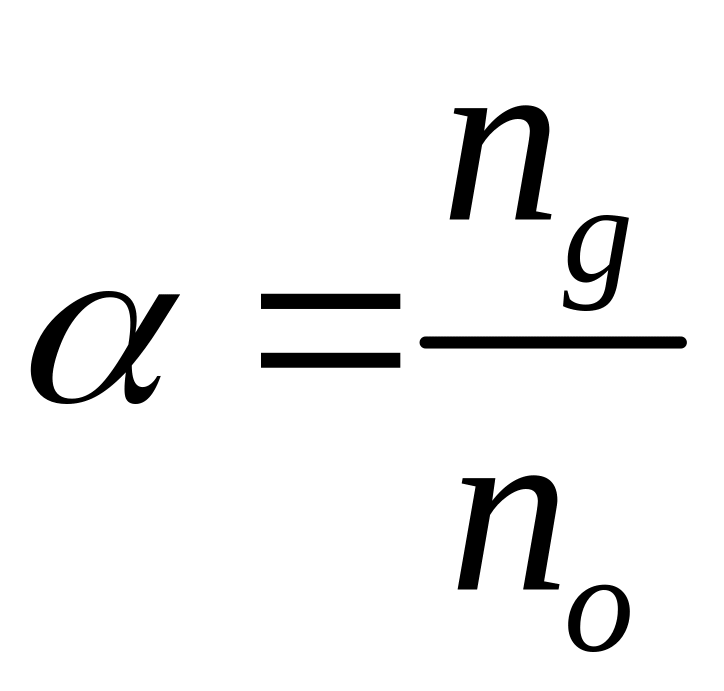 ,
(7.1)
,
(7.1)
де
![]() – число дисоційованих молекул ,
– число дисоційованих молекул ,
![]() - число всіх молекул в одиниці об`єму.
- число всіх молекул в одиниці об`єму.
Значення енергій дисоціації для найбільш використовуваних газів наведені в табл. 7.1
Таблиця 7.1
Газ |
Енергія дисоціації, еВ |
Енергія дисоціації, Дж. |
H2 N2 O2 CO NO OH CO2 H2O |
4.4777 9.76 5.08 11.11 6.48 4.37 6.56 12.59 |
7.163 15.616 8.128 17.776 10.368 6.992 26.496 20.144 |
При подальшому підвищенні дисоційованого газу від атомів відриваються електрони і здійснюється процес іонізації. При температурах Т>10000 оК такі гази, як кисень і азот, є досить іонізованими. Так, для азоту:
![]()
де
![]() – енергія іонізації одного атома, еВ.
– енергія іонізації одного атома, еВ.
Ступінь
іонізації характеризується коефіцієнтом
![]() ,
який є відношенням кількості іонізованих
атомів (сума пар частинок різного знака)
до загальної кількості атомів в одиниці
об`єму:
,
який є відношенням кількості іонізованих
атомів (сума пар частинок різного знака)
до загальної кількості атомів в одиниці
об`єму:
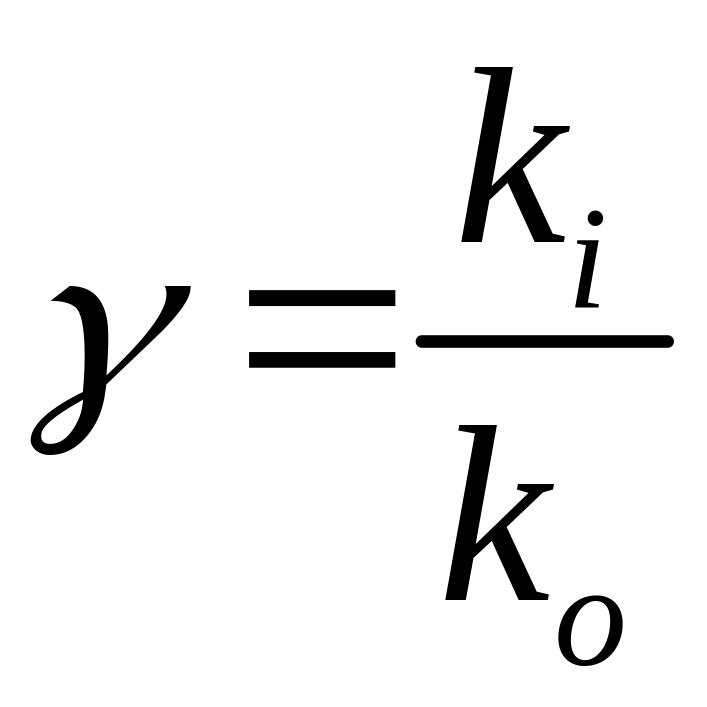 ,
(7.2)
,
(7.2)
де
![]() –
число іонізованих атомів;
–
число іонізованих атомів;
![]() – кількість всіх атомів в одиниці
об`єму.
– кількість всіх атомів в одиниці
об`єму.
Для
газорозрядної плазми високого тиску
характерна концентрація електронів
![]() , що відповідає ступені іонізації
, що відповідає ступені іонізації
![]() .
.
Повністю іонізована плазма може бути одержана при умові , що
![]() ,
(7.3)
,
(7.3)
де
k – постійна Больцмана
![]() ,
Т – абсолютна температура ,
,
Т – абсолютна температура ,
![]() ;
;
![]() –
потенціал іонізації газу .
–
потенціал іонізації газу .
Потенціалом
іонізації
називається різниця потенціалів, яку
має пройти електрон у прискорюючому
електричному полі, щоб його енергія
досягла значення роботи іонізації
![]() ,
тобто
,
тобто
![]() , де е – заряд електрона.
, де е – заряд електрона.
Для
водню температура повної іонізації
становить
![]() .
.
Енергія іонізації залежить від глибини процесу, тобто від кількості відірваних електронів. Тому розрізняють первинну, вторинну , третинну і тощо іонізацію. Чим вища ступінь іонізації, тим більша робота (табл. 7.2)
Таблиця 7.2
Енергія іонізації, еВ |
||||||
Газ |
Ступені іонізації |
|||||
1 |
2 |
3 |
4 |
5 |
6 |
|
Ar He H Kr N O Xe |
15.777 24.58 13.595 13.99 14.54 13.614 12.13 |
27.62 54.4 ------ 24.56 29.6 35.146 21.2 |
40.9 ------ ------ 36.9 47.426 54.934 ----- |
59.79 ------- ------- ------- 77.45 77.394 ------- |
75 ----- ----- ----- 97.963 113.873 ----- |
91.3 ----- ----- ----- 551.92 138.08 ----- |
При іонізації і дисоціації водню та азоту, а також при іонізації гелію та аргону відбувається поглинання енергії. А при охолодженні плазми протікає зворотний процес рекомбінації і деіонізації газу.
Якщо
у першому випадку енергія поглиналась,
то у другому вона буде виділятись. При
цьому двохатомні гази виділяють енергії
більше, ніж одноатомні.. Чим менша площа,
на якій виділяється енергія,
тим більша її концентрація. У ідеальному
випадку
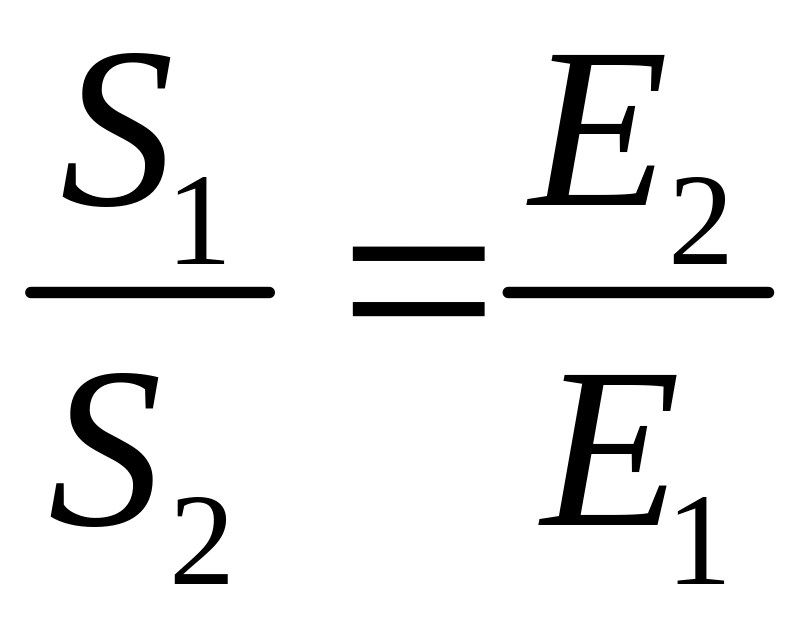 ,
,
де
![]() – поперечний розріз струменю плазми в
районі виходу її з плазмотрона,
– поперечний розріз струменю плазми в
районі виходу її з плазмотрона,
![]() – в області дуги на відстані
від плазмотрона.
– в області дуги на відстані
від плазмотрона.
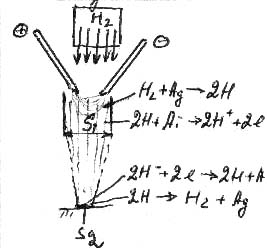
Рис.
7.1 Процеси, що відбуваються в плазмі:![]() – затрачена енергія на одиницю площі
;
– затрачена енергія на одиницю площі
;
![]() – енергія, що виділяється на одиницю
площі
– енергія, що виділяється на одиницю
площі
7.2. Види плазми
Залежно
від температури плазма буває
низькотемпературна
![]() і високотемпературна
і високотемпературна
![]() .
Остання складається із дейтерію і
тритію, якщо плазмоутворюючим газом є
водень. Така плазма вивчається з метою
одержання керованої ядерної реакції .
.
Остання складається із дейтерію і
тритію, якщо плазмоутворюючим газом є
водень. Така плазма вивчається з метою
одержання керованої ядерної реакції .
Залежно від співвідношення середньої відстані між частинками, амплітуди кулонівського розсіювання частинок і дебройлівської довжини хвилі розрізняють плазму класичну і квантову, або ідеальну і неідеальну.
У
розглянутих діапазонах тиску
![]() і діапазонах температур
і діапазонах температур
![]() плазма може дещо відрізнятися від
класичної.
плазма може дещо відрізнятися від
класичної.
Критерієм збереження ідеальності реального одноатомного нейтрального газу є умова:
![]()
де
![]() – середня енергія взаємодії атомів; k
–
постійна Больцмана , Т – абсолютна
температура °К.
– середня енергія взаємодії атомів; k
–
постійна Больцмана , Т – абсолютна
температура °К.
У фізиці температуру плазми часто виражають в енергетичних одиницях, наприклад в електронвольтах, яка зв’язана з температурою Кельвіна відношенням
![]() ,
(7.4)
,
(7.4)
де е - елементарний заряд.
Таким чином, один електрон-вольт відповідає температурі в °К
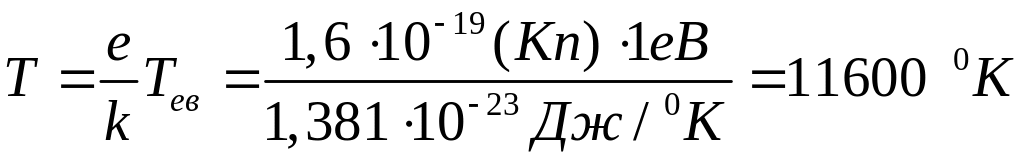
Для ідеальності повністю іонізованого газу, що складається із заряджених частинок різних знаків, які взаємодіють між собою за законом Кулона, повинна виконуватись умова:
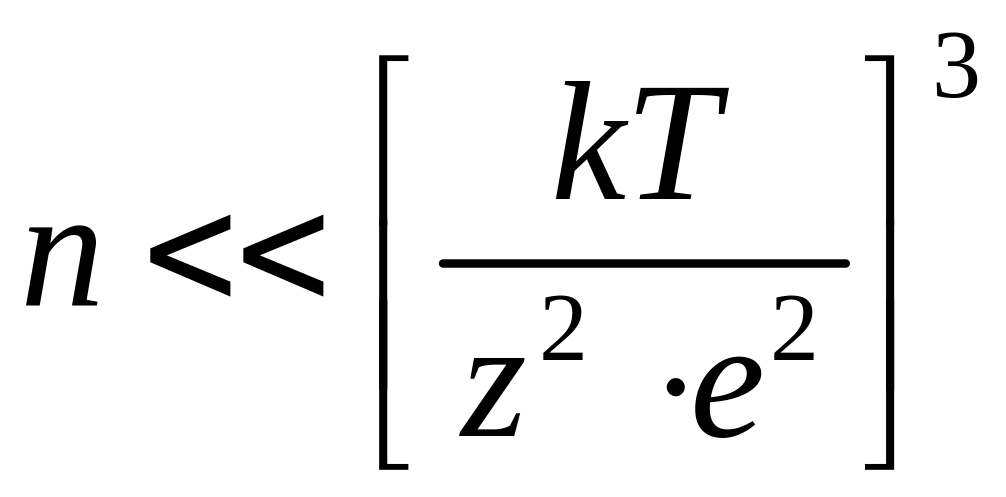 ,
(7.5)
,
(7.5)
де n – число частинок в одиниці об`єму; z – зарядне число.
Тобто ідеальність плазми виконується тоді, коли частинки знаходяться одна від одної на великих відстанях і їхня кінетична енергія значно більше енергії взаємодії. Умова розрідженості плазми
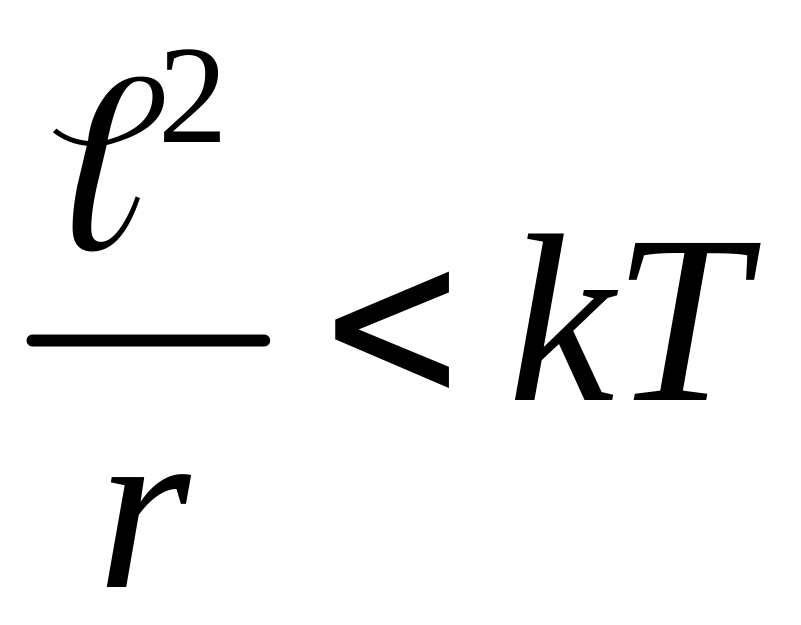 ,
(7.6)
,
(7.6)
де
![]() – середня потенціальна енергія
кулонівської взаємодії частинок зі
зарядом, що знаходиться на середній
відстані
– середня потенціальна енергія
кулонівської взаємодії частинок зі
зарядом, що знаходиться на середній
відстані
![]() ;
кТ – середня енергія теплового руху
частинок.
;
кТ – середня енергія теплового руху
частинок.
При підвищених тисках і відносно низькій температурі починає позначатися неідеальність плазми, тобто енергія взаємодії частинок становиться близькою за значенням з їхньою кінетичною енергією.
До класичної плазми можна застосувати статистику: постійна Больцмана і рух газу в ній класичний.
Для спрощення розрахунків плазмових процесів використовують прості моделі стану.
Найпростішою є модель повної динамічної рівноваги, яка характеризується температурою і тиском.
У плазмі постійно відбуваються два протилежні процеси: іонізація і деіонізація, тобто відновлення іонів до нейтральних атомів.
Іонізація відбувається за декілька етапів. Спочатку атом збуджується. Електрон в ньому переходить на більш високий енергетичний рівень, і якщо енергія збудження перевищує енергію граничного рівня, він покидає атом. При деіонізації процес відбувається в зворотному напрямку: електрон захоплюється атомом на найвищій енергетичний рівень, а потім випромінює енергію і спускається на стабільний рівень. Але існує і інша модель деіонізації, коли надлишок енергії електрона забирає інший електрон або іон.
Джерелом
енергії електронів в електричній дузі
є електричне поле. Величина енергії
![]() ,
де
,
де
![]() – електропровідність плазми; а
Е – напруженість електричного поля.
Для існування плазми повинен виконуватись
баланс енергії.
– електропровідність плазми; а
Е – напруженість електричного поля.
Для існування плазми повинен виконуватись
баланс енергії.
![]() ,
(7.7)
,
(7.7)
де
теплота
![]() -
пружних; а
-
пружних; а
![]() -
непружних зіткнень;
-
непружних зіткнень;
![]() -
втрати теплоти за рахунок дифузії
частинок плазми;
-
втрати теплоти за рахунок дифузії
частинок плазми;
![]() -
втрати тепла за рахунок теплопровідності,
враховуючи природні втрати енергії.
ККД плазми, залежно від газу і режимів,
коливається від 40 до 80 %. Найбільший ККД
у разі використовування в якості
плазмоутворюючого газу водню. Він у
цьому випадку становить 80 %.
-
втрати тепла за рахунок теплопровідності,
враховуючи природні втрати енергії.
ККД плазми, залежно від газу і режимів,
коливається від 40 до 80 %. Найбільший ККД
у разі використовування в якості
плазмоутворюючого газу водню. Він у
цьому випадку становить 80 %.
У плазмі, крім поняття середньої температури плазми, відрізняють температуру електронів та температуру важких частинок (атомів та іонів). При струмах менше ніж 10 А температура електронів в 7 – 10 разів вище ніж важких частинок газу. При струмах вище 10 А температура електронів та важких частинок становиться однаковою навіть при дуже великих струмах.
