
- •Абсолютная и относительная погрешности.
- •2. Классификация погрешностей
- •По форме представления:
- •2. По причине возникновения:
- •3. По характеру проявления:
- •5. Генеральная и выборочная совокупность
- •6. Среднее арифметическое выборочной совокупности. Случайное отклонение.
- •7. Выборочное стандартное отклонение. Дисперсия
- •8. Среднеквадратичное отклонение
- •9. Нормальное распределение
- •10. Распределение Стьюдента
- •11. Требование к пробе анализа. Генеральная, средняя, лабораторная и анализируемая проба
- •12. Отбор проб газов, жидкостей и твердых веществ.
- •13. Отбор проб пищевой продукции и продовольственного сырья.
- •14. Общие принципы подготовки проб к анализу
- •15. Метод разложения проб
- •16. Растворение проб
- •17. Сплавление пробы
- •18. Пиролиз пробы
- •19. Метод разделения и концентрирования
- •20. Сущность титриметрии
- •21. Стандартизация растворов титрантов
- •22. Точка эквивалентности
- •23. Точка конца титрования
- •24. Кривые титрования
- •Кривая титрования реакции кислотно-оснавного взаимодействия между нсi и NaOh
- •Кривая титрования слабой кислоты и сильного основания
- •Кривая титрования многоосновных кислот и оснований
- •25. Способы титрования
- •26. Индикаторы и правила выбора индикатора
- •27. Гальванический элемент
- •28. Общие принципы электрохимических методов анализа. Классификация электродов и электродных систем.
- •29. Метод прямой кондуктометрии
- •30. Безэлектродная кондуктометрия
- •31. Кондуктометрическое титрование
- •32. Сущность потенциометрического анализа.
- •33. Методы прямой потенциометрии
- •34. Электроды сравнения и индикаторный электрод
- •35. Ионоселективные электроды
- •1. Первичные:
- •2. Сложные и многомембранные
- •36. Методы потенциометрического титрования
- •38. Сущность кулонометрического анализа.
- •42. Схема установки полярографического анализа
- •43. Методы полярографии
- •44. Метод дифференциальной полярографии
- •45. Инверсионная вольтамперометрия
- •48. Основы хроматографии:
- •50. Хромотографич колонки:
- •52. Радиоактивность. Методы регистрации радиоактивности
Кривая титрования многоосновных кислот и оснований
Н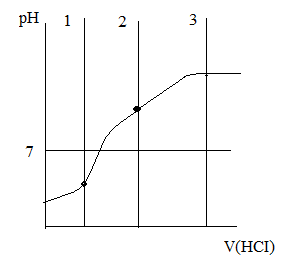 аблюдается
2 и > скачка титрования, что объясняется
ступенчатой диссоциацией.
аблюдается
2 и > скачка титрования, что объясняется
ступенчатой диссоциацией.
При титровании фосфорной кислоты NaOH.
25. Способы титрования
В титриметрии испол. 3 способа титрования: прямое, обратное и по заместителю.
Прямое титрование – титров. р-ра опред.вещества А непосредственно р-м титранта В. Его применяют в том случае, если р-я между А и В протекает быстро. Содержание комп-та А при прямом титр-нии титрантом В рас-ся на основе р-ва п(А)=п(В). В кач-ве примера определ.в-ва сп-м прямого тит-я след.р-я титр-я:
CH3COOH + NaOH CH3COONa + H2O
n (CH3COOH)=n (NaOH)
Обратное титр-е зак-ся в добавлении к опред.в-ву А избытка точно известного к-ва станд.р-ра В и после завершения р-ии между ними осущ.титров-е ост-гося кол-ва в-вар-м титранта В’. Этот способ применяют в тех случаях, когда р-я между А и В протек.нед.быстро, либо нет подх-гоиндикатора для фиксир-я точки экв-ти этой реакции. Пример:
CaCO3 + 2HCl (из-к) CaCl2 + CO2 + H2O
HCl (ост) + NaOH NaCl + H2O
n(1/2 CaCO3)=n(HCl)- n(NaOH)
Титрование по заместителю з-ся в титр-ии титрантом В не опред.в-ва А, а экв-го ему кол-ва з-ля А’, получив-гося в рез-те предвар.провед-й р-ии между опред.в-м А и каким-либо реагентом. Титров-е по з-лю примен.обычно в тех случаях, когда невозможно провести прямое титрование.
К-во молей эк-та опред-го в-ва титр-ии з-ля всегда равно к-ву молей эк-та титранта п(А)=п(В)=п(А’). пример:
K2Cr2O7 + 6KI + 7H2SO4 Cr2(SO4)3 + 3I2 (з-ль) + 4K2SO4 + 7H2O
I2 + 2Na2S2O3 2NaI + Na2S4O6
n(K2Cr2O7)= n(I2)= n(Na2S2O3)
26. Индикаторы и правила выбора индикатора
Индикаторы – в-ва, кот изменяют свою окраску при изменении рН.
В качестве индикаторов применяют:
Лакмус, кот в кисл среде – красн, в щелочн – синий;
Фенолфталеин, кот в кисл среде – бесцвет, в щелочн – малиновый;
Метилоранжевый, кот в кисл среде - розовый, в щелочной – желт.
У правильно выбранного индикатора интервал перехода окраски должен полностью или частично перекрываться скачком титрования. Если такого перехода нет, то индикатор для данного титрования не подходит.
В частности для кислот – основн титрования использ лакмус, метилоранжевый, метилкрасный, фенолфталеин.
Для фиксирования точки стехеометричности по промежуточ оттенкам окраски индикатора вводят такое понятие как показатель титрования, кот соотвевт значен рН, при кот заканчивается титрование, при кот находится конечная точка титрования.
Необходимо знать, что погрешность титр может быть обусловлена тем, что рН индикатор сам имеет кислот-осн природу, т.е. наличие индикатора в р-ре изменяет его рН, следовательно, колич необходимо ограничивать при добавлении в р-р, т.е. обходиться минимальным его колич. Кроме этого на погрешность влияет ещё то, что добавление индикатора вызывает постепенное разбавление р-ра, а также из-за увеличения воды, кот получ в результате реакции: Н+ + ОН- = Н2О.
