
- •Абсолютная и относительная погрешности.
- •2. Классификация погрешностей
- •По форме представления:
- •2. По причине возникновения:
- •3. По характеру проявления:
- •5. Генеральная и выборочная совокупность
- •6. Среднее арифметическое выборочной совокупности. Случайное отклонение.
- •7. Выборочное стандартное отклонение. Дисперсия
- •8. Среднеквадратичное отклонение
- •9. Нормальное распределение
- •10. Распределение Стьюдента
- •11. Требование к пробе анализа. Генеральная, средняя, лабораторная и анализируемая проба
- •12. Отбор проб газов, жидкостей и твердых веществ.
- •13. Отбор проб пищевой продукции и продовольственного сырья.
- •14. Общие принципы подготовки проб к анализу
- •15. Метод разложения проб
- •16. Растворение проб
- •17. Сплавление пробы
- •18. Пиролиз пробы
- •19. Метод разделения и концентрирования
- •20. Сущность титриметрии
- •21. Стандартизация растворов титрантов
- •22. Точка эквивалентности
- •23. Точка конца титрования
- •24. Кривые титрования
- •Кривая титрования реакции кислотно-оснавного взаимодействия между нсi и NaOh
- •Кривая титрования слабой кислоты и сильного основания
- •Кривая титрования многоосновных кислот и оснований
- •25. Способы титрования
- •26. Индикаторы и правила выбора индикатора
- •27. Гальванический элемент
- •28. Общие принципы электрохимических методов анализа. Классификация электродов и электродных систем.
- •29. Метод прямой кондуктометрии
- •30. Безэлектродная кондуктометрия
- •31. Кондуктометрическое титрование
- •32. Сущность потенциометрического анализа.
- •33. Методы прямой потенциометрии
- •34. Электроды сравнения и индикаторный электрод
- •35. Ионоселективные электроды
- •1. Первичные:
- •2. Сложные и многомембранные
- •36. Методы потенциометрического титрования
- •38. Сущность кулонометрического анализа.
- •42. Схема установки полярографического анализа
- •43. Методы полярографии
- •44. Метод дифференциальной полярографии
- •45. Инверсионная вольтамперометрия
- •48. Основы хроматографии:
- •50. Хромотографич колонки:
- •52. Радиоактивность. Методы регистрации радиоактивности
38. Сущность кулонометрического анализа.
На основе закономерности, что m пропорциональна Q, разработаны кулонометрические методы анализа, при которых исследуемый раствор подвергают электролизу, при этом измеряют Q, затраченную на электрохимическое восстановление или окисление определенного элемента. Прибор в котором осуществляется электролиз - гальванометр. Они позволяют измерить очень слабые токи. Этим методом можно определить очень маленькие значения. Однако эти методы трудно применить при электролизе веществ с близкими Eразл .
39. Прямая кулонометрия
При прямой кулонометрии, определяют в-во окислившееся либо восстановившееся непосредственно на одном из электродов, при этом побочные химические реакции не протекают. Этот метод прямой кулонометрии применяют для определения многих органических веществ (аскорбиновые кислоты, эпикриловые кислоты, новакаин и т.д.), при этом различают на практике кулонометрию при постоянном потенциале и при постоянной силе тока.
Кулонометрия при пост потенц (прям кулонометрия): В этом случае при пост потенциале электролиза сила тока постоянно изменяется, т.к. концентрация определяемого в-ва непрерывно падает. Сила тока изменяется по экспоненте в зависимости от времени эл-за, если построить графич зависимость в корд (ln I от t), то зависимость – прямая линия. Ln I=kt: k=tg α.
С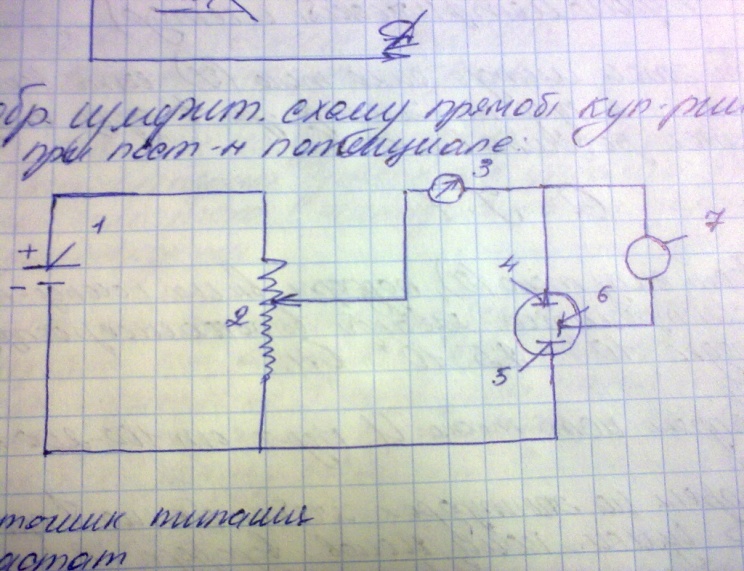 хема
прямой кулонометрии при пост потенц.
хема
прямой кулонометрии при пост потенц.
1 – источ питания,
2 – реастат,
3 – амперметр,
4- раб эл-д,
5 – эл-д,
6 – стандарт эл-д,
7 – потенциом электролизер.
Кулонометрия при пост силе тока (хронометр. М-д): При этом м-де сила тока постоянная величина, а продолжительность электролиза t опред секундомером, затем рассчит Q: Q=I*t.
40. Кулонометрия при постоянной силе тока
Кулонометрия при пост силе тока (хронометр. М-д): При этом м-де сила тока постоянная величина, а продолжительность электролиза t опред секундомером, затем рассчит Q: Q=I*t. Постоянную силу тока поддерживают включая последовательно с электролитической ячейкой высокополное сопротивление порядка 1*104 – 2.5*10 4. Наряжение поддерживается 100-200 В. Напряжение на ячейках обычно повышается при электролизе вследствие изменения концентрации ионов водорода в растворе.

Схема:
1 – источник питания,
2 – ключ,
3 – реастат,
4 – амперметр,
5 – ячейка для электролиза.
41. Теоретические основы вольтамперометрии
Вольтамперометрия основана на изучении поляризационных или вольтамперных кривых, т.е. изучение графических зависимостей силы тока в электролите от напряжения между электродами.
Если приложить небольшую разность потенциалов к электродам, кот. опущены в раствор электролита, а затем постепенно увеличить эту разность потенциалов, то как в электролите будет сначала небольшим, и будет возрастать по закону ОМА: J=E/R.
При этом в электролите, ионы будут разлагаться, либо восстанавливаться, либо окисляться на электродах, но в очень небольшом количестве. Как только разность потенциалов достигнет этого значения, для конкретных ионов, сила тока начнет резко возрастать. Если же при этом еще 1 из электродов сделать с малой поверхностью, а другой, со значительно большей, то на электроде с малой поверхностью, будет очень высокая плотность тока: ĵ=J/S. Поэтому, на поверхности малого электрода, начнет происходить интенсивное разложение ионов. При некотором напряжении, скорость разрядки ионов станет больше скорости диффузии этих ионов к малому электроду у глубины электролита, а концентрация ионов у поверхности электрода станет ничтожно малой (≈0). Ток этих ионов будет определяться скоростью диффузии этих ионов к поверхности электрода. Поэтому, ток, проходящий через электролит, практически не будет увеличиваться, с возрастанием разности потенциалов – предельный ток, а сила пропорциональна концентрации, иона в электролите. Эта зависимость называется – полярограммой, либо полярографической кривой.
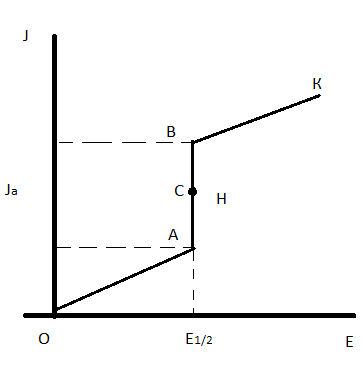
рис. Полярограмма
 ОА:
ток протекает практически без разрядки
ионов.
ОА:
ток протекает практически без разрядки
ионов.
АВ: резкое возрастание тока и соответственно резкое увеличение разрядки ионизирующих ионов.
ВК: все анализируемые ионы, успевают разрядиться со скоростью большей скорости их диффузии из ядра электролита.
H: характеризует предельный ток (Ja ) и дает определить концентрацию анализируемого вещества.
С: характеризует потенциал ½ необходимый для достижения половины предельного тока (потенциал полуволны).
Е1/2 не зависит от концентрации растворимого вещества, а зависит от природы восстановленного иона , и она служит для качественной оценки присутствующих в электролите ионов, т.е. по нему узнают какой ион разряжается.
Зависимость силы тока(J) от концентрации и анализируемых ионов(C): J=K*C, где К- коэффициент, зависящий от числа электронов принимающих или определяющих ионом при разрядке, и зависящий от коэффициента диффузии иона.
