
- •Абсолютная и относительная погрешности.
- •2. Классификация погрешностей
- •По форме представления:
- •2. По причине возникновения:
- •3. По характеру проявления:
- •5. Генеральная и выборочная совокупность
- •6. Среднее арифметическое выборочной совокупности. Случайное отклонение.
- •7. Выборочное стандартное отклонение. Дисперсия
- •8. Среднеквадратичное отклонение
- •9. Нормальное распределение
- •10. Распределение Стьюдента
- •11. Требование к пробе анализа. Генеральная, средняя, лабораторная и анализируемая проба
- •12. Отбор проб газов, жидкостей и твердых веществ.
- •13. Отбор проб пищевой продукции и продовольственного сырья.
- •14. Общие принципы подготовки проб к анализу
- •15. Метод разложения проб
- •16. Растворение проб
- •17. Сплавление пробы
- •18. Пиролиз пробы
- •19. Метод разделения и концентрирования
- •20. Сущность титриметрии
- •21. Стандартизация растворов титрантов
- •22. Точка эквивалентности
- •23. Точка конца титрования
- •24. Кривые титрования
- •Кривая титрования реакции кислотно-оснавного взаимодействия между нсi и NaOh
- •Кривая титрования слабой кислоты и сильного основания
- •Кривая титрования многоосновных кислот и оснований
- •25. Способы титрования
- •26. Индикаторы и правила выбора индикатора
- •27. Гальванический элемент
- •28. Общие принципы электрохимических методов анализа. Классификация электродов и электродных систем.
- •29. Метод прямой кондуктометрии
- •30. Безэлектродная кондуктометрия
- •31. Кондуктометрическое титрование
- •32. Сущность потенциометрического анализа.
- •33. Методы прямой потенциометрии
- •34. Электроды сравнения и индикаторный электрод
- •35. Ионоселективные электроды
- •1. Первичные:
- •2. Сложные и многомембранные
- •36. Методы потенциометрического титрования
- •38. Сущность кулонометрического анализа.
- •42. Схема установки полярографического анализа
- •43. Методы полярографии
- •44. Метод дифференциальной полярографии
- •45. Инверсионная вольтамперометрия
- •48. Основы хроматографии:
- •50. Хромотографич колонки:
- •52. Радиоактивность. Методы регистрации радиоактивности
23. Точка конца титрования
В точке эквивалентности наблюдается резкое изменение электропроводности.
Титрование проводят до точки конца титрования, когда с помощью приборных методов устанавливают состояние эквивалентности титранта и титруемого вещества.
Точка конца титрования соответствует точному объему добавленного титранта, кот. не меньше эквивалентного объема титранта, т.е. равно или чуть больше, эта точка устанавливается индикатор.методами, физико-хим.инструм-ми методами.
В индикаторных методах чаще всего исп.цветной индикатор, кот.изменяет свой цвет.
24. Кривые титрования
Важной характеристикой титриметрических методов являются кривые титрования - они показывают графическую зависимость концентрации участника реакции, протекающей при титровании (либо логарифма концентрации или какой-то характеристики раствора) от объема добавленного титранта (либо от степени оттитрованности). Например, для реакций кислотно-основного взаимодействия такой характеристикой раствора служит его pH.
Различают: 1) линейные кривые титрования
2) логарифмические кривые титрования
И в 1) и 2): при построении кривых, на оси абсцисс откладывается количество добавляемого реагента, а на оси ординат:
1)в случае линейных кривых откладывается измеряемая величина, которая зависит от концентрации ( плотность раствора, сила тока).
2)в случае построения логарифмических кривых на оси ординат откладываются величины, связ. с логарифмами концентраций реагир. в-ва . К ним относятся: -рН, -рС, -окислительно-восстановительный потенциал.
Кривая титрования реакции кислотно-оснавного взаимодействия между нсi и NaOh
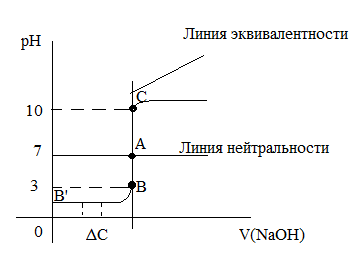
Вначале участок В’-В, рН раствора меняется очень медленнодаже при большом добавлении титранта NaОН.
При приближении к точке В, отношение ∆рН/∆С, начинает существенно расти.
От точки В к точке С, наблюдается резкое увеличение, даже при прибавлении очень малого количества титранта.
Точка А, на этом графике- является точкой эквивалентности, с ней совпадает точка нейтральности, либо они очень близки.
Линия ВС – называется участком скачка титрования, а тока эквивалентности А, всегда находится на участке ВС.
Достижение точки С, должно соответствовать конечно токе титрования точки А, часто берут приблизительно.
Чем > отношение ∆рН/∆С (т.е. чем больше участок ВС), тем точнее титрование.
Кривая титрования слабой кислоты и сильного основания
Э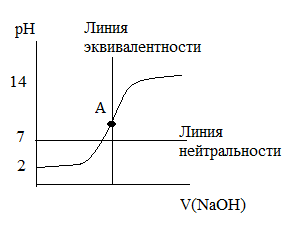 ту
кривую раствором на примере титровании
уксусной кислоты NaOH:
ту
кривую раствором на примере титровании
уксусной кислоты NaOH:
Кривая до точки эквивалентности А, изменяется плавно, а линия нейтральности пересекается этой кривой до точки эквивалентности, т.е. в этом случае, они не совпадают, а сама точка эквивалентности находится в щелочной области, что является ее характерной особенностью этой кривой титрования.
Кривая титрования слабого основания сильной кислотой
Титрование аммиака соляной кислотой(НСI)
р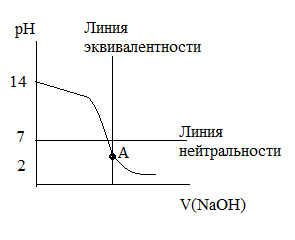 Н
плавно уменьшится до скачка, в области
точки эквивалентности, которая расположена
в кислотной области.
Н
плавно уменьшится до скачка, в области
точки эквивалентности, которая расположена
в кислотной области.
