
- •2В: Необратимые поликонденсационные процессы.
- •2.Влияние основных факторов на поликонденсацию в расплаве.
- •2.Поликонденсация в расплаве. Кинетика процесса.
- •3.Полимераналогичные превращения. Реакционная спос-сть полимеров.
- •Передача цепи через растворитель, мономер, инициатор, регулятор мм полимера.
- •Типы и характер реакций поликонденсации.
- •Стадии поликонденсационных процессов. Образование реакционных центров.
- •Способность мономера к радикально-цепной полимеризации.
- •Катионная полимеризация. Инициирование процесса.
- •3.Стадии поликонденсационных процессов. Ступенчатый рост цепей.
- •1. Регулирование и ингибирование радикальной полимеризации.
- •2 Кинетика поликонденсации.
- •3 Циклизация при полимеранологичных превращениях.
- •1. Предельная температура процесса. Влияние давления и конверсии на радикальную полимеризацию.
- •2. Поликонденсация в растворе. Роль растворителя в процессе
- •Поликонденсация в растворе, влияние бинарных растоврителей.
- •Побочные реакции при поликонденсации в расплаве.
3 Циклизация при полимеранологичных превращениях.
В результате полимеранологичных превращениях боковых функциональных групп изменяется строение основной цепи. Например, это происходит в результате циклизации (ацеталирование ПВС и отщепление хлора от ПВХ)
Циклизация при химическом превращении возможна с низкомолекулярным реагентом (взаимодействие ПВХ с толуолом в присутствии AlCl3)

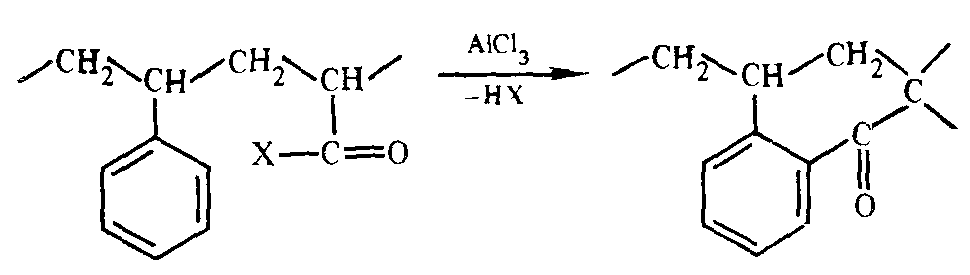
Образование циклов в результате межфрагментной реакции звеньев сополимеров (сополимеризация стирола и произв.акриловой кислоты в условиях реакции Фриделя Крафтса).
Реакция образования полиметакриламида при взаимодействии одинаковых или различных функциональных групп (пример формирования изолированных циклов в цепях макромолекул):

Взаимодействие функциональных групп в боковых цепях могут приводить к образованию конденсированных циклов. Боковые участки 1,2-полибутодиена формируют участки цепей с конденсированными циклогексановыми фрагментами:

При анионном инициировании или при термическом воздействии (~200°C) боковые нитрильные группы полиакрилонитрила превращаются по схеме:

Билет 8
1. Предельная температура процесса. Влияние давления и конверсии на радикальную полимеризацию.
Из уравнения ∆G=∆H-T∆S, определяющего термодинамическую возможность протекания полимеризации, следует, что при повышении температуры может быть достигнуто равенство энтальпийного и энтропийного члена (∆G=0 – процесс прекращается). При дальнейшем росте температуры ∆G>0 происходит деполимеризация. Следовательно, процесс полимеризации равновесный:

Температура, при которой скорость прямого и обратного процесса равны – предельная температура.
Tпр=∆Hp/∆Sp
∆Hp, ∆Sp – изменение энтропии и энтальпии при росте цепи, считая на повторяющееся звено.
Сначала с повышением температуры, Кр повышается и скорость полимеризации увеличивается. Затем более быстро увеличивается скорость деполимеризации (рост kдеп). При Тпред скорость полимеризации равна скорости деполимеризации. Для нахождении Тпред используют уравнение изотермы:
∆G=∆Gº+RTlnK
Полимеризация раствора мономера определенной концентрации при заданной температуре идет до установления равновесия, т.е. до критической концентрации мономера [M]кр, отвечающей Тпр. Для каждой концентрации мономера своя Тпред выше которой полимеризация не идет.

Влияние давления.
Повышение давления до нескольких атмосфер мало влияет на скорость процесса и молекулярную массу полимера. Однако высокое давление существенно ускоряют радикальную полимеризацию, повышают молекулярную массу образующегося полимера (см.рис.):

Зависимость
скорости r
и средней степени полимеризации ![]() от давления определяются изменениями
констант скорости элементарных реакций,
так как объем активированного комплекса
в каждой реакции отличается от объемов
исходных реагирующих частиц. В соответствии
с уравнение скорости полимеризации:
от давления определяются изменениями
констант скорости элементарных реакций,
так как объем активированного комплекса
в каждой реакции отличается от объемов
исходных реагирующих частиц. В соответствии
с уравнение скорости полимеризации:

И с уравнением Вант-Гоффа влияние давления P на r можно определить:

где
![]() - изменение объема активации (разность
объемов исходных веществ и активированного
комплекса) на стадии роста цепи:
- изменение объема активации (разность
объемов исходных веществ и активированного
комплекса) на стадии роста цепи:

Отрицательное значение обусловлено тем, что объем активированного комплекса меньше объема исходных веществ, а отсюда: константа скорости полимеризации растет с увеличением давления.
Более сложно влияет давление на молекулярную массу. Анализ этого влияния проводят в рамках уравнения:

и уравнения Вант-Гоффа, рассматривая изменение с давлением каждой из констант.
Влияние конверсии.
При увеличении конверсии в полимеризационной системе прежде всего
возрастает вязкость реакционной смеси, что ограничивает диффузионную подвижность реагирующих частиц. Если образующийся полимер растворим в собственном мономере (гомофазная полимеризация в массе), то выделяют четыре стадии полимеризации (см.рис.):
П ри
низких конверсиях (I)
скорость процесса описывается уравнениями
для идеальной полимеризации, при этом
молекулярная масса практически постоянна.
При большей конверсии (20-65%) (II)
процесс ускоряется и молекулярная масса
существенно возрастает, хотя скорость
инициирования постоянна. При более
высокой конверсии (III)
ускорение процесса прекращается, но
скорость и молекулярная масса остается
высокими. На последних стадиях (IV)
происходит замедление процесса
(исчерпание мономера, отверждение
системы, приближение к [Мкр]).
ри
низких конверсиях (I)
скорость процесса описывается уравнениями
для идеальной полимеризации, при этом
молекулярная масса практически постоянна.
При большей конверсии (20-65%) (II)
процесс ускоряется и молекулярная масса
существенно возрастает, хотя скорость
инициирования постоянна. При более
высокой конверсии (III)
ускорение процесса прекращается, но
скорость и молекулярная масса остается
высокими. На последних стадиях (IV)
происходит замедление процесса
(исчерпание мономера, отверждение
системы, приближение к [Мкр]).
На практике с увеличением продолжительности процесса наблюдается увеличение скорости и молекулярной массы. Это явление гель-эффект. Причина: резкое возрастание вязкости, уменьшение скорости роста, но в еще большей степени, скорости обрыва цепи.
