
- •Онкологические заболевания органов грудной клетки
- •1.1. Эпидемиология
- •1.2.2. Профессиональные вредности
- •1.3. Предраковые заболевания легких
- •1.4. Профилактика рака легкого
- •1.5. Классификация рака легкого
- •1.5.1. Клинико-анатомическая классификация
- •1.5.3. Международная классификация рака легкого по системе tnm
- •Международная классификация стадий рака легкого (1997 год)
- •1.6. Закономерности метастазирования рака легких
- •1.7. Диагностика рака легкого
- •1.7.1. Принципы диагностики рака легкого
- •1.7.3. Клиническая картина
- •I. Симптомы, вызванные внутриторакальным распространением опухоли
- •II. Симптомы, обусловленные внеторакальным распространением опухоли
- •III. Паранеопластические синдромы
- •1.7.4. Методы первичной диагностики рака легкого
- •I. Центральный рак легкого
- •III. Верхушечный рак Панкоста.
- •1.7.5. Скрытый рак легкого
- •1.7.6. Методы уточняющей диагностики рака легкого
- •1.7.7. Скрининг в диагностике рака легкого
- •1.8. Лечение рака легкого
- •1.8.1. Общие принципы лечения немелкоклеточного рака легкого
- •1.8.2. Хирургический метод
- •1.8.3. Лучевое лечение
- •1.8.4. Химиотерапия
- •1.8.5. Лечение мелкоклеточного рака
- •1.9. Симптоматическое лечение рака легкого
- •1.10. Результаты лечения и прогноз
- •1.11. Контрольные вопросы
- •1.12. Тестовые задания
- •Рекомендуемая литература
- •2.1. Эпидемиология рака пищевода
- •2.2. Анатомия средостения и пищевода
- •2.3. Этиология и патогенез рака пищевода
- •2.3.1. Предрасполагающие факторы этиопатогенеза
- •2.3.2. Предраковые заболевания
- •2.3.3. Аденокарциномные предраки
- •2.4. Классификация рака пищевода
- •2.4.1. Клиническая классификация
- •2.4.2. Международная классификация tnm
- •2.4.3. Японская классификация лимфоузлов
- •2.5. Диагностика рака пищевода
- •2.5.1. Клинические проявления рака пищевода
- •2.5.2. Дифференциальная диагностика заболевания
- •2.5.3. Эндоскопическая диагностика рака пищевода
- •2.5.4. Рентгенодиагностика рака пищевода
- •2.5.5. Дополнительные методы исследования
- •2.5.6. Скрининг в ранней диагностике рака пищевода
- •2.6. Лечение рака пищевода
- •2.6.1. Хирургическое лечение рака пищевода
- •2.6.1.1. Историческая справка хирургии рака пищевода
- •2.6.1.2. Противопоказания к оперативному лечению
- •2.6.1.3. Характеристика доступов в хирургии рака пищевода
- •2.6.1.4. Эндоскопическая хирургия рака пищевода
- •2.6.1.5. Лимфодиссекция при раке пищевода
- •2.6.1.6. Вопросы пластики пищевода
- •2.6.1.7. Прогноз хирургического лечения рака пищевода
- •2.6.1.8. Результаты хирургического лечения рака пищевода
- •2.6.2. Лучевая терапия рака пищевода
- •2.6.3. Химиотерапия рака пищевода
- •2.6.4. Комбинированное лечение рака пищевода
- •2.6.5. Паллиативное лечение рака пищевода
- •2.7. Контрольные вопросы
- •2.8. Тестовые задания
- •Рекомендуемая литература
- •3.1. Анатомия и физиология средостения
- •3.2. Классификация опухолей и кист средостения
- •3.3. Характеристика опухолей средостения
- •3.3.1. Опухоли тимуса
- •I. Органоспецифические опухоли вилочковой железы.
- •II. Органонеспецифические опухоли вилочковой железы.
- •3.3.2. Неврогенные опухоли средостения
- •I. Неврогенные опухоли из собственно нервной ткани.
- •II. Неврогенные опухоли из оболочек нервов.
- •3.3.3. Мезенхимальные опухоли средостения
- •I. Опухоли волокнистой соединительной ткани.
- •II. Опухоли жировой ткани.
- •III. Мезенхимальные опухоли из сосудов.
- •VI. Опухоли из гладкомышечной ткани.
- •V. Опухоли из нескольких тканей мезенхимальной природы.
- •3.3.4. Опухоли из лимфоретикулярной ткани
- •3.3.5. Опухоли из нескольких тканей, смещенных в средостение
- •3.4. Характеристика кист средостения
- •I. Врожденные кисты средостения.
- •II. По локализации:
- •3.5. Клиника опухолей средостения
- •3.5.1. Объективные признаки опухолевых образований средостения
- •3.5.2. Осложнения, вызываемые опухолями средостения
- •3.6. Диагностика опухолей средостения
- •3.6.1. Рентгенодиагностика
- •3.6.2. Компьютерная томография в диагностике опухолей средостения
- •3.6.3. Узи в диагностике опухолей средостения
- •3.6.4. Эндоскопическая и морфологическая диагностика опухолей средостения
- •3.6.5. Необходимый минимум обследования
- •3.6.6. Дифференциальная диагностика
- •3.7. Лечение опухолей средостения
- •3.7.1. Хирургическое лечение
- •3.7.2. Типы оперативных вмешательств
- •3.7.3. Выбор оперативного доступа
- •Основные принципы выбора оперативного доступа при новообразованиях средостения
- •3.7.4. Выбор объема операции
- •Основные принципы выбора объема операции при новообразованиях средостения
- •3.7.5. Особенности хирургической техники
- •3.7.6. Хирургическое лечение синдрома компрессии
- •3.7.7. Лечение злокачественных лимфом
- •3.8. Контрольные вопросы
- •3.10. Рекомендуемая литература
- •Ошибки в клинической онкологии: Руководство для врачей / Под ред. В.И.Чиссова, а.Х.Трахтенберга. – м.: Медицина, 2001. – 544с. Тестовые задания для самопроверки знаний Вариант I
- •Вариант II
- •Матрицы ответов к заданиям в тестовой форме для самопроверки знаний Модуль 1. Рак легкого
- •Модуль 2. Опухоли пищевода
- •Матрицы ответов к итоговым тестам Вариант 1.
- •Глоссарий
- •Интернет ресурсы
- •Онкологические заболевания органов грудной клетки
- •644043 Г. Омск, ул. Ленина, 12; тел. 23-05-98
1.8.3. Лучевое лечение
Большинство больных раком легкого к моменту установления диагноза в силу распространенности опухолевого процесса или серьезных сопутствующих заболеваний являются неоперабельными. Среди пациентов, у которых опухоль признана резектабельной, подавляющее большинство относится к лицам старше 60 лет, и из них серьезные сопутствующие заболевания имеют более 30%. Вероятность «функциональной» неоперабельности у них весьма высока. Это требует проведения лучевого лечения (рис. 30).

Рис. 30. Современный аппарат для лучевой терапии.
Немелкоклеточный рак легкого характеризуется невысокой радиочувствительностью, особенно в поздних стадиях, поэтому с помощью лучевой терапии удается добиться излечения лишь у 7-12% больных.
Традиционно при лучевой терапии рака легкого применяют режим так называемого классического фракционирования, заключающийся в подведении разовых доз 1,8-2,5 Гр ежедневно 5-6 раз в неделю до суммарных доз 60 Гр. Подобный вариант фракционирования обеспечивает достаточно хорошее восстановление нормальной соединительной ткани.
К настоящему времени накоплен значительный опыт применения при немелкоклеточном раке легкого, наряду с классическим режимом фракционирования дозы, укрупненных (3-5 Гр) и крупных (более 6 Гр) фракций дозы при ежедневном облучении, с интервалом 48 ч. и более.
Суммарная очаговая доза, необходимая для разрушения первичной опухоли, по данным различных авторов, колеблется от 50 до 80 Гр. Ее подводят за 5-8 нед. При этом в связи с разной радиочувствительностью следует учитывать гистологическое строение опухоли. При плоскоклеточном раке суммарная доза обычно составляет 60-65 Гр, при железистом 70-80 Гр.
Для лечения рака легкого применяют статическую и ротационную гамма-терапию либо тормозное излучение ускорителей.
Лучевая терапия рака легкого может носить радикальный или паллиативный характер.
Радикальное лучевое лечение предусматривает получение длительного и стойкого эффекта в результате гибели всей опухоли в облучаемом объеме, тогда как при паллиативном облучении имеется в виду лишь частичное ее разрушение с целью облегчения клинических проявлений опухоли.
Объем тканей, подвергающихся радикальному лучевому воздействию, должен охватывать видимую первичную опухоль, вероятные метастазы I-III этапа лимфогенного распространения бронхолегочные, прикорневые, верхние и нижние (бифуркационные) трахеобронхиальные, паратрахеальные лимфатические узлы.
Показания к лучевой терапии рака легкого по радикальной программе (суммарная очаговая доза не менее 60-70 Гр):
1) центральный рак легкого I-III стадии (при отсутствии или наличии увеличенных лимфатических узлов в зонах регионарного метастазирования) у больных, которые отказались от операции или которым хирургическое лечение противопоказано (низкие функциональные резервы, сопутствующие заболевания);
2) периферический рак легкого I-III стадии (при отсутствии или наличии увеличенных регионарных лимфатических узлов) у больных, которым операция противопоказана или которые отказались от нее. Показания к лучевой терапии по радикальной программе обычно расширяют.
Показания к лучевой терапии по паллиативной программе (суммарная очаговая доза не превышает 40 Гр):
1) центральный или периферический рак легкого с метастазами во все группы лимфатических узлов средостения;
2) значительное распространение опухоли на грудную стенку, сдавление магистральных сосудов средостения, прорастание в перикард, диафрагму;
3) метастазы в надключичные лимфатические узлы;
4) рецидив или солидные метастазы в легком;
5) состояние после пробной торакотомии. Обусловленной прорастанием опухоли в перикард, обширным распространением по клетчатке средостения.
Довольно часто в процессе лучевой терапии отмечается выраженная регрессия опухоли, поэтому при хорошем общем состоянии больного можно изменить план лечения и провести лучевую терапию по радикальной программе.
Современные методы радиохирургического лечения. Система стереотаксической хирургии CyberKnife (рис. 31) была создана в Стенфордском университете (США) в 1992 году.
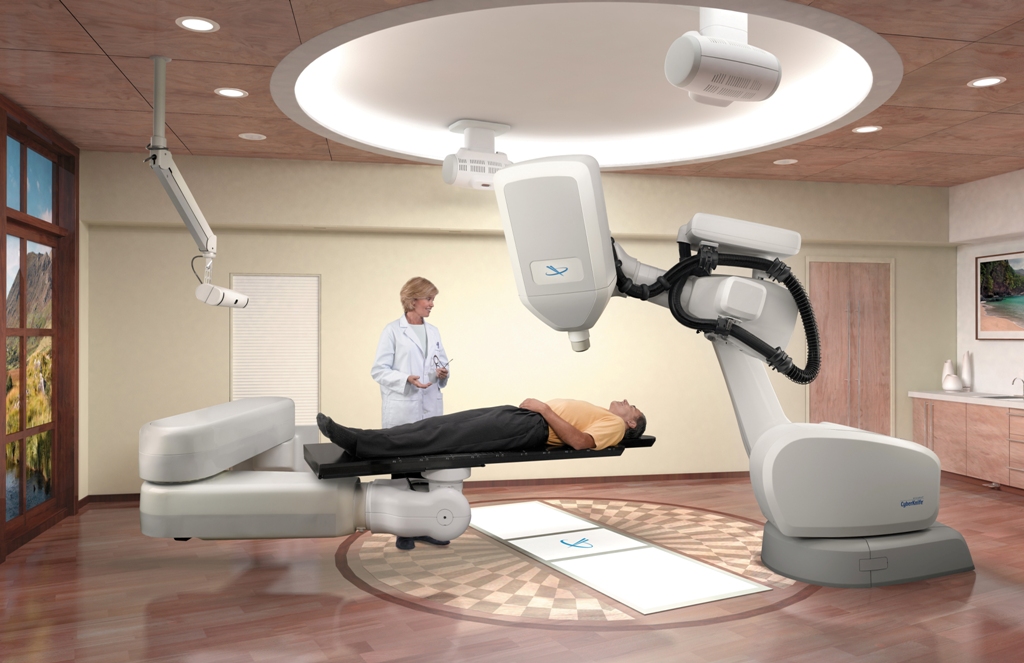
Рис. 31. Система стереотаксической радиохирургии CyberKnife.
Первая из двух основных уникальных особенностей системы CyberKnife – это миниатюрный линейный ускоритель, установленный на мобильной роботизированной руке, что в значительной степени улучшает маневренность, обеспечивая не имеющие аналогов 6 степеней свободы (рис. 32).
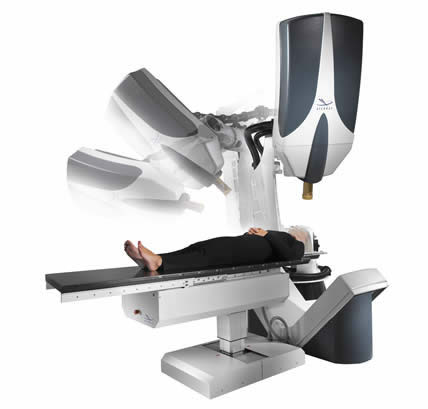
Рис. 32. Система стереотаксической радиохирургии CyberKnife.
Принцип работы мобильной роботизированной руки.
Вторая инновация – это сложная система получения изображения, устраняющая необходимость стереотаксической головной рамки. Посредством использования костных ориентиров и специализированных маркеров для локализации поражения, а также системы отслеживания изображения, работающей в реальном времени, CyberKnife способен делать поправку на движения пациента во время процесса лечения, обеспечивая точную локализацию и поражение цели (рис. 33). Источник радиации генерирует многочисленные перекрестные лучи и направляет точно сфокусированный поток радиации на специально выбранное поражение внутри тела. Такая техника позволяет обеспечить концентрацию высокой дозы радиации на объекте-мишени, в то время как окружающие здоровые ткани получают более низкие, безвредные дозы.
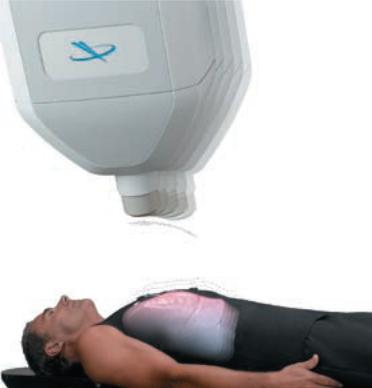
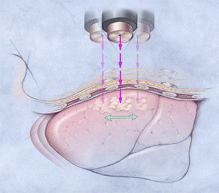
Рис. 33. Принцип учета поправок на движение опухоли при использовании стереотаксической радиохирургии CyberKnife.
Стереотаксическая радиохирургия отличается от обычной фракционированной радиотерапии тем, что ее эффективность не зависит от большей чувствительности к излучению клеток опухоли в отличие от нормальной ткани. Из-за резкого уменьшения дозы излучения за пределами мишени, при применении радиохирургии здоровая ткань получает значительно меньшую дозу и не повреждается, в то время как выбранные клетки внутри мишени получают летальную дозу. Так как с помощью выборочного дозирования в радиохирургии могут быть сведены к минимуму повреждения здоровой ткани, то поддаются лечению и традиционно устойчивые к излучению опухоли, для которых неэффективна обычная радиотерапия. Стереотаксическая радиохирургия обладает рядом достоинств в сравнении с хирургической резекцией. Радиохирургическая процедура неинвазивна, не требует применения общей анестезии, и обычно позволяет немедленное возвращение пациента к нормальной жизни. Поскольку не производится хирургическое вмешательство, при использовании радиохирургии также меньше риск занесения инфекции и возникновения осложнений. Кроме того, радиохирургия оказывается более выгодным по стоимости методом, чем хирургическая резекция, благодаря таким факторам, как меньшее количество острых осложнений, меньшее количество дней, необходимых для госпитализации пациента, и более короткий период выздоровления. Все эти факторы при наличии соответствующих показаний делают радиохирургию очень привлекательной альтернативой хирургической резекции (рис. 34).

Рис. 34. Результаты лечения рака легкого системой CyberKnife
