
- •Реферат
- •Содержание
- •Введение
- •1 Литературный обзор
- •1.1 Физико-химические свойства серной кислоты
- •1.2 Методы получения серной кислоты
- •1.3 Методы охлаждения серной кислоты в теплообменниках
- •1.4 Физико-химические основы производства серной кислоты
- •1.4.1 Физико-химические основы процесса очистки газа
- •1.4.2 Физико-химические основы осушки газа
- •1.4.3 Потери сернистого ангидрида с сушильной кислотой
- •1.4.4 Физико-химические основы процесса окисления сернистого ангидрида
- •1.4.4 Физико-химические основы процесса абсорбции серного ангидрида
- •2 Описание технологического процесса производства контактной серной кислоты
- •2.1 Специальная очистка газа
- •2.1.1 Основы очистки газа в промывном отделении
- •2.1.2 Очистка от тумана серной кислоты
- •2.2 Осушка газа в башнях с насадкой, орошаемых крепкой серной кислотой
- •2.3 Окисление сернистого ангидрида до серного на поверхности ванадиевого катализатора
- •2.3.1 Сущность технологического процесса контактного отделения
- •2.4 Поглощение серного ангидрида в абсорберах, орошаемых моногидратом
- •3 Реконструкция холодильного оборудования сушильно-абсорбционного отделения
- •4 Технологические расчеты
- •4.1 Расчет материального баланса сушильно-абсорбционного отделения
- •4.1.1 Расчет материального баланса осушки газа
- •4.1.2 Расчет материального баланса абсорбции серного ангидрида
- •4.2 Тепловой расчет сушильно-абсорбционного отделения
- •4.2.1 Тепловой расчет сушильной башни
- •4.2.2 Тепловой расчет моногидратного абсорбера
- •4.2.3 Конструктивный и гидравлический расчет моногидратного абсорбера
- •4.3 Конструктивный расчет пластинчатого холодильника «Альфа-Лаваль»
- •4.3.1 Расчет поверхности теплообмена
- •4.3.2. Расчет схемы компоновки пластин
- •4.3.3 Расчет гидравлических сопротивлений
- •4.4 Расчет материального баланса контактного отделения
- •4.4.1 Расчет материального баланса контактного узла
- •4.5 Тепловой расчет контактного узла
- •433 Tх5 273 (tабс )
- •433 329 273 (Tабс )
- •433 Tх5 243 (tабс )
- •433 306 243 (Tабс )
- •39 119 Нм3/ч (0,82 Vисх.)
- •5 Безопасность жизнедеятельности
- •5.1 Краткая характеристика производства
- •5.2 Характеристика основных опасностей производства и условий труда
- •5.3 Обеспечение безопасности работы
- •5.3.1 Электробезопасность
- •5.3.2 Освещенность проектируемого цеха
- •5.3.3 Защита от шума и вибраций
- •5.3.4 Вентиляция и аспирация
- •5.3.5 Микроклимат рабочей зоны проектируемого цеха
- •5.3.6 Эргономика рабочего места
- •Р ис. 5.2. Зона досягаемости моторного поля в горизонтальной плоскости при высоте рабочей поверхности над полом 725мм
- •5.3.6.1 Требования к размещению технических устройств и рабочих мест
- •5.4 Пожаробезопасность
- •5.5 Требования безопасности в аварийных ситуациях
- •Выводы по разделу проекта бжд:
- •6 Технико-экономические расчеты
- •6.1 Расчет общей суммы капитальных вложений
- •6.2 Расчет амортизационных отчислений
- •6.3 Расчет материальных затрат в проектном варианте
- •6.4 Расчет численности работающих и фонда заработной платы
- •6.5 Расчет накладных расходов
- •6.6 Расчет изменения себестоимости продукции
- •6.7 Расчет показателей экономической эффективности инвестиций
- •Заключение
- •Библиографический список
1.4.4 Физико-химические основы процесса абсорбции серного ангидрида
Последней стадией процесса производства серной кислоты контактным методом является извлечение триоксида серы из газовой смеси и превращение его в серную кислоту.
В абсорберах SO3 абсорбируется серной кислотой. Триоксид серы растворяется в серной кислоте, а затем взаимодействует с содержащейся в ней водой. Взаимодействие серного ангидрида с водой можно описать уравнением реакции:
![]() (1.4.13)
(1.4.13)
В зависимости от количественного соотношения воды и SO3 получают серную кислоту различной концентрации. При n > 1 образуется олеум, при n = 1 – моногидрат (100%-ная серная кислота), а при n < 1 – водный раствор серной кислоты, т. е. разбавленная серная кислота.
После абсорбции газовая смесь вместе с непоглощенным серным ангидридом удаляется в атмосферу. Для уменьшения потерь SO3 с отходящими газами его поглощение в абсорбционном отделении должно быть возможно более полным.
Для получения олеума газ, содержащий SO3, пропускают вначале через абсорбер, орошаемый олеумом (олеумный абсорбер). Здесь поглощается только часть SO3, окончательное поглощение происходит во втором абсорбере, орошаемом моногидратом (моногидратный абсорбер).
Стандартом предусматривается содержание в продукционном олеуме не менее 20 % SO3 своб., им и орошают олеумный абсорбер. Концентрация H2SO4, орошающей моногидратный абсорбер, составляет около 98,3%. Кислота такой концентрации хорошо абсорбирует серный ангидрид, так как давление паров SO3 и воды над ней ничтожно мало.
Количество выпускаемого олеума зависит от того, какая часть серного ангидрида поглощается в олеумном абсорбере, и от объема воды, поступающей с сушильной кислотой из очистного отделения в абсорбционное.
Газообразный
серный ангидрид наиболее полно
абсорбируется серной кислотой концентрации
98,3 % масс. H2SO4,
при меньшей или большей концентрации
H2SO4
способность ее к поглощению ухудшается.
Такая зависимость объясняется тем, что
над серной кислотой концентрацией ниже
98,3 % масс. H2SO4
равновесное давление SO3
ничтожное (![]() ),
а равновесное давление паров воды
значительное (
),
а равновесное давление паров воды
значительное (![]() ),
поэтому с поверхности серной кислоты
происходит испарение (десорбция) молекул
воды.
),
поэтому с поверхности серной кислоты
происходит испарение (десорбция) молекул
воды.
Основное количество молекул SO3 диффундирует к поверхности серной кислоты и абсорбируются ею, но часть их встречается с молекулами воды, испаряющимися с поверхности серной кислоты и диффундирующими в основной поток газа. Сталкиваясь, эти молекулы соединяются с образованием паров серной кислоты, которые затем конденсируются в объеме с образованием мельчайших капель (тумана) серной кислоты, по уравнению (1.4.14):
![]() (1.4.14)
(1.4.14)
Туман плохо улавливается в обычной абсорбционной аппаратуре и в основном уносится с отходящими газами в атмосферу. Чем ниже концентрация серной кислоты и выше ее температура, тем больше выделяется из нее паров воды, больше образуется тумана и больше теряется SO3.
Над кислотой концентрацией выше 98,3 % масс. H2SO4 равновесное давление , поэтому он абсорбируется серной кислотой неполностью. В этом случае отходящие газы также уносят в атмосферу часть SO3. Таким образом, при концентрации орошающей кислоты менее и более 98,3 % масс. H2SO4 абсорбция серного ангидрида снижается; она тем ниже, чем выше температура, поскольку равновесные давления паров Н2O и SO3 над кислотой возрастают с повышением температуры.
При концентрации
кислоты 98,3 % масс. H2SO4
равновесные давления паров воды и SO3
малы (![]() ;
;![]() но
равновесное давление паров самой серной
кислоты значительное (
но
равновесное давление паров самой серной
кислоты значительное (![]() ),
поэтому происходит испарение (десорбция)
паров серной кислоты с ее поверхности
и степень абсорбции SO3
снижается. Однако при температуре ниже
100 °С равновесное давление паров серной
кислоты очень мало, поэтому в
производственных условиях 98,3%-ная серная
кислота обладает наиболее высокой
абсорбционной способностью по отношению
к SO3.
),
поэтому происходит испарение (десорбция)
паров серной кислоты с ее поверхности
и степень абсорбции SO3
снижается. Однако при температуре ниже
100 °С равновесное давление паров серной
кислоты очень мало, поэтому в
производственных условиях 98,3%-ная серная
кислота обладает наиболее высокой
абсорбционной способностью по отношению
к SO3.
Если концентрация серной кислоты выше 98,3 % масс. H2SO4, то при соприкосновении ее с SO3 протекает обычный процесс абсорбции. Тогда количество абсорбируемого серного ангидрида можно рассчитать по уравнению (1.4.15):
![]() (1.4.15)
(1.4.15)
где
![]() – количество
абсорбируемого SO3,
кг/ч;
– количество
абсорбируемого SO3,
кг/ч;
К – коэффициент абсорбции, кг/(м2·ч·Па);
F – Поверхность насадки, м2;
![]() — движущая сила
абсорбции, Па.
— движущая сила
абсорбции, Па.
Коэффициент абсорбции при поглощении SO3 серной кислотой можно определить по уравнению (1.4.16):
![]() ,
(1.4.16)
,
(1.4.16)
где
K – коэффициент, зависящий от концентрации и температуры;
![]() – фактическая
скорость газа в абсорбере, м/с.
– фактическая
скорость газа в абсорбере, м/с.
Абсорбция SO3 олеумом в олеумном абсорбере также ухудшается с повышением температуры вследствие уменьшения движущей силы абсорбции, выражаемой при противоточном движении компонентов.
Движущую силу процесса абсорбции можно определить по уравнению (1.4.17):
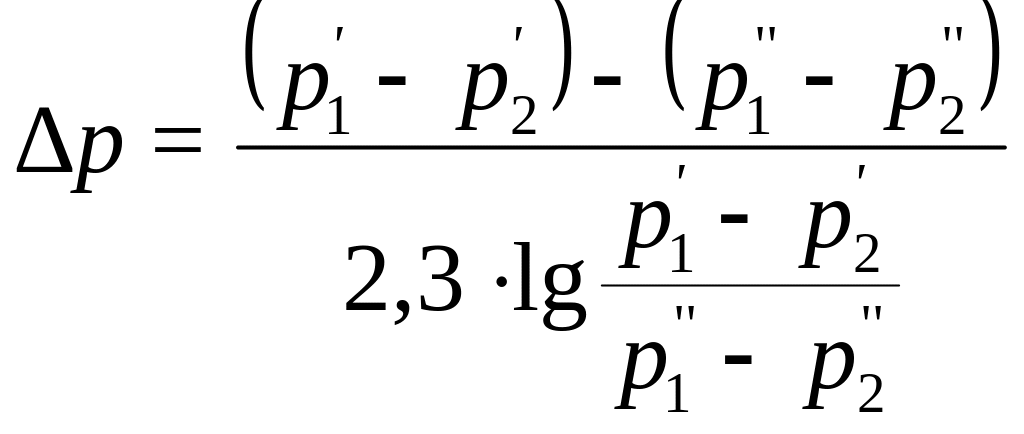
, (1.4.17)
где
p’1, p’’1 - парциальное давление SO3 в газе до и после абсорбера, Па;
p’2, p’’2 - равновесное давление SO3 над олеумом на входе газа в абсорбер и выходе из него, Па.
В производственных
условиях концентрация SO3
в газовой и жидкой фазах меняется
незначительно. Величина
![]() ,
зависит главным образом от температуры,
поскольку входящие в уравнение величины
связаны определенной зависимостью с
температурой, которая сильно возрастает
при ее повышении.
,
зависит главным образом от температуры,
поскольку входящие в уравнение величины
связаны определенной зависимостью с
температурой, которая сильно возрастает
при ее повышении.
Следовательно, с повышением температуры степень абсорбции SO3 сильно уменьшается и при определенной температуре абсорбция полностью прекращается. Максимальное содержание SO3 (своб.) в получаемом олеуме (при заданном содержании серного ангидрида в газе, поступающем на абсорбцию) зависит от температуры абсорбции, так как оно определяется равновесным давлением SO3 над олеумом.
После олеумного абсорбера газ направляется в моногидратный абсорбер, где происходит окончательная абсорбция серного ангидрида. Поглощение серного ангидрида при абсорбции должно быть полным, поскольку газовая смесь после абсорбции выбрасывается в атмосферу [1 – 5].
Абсорбция протекает с выделением значительного количества тепла, зависищее от концетрации исходного газа. Выпускаемые в настоящее время промышленностью разборные пластинчатые холодильники относятся к наиболее интенсивным типам теплообменных аппаратов. Их применение резко уменьшает попадание сточных вод в реки и другие водоемы при минимальных затратах энергии на прекачку жидкостей. Поэтому мною в данном дпломном проекте предложена замена двух холодильника АВЗ на пластинчатый холодильник «Альфа-Лаваль».
