
- •Реферат
- •Содержание
- •Введение
- •1 Литературный обзор
- •1.1 Физико-химические свойства серной кислоты
- •1.2 Методы получения серной кислоты
- •1.3 Методы охлаждения серной кислоты в теплообменниках
- •1.4 Физико-химические основы производства серной кислоты
- •1.4.1 Физико-химические основы процесса очистки газа
- •1.4.2 Физико-химические основы осушки газа
- •1.4.3 Потери сернистого ангидрида с сушильной кислотой
- •1.4.4 Физико-химические основы процесса окисления сернистого ангидрида
- •1.4.4 Физико-химические основы процесса абсорбции серного ангидрида
- •2 Описание технологического процесса производства контактной серной кислоты
- •2.1 Специальная очистка газа
- •2.1.1 Основы очистки газа в промывном отделении
- •2.1.2 Очистка от тумана серной кислоты
- •2.2 Осушка газа в башнях с насадкой, орошаемых крепкой серной кислотой
- •2.3 Окисление сернистого ангидрида до серного на поверхности ванадиевого катализатора
- •2.3.1 Сущность технологического процесса контактного отделения
- •2.4 Поглощение серного ангидрида в абсорберах, орошаемых моногидратом
- •3 Реконструкция холодильного оборудования сушильно-абсорбционного отделения
- •4 Технологические расчеты
- •4.1 Расчет материального баланса сушильно-абсорбционного отделения
- •4.1.1 Расчет материального баланса осушки газа
- •4.1.2 Расчет материального баланса абсорбции серного ангидрида
- •4.2 Тепловой расчет сушильно-абсорбционного отделения
- •4.2.1 Тепловой расчет сушильной башни
- •4.2.2 Тепловой расчет моногидратного абсорбера
- •4.2.3 Конструктивный и гидравлический расчет моногидратного абсорбера
- •4.3 Конструктивный расчет пластинчатого холодильника «Альфа-Лаваль»
- •4.3.1 Расчет поверхности теплообмена
- •4.3.2. Расчет схемы компоновки пластин
- •4.3.3 Расчет гидравлических сопротивлений
- •4.4 Расчет материального баланса контактного отделения
- •4.4.1 Расчет материального баланса контактного узла
- •4.5 Тепловой расчет контактного узла
- •433 Tх5 273 (tабс )
- •433 329 273 (Tабс )
- •433 Tх5 243 (tабс )
- •433 306 243 (Tабс )
- •39 119 Нм3/ч (0,82 Vисх.)
- •5 Безопасность жизнедеятельности
- •5.1 Краткая характеристика производства
- •5.2 Характеристика основных опасностей производства и условий труда
- •5.3 Обеспечение безопасности работы
- •5.3.1 Электробезопасность
- •5.3.2 Освещенность проектируемого цеха
- •5.3.3 Защита от шума и вибраций
- •5.3.4 Вентиляция и аспирация
- •5.3.5 Микроклимат рабочей зоны проектируемого цеха
- •5.3.6 Эргономика рабочего места
- •Р ис. 5.2. Зона досягаемости моторного поля в горизонтальной плоскости при высоте рабочей поверхности над полом 725мм
- •5.3.6.1 Требования к размещению технических устройств и рабочих мест
- •5.4 Пожаробезопасность
- •5.5 Требования безопасности в аварийных ситуациях
- •Выводы по разделу проекта бжд:
- •6 Технико-экономические расчеты
- •6.1 Расчет общей суммы капитальных вложений
- •6.2 Расчет амортизационных отчислений
- •6.3 Расчет материальных затрат в проектном варианте
- •6.4 Расчет численности работающих и фонда заработной платы
- •6.5 Расчет накладных расходов
- •6.6 Расчет изменения себестоимости продукции
- •6.7 Расчет показателей экономической эффективности инвестиций
- •Заключение
- •Библиографический список
1 Литературный обзор
1.1 Физико-химические свойства серной кислоты
Серная кислота – одна из самых активных неорганических кислот. Она реагирует почти со всеми металлами и их оксидами, вступает в реакции обменного разложения, энергично соединяется с водой, обладает окислительными и другими важными химическими свойствами.
Химический состав серной кислоты выражается формулой H2SO4 (молекулярная масса 98,08). Безводная серная кислота представляет собой при 20 °С бесцветную маслянистую жидкость, кристаллизующуюся при 10,37 °С. Техническая серная кислота окрашена примесями в темный цвет. При 296,2 °С и 0,98∙105 Па безводная серная кислота начинает кипеть с разложением до образования азеотропной смеси, содержащей 98,3 % мас. H2SO4 и 1,7 % мас. H2O и кипящей при 336, 5 °С.
С водой и триоксидом серы серная кислота смешивается в любых соотношениях. С повышением концентрации водных растворов серной кислоты температура их кипения увеличивается, достигая максимума в 336,5 °С при 98,3 % мас. H2SO4, а затем понижается (рис.1.1). Температура кипения олеума с увеличением содержания свободного SO3 снижается с 296,2 °С при 0 % мас. SO3 до 44,7 °С при 100 % мас. SO3, т. е. температуры кипения серного ангидрида.
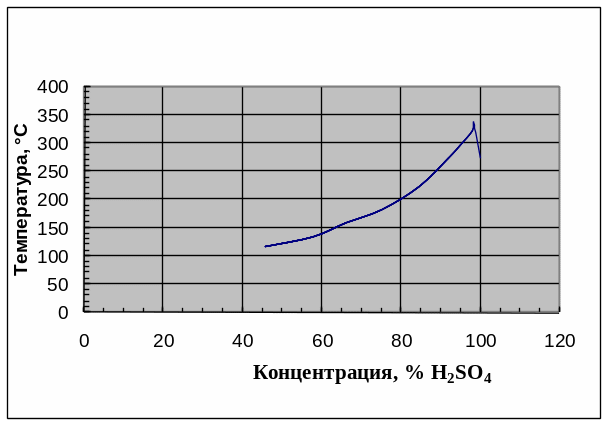
Рис. 1.1-Температура кипения водных растворов серной кислоты
При увеличении концентрации водных растворов серной кислоты общее давление паров над растворами понижается, а при 98,3 % мас. H2SO4 достигает минимума (рис.1.2). Низкое давление водяных паров над растворами концентрированной серной кислоты лежит в основе осушки газов и абсорбции серного ангидрида. При увеличении концентрации олеума общее давление паров над ним повышается.
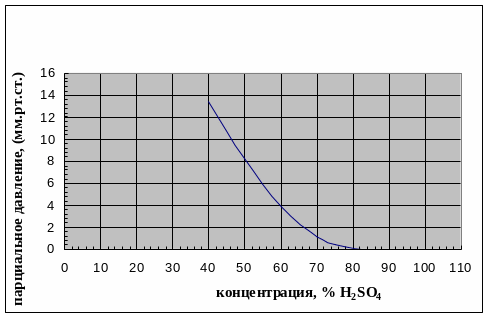
Рис. 1.2-Парциальное давление (в мм рт. ст.) паров воды над серной кислотой при 25ºС
С увеличением содержания H2SO4 плотность водных растворов серной кислоты повышается и достигает максимума при 98,3 % мас. H2SO4, затем несколько уменьшается и при 20 °С для серной кислоты концентрации 100 % мас. H2SO4 достигает 1,8305 г/см3. С повышением температуры плотность серной кислоты снижается.
С повышением концентрации водных растворов серной кислоты их теплоемкость уменьшается и достигает минимума для безводной серной кислоты 1,42 Дж/(г∙°С). С ростом температуры теплоемкость водных растворов серной кислоты несколько увеличивается.
С повышением концентрации водных растворов серной кислоты их вязкость увеличивается (рис.1.3), а с ростом температуры уменьшается (рис.1.4).
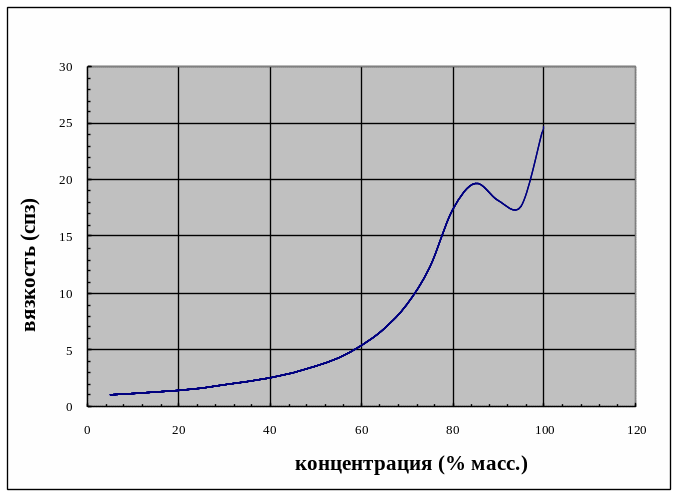
Рис. 1.3-Зависимость вязкости растворов серной кислоты (в cпз) от концентрации серной кислоты (в % масс.) при 25ºС
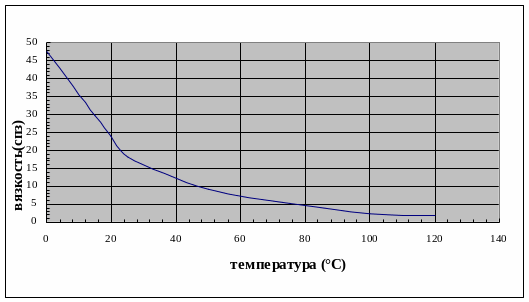
Рис. 1.4-Зависимость вязкости растворов серной кислоты (в спз) от температуры (в ºС) для 90 %-ой серной кислоты
Промышленность выпускает несколько сортов серной кислоты, различающихся содержанием H2SO4 , а также содержанием примесей. Состав и содержание примесей зависят от метода производства серной кислоты.
При получении серной кислоты в нее могут попадать частицы пыли, остающиеся в обжиговом газе даже после его очистки в сухих электрофильтрах. Серная кислота может быть также загрязнена продуктами коррозии аппаратуры, растворимыми в ней [1- 3].
Требования к качеству различных сортов серной кислоты регламентируются стандартами и представлены в ГОСТ 2184–77. Настоящий стандарт распространяется на техническую серную кислоту следующих видов: контактную (улучшенную и техническую); олеум (улучшенный и технический); башенную и регенерированную. В соответствии с ним по физико-химическим показателям серная кислота должна соответствовать нормам, которые указаны в табл.1.1.
Таблица 1.1 – Требования к качеству товарной серной кислоты [1]
Наименование показателя |
Норма |
|||||||
Контактная |
Олеум |
Башенная |
||||||
Улучшенная |
Техническая |
Улучшенный |
Технический |
|||||
Высший сорт |
Первый сорт |
Первый сорт |
Второй сорт |
Высший сорт |
Первый сорт |
|||
1. Массовая доля моногидрата (H2SO4), %, не менее |
от 92,5 до 94,0 |
92,5 |
— |
— |
— |
75,0 |
||
2. Массовая доля свободного серного ангидрида (SO3), %, не менее |
— |
— |
— |
— |
24 |
24 |
19 |
— |
3. Массовая доля железа (Fe), %, не более |
0,007 |
0,015 |
0,02 |
0,1 |
0,007 |
0,01 |
— |
0,05 |
4. Массовая доля остатка после прокаливания, %, не более |
0,02 |
0,03 |
0,05 |
— |
0,02 |
0,03 |
— |
0,3 |
5. Массовая доля окислов азота (N2O3), %, не более |
0,00005 |
0,0001 |
— |
— |
0,0002 |
0,0005 |
— |
0,05 |
6. Массовая доля мышьяка (As), %, не более |
0,00008 |
0,0001 |
— |
— |
0,00008 |
0,0001 |
— |
— |
7. Массовая доля хлористых соединений (Cl), %, не более |
0,0001 |
0,0005 |
— |
— |
— |
— |
— |
— |
8. Массовая доля свинца (Pb), %, не более |
0,001 |
0,01 |
— |
— |
0,0001 |
— |
— |
— |
