
- •Глава 11 написана г. О. Митом, г. Гамбург
- •Сырье 37
- •Визуальное и ручное обследование 180
- •2.10. Техника безопасности в солодовенном предприятии (цехе) 192
- •Кипячение сусла 312
- •3 .9.3. Аэрация сусла 347
- •Управление и контроль за технологическими процессами производства сусла 351
- •Техника безопасности при производстве сусла 353
- •4.2. Разведение чистой культуры дрожжей 380
- •Комплектная линия розлива 656
- •6.1. Материалы, используемые для изготовления емкостей и трубопроводов, и их устойчивость по отношению
- •Проведение мойки и дезинфекции в системе cip 685
- •11. От автоматизации - к интеграции технологических
- •11.2. Обозначения и системный подход к проектированию систем автоматизации пивоварения в соответствии с общими
- •11.3. КиПиА согласно din и в практике автоматизации
- •25 Балтика
- •0. Пиво — древнейший народный напиток
- •1. Сырье
- •1.1. Ячмень
- •1.1.1. Группы и сорта ячменя
- •1.1.1.1. Группы ячменя
- •1.1.1.2. Сорта ячменя
- •1.1.2. Возделывание ячменя
- •1.1.3. Строение
- •1.1.3.1. Наружное строение
- •1.1.3.2. Внутреннее строение
- •1.1.4. Состав и свойства отдельных частей ячменя
- •1.1.4.1.2. Сахар
- •1.1.4.1. Углеводы
- •1.1.4.2. Белковые вещества
- •1.1.4.2.2. Продукты
- •1.1.4.3. Жиры (липиды)
- •1.1.4.4. Минеральные вещества
- •1.1.4.5. Прочие вещества
- •1.1.5. Оценка качества ячменя
- •1.1.5.1. Визуальное и ручное обследование
- •1.1.5.2. Технохимический анализ
- •1.1.5.2.2. Масса 1000 зерен
- •1.1.5.2.3. Масса гектолитра
- •1.1.5.2.4. Проба на срез
- •1.1.5.2.5. Технохимический анализ
- •1.1.5.3. Физиологические исследования
- •1.1.5.3.1. Прорастаемость
- •1.1.5.3.2. Энергия и способность прорастания
- •1 .2. Хмель
- •1.2.1. Области возделывания хмеля
- •1.2.2. Сбор, сушка и предохранение хмеля от порчи
- •1.2.2.1. Сбор хмеля
- •1.2.2.2. Сушка хмеля
- •1.2.2.3. Стабилизирующая обработка
- •1.2.3. Строение хмелевой шишки
- •1.2.4. Состав и свойства компонентов хмеля
- •1.2.4.1. Горькие вещества или хмелевые смолы
- •1.2.4.2. Хмелевое эфирное масло
- •1.2.4.3. Дубильные вещества (полифенолы)
- •1.2.4.4. Белковые вещества
- •1.2.5. Оценка качества хмеля
- •1.2.5.1. Ручная оценка качества хмеля в шишках
- •1.2.5.2. Содержание в хмеле горьких веществ
- •1.2.6. Сорта хмеля
- •1.2.7. Хмелепродукты
- •1.2.7.1. Гранулированный хмель
- •1.2.7.2. Экстракты хмеля
- •1.3. Вода
- •1.3.1. Круговорот воды
- •1.3.2. Потребление воды в пивоваренном производстве
- •1.3.3. Забор воды
- •1.3.3.1. Забор подземных вод
- •1.3.3.2. Забор поверхностных вод
- •1.3.3.3. Значение собственного водоснабженния
- •1.3.4. Требования к воде
- •1.3.4.1. Требования к питьевой воде
- •1.3.4.2. Требования к воде для пивоварения
- •1.3.5. Способы улучшения состава воды
- •1.3.5.1. Способы удаления взвешенных частиц
- •1.3.5.2. Удаление растворенных в воде веществ
- •1.3.5.3. Способы улучшения
- •1.3.5.3.1. Декарбонизация
- •1.3.5.4. Обеззараживание воды
- •1.3.5.4.1. Обеззараживание фильтрованием
- •1.3.5.4.2. Обеззараживание ультрафиолетом
- •1.3.5.4.3. Обеззараживание озоном
- •1.3.5.4.4. Обеззараживание
- •1.3.5.4.5. Обеззараживание двуокисью хлора
- •1.3.5.4.6. Обеззараживание ионами серебра
- •1.3.5.5. Способы деаэрации воды
- •1.4. Дрожжи
- •1.4.1. Строение и состав дрожжевой клетки
- •1.4.2. Обмен веществ дрожжевой клетки
- •1.4.3. Размножение и рост дрожжей
- •1.4.4. Характеристики
- •1.4.4.1. Морфологические признаки
- •1.4.4.2. Физиологические различия
- •1.4.4.3. Технологические различия при сбраживании
- •1.4.4.4. Систематическая классификация
- •1.5. Несоложеное сырье
- •1.5.1. Кукуруза
- •1.5.3. Ячмень
- •1.5.4. Сорго
- •1.5.5. Пшеница
- •1.5.6. Сахарный колер
- •1.5.7. Сахар
- •105 Балтика
- •2. Производство солода
- •2.1. Приемка, очистка, сортирование и транспортирование ячменя
- •2.1.1. Приемка ячменя
- •2.1.1.1. Приемка ячменя с рельсового или автомобильного транспорта
- •2.1.1.2. Приемка ячменя
- •2.1.2. Очистка
- •2.1.2.1. Предварительная очистка ячменя
- •2.1.2.2. Магнитные сепараторы
- •2.1.2.3. Камнеотборник
- •2.1.2.4. Обоечная машина
- •2.1.2.5. Триер
- •2.1.2.6. Сортирование ячменя
- •2.1.2.6.1. Основа
- •2.1.2.6.2. Сортировочный цилиндр
- •2.1.2.6.3. Планзихтер
- •2.1.3. Транспортирование ячменя и солода
- •2.1.3.1. Механические
- •2.1.3.1.1. Нория или элеватор
- •2.1.3.1.2. Шнековый транспортер
- •2.1.3.1.3. Скребковый цепной транспортер
- •2.1.3.1.4. Ленточный транспортер
- •2.1.3.2. Пневматические
- •2.1.3.2.1. Всасывающая
- •2.1.3.2.2. Нагнетательная
- •2.1.4.1. Циклоны
- •2.1.4.2. Пылеотделительный фильтр
- •2.1.4.2.1. Пылеотделительный фильтр старой конструкции
- •2.1.4.2.2. Пылеотделительный фильтр новой конструкции
- •2.1.4.2.2.1. Рукавный фильтр
- •2.1.4.2.2.2. Прочие
- •2.2. Сушка и хранение ячменя
- •2.2.1. Дыхание ячменя
- •2.2.2. Сушка ячменя
- •2.2.3. Охлаждение ячменя
- •2.2.4. Хранение ячменя
- •2.2.4.1. Хранение в силосах
- •2.2.4.2. Хранение на складах
- •2.2.4.3. Заражение вредителями
- •2.2.4.3.1. Насекомые-вредители
- •2.2.4.3.2. Плесени
- •2.3. Замачивание ячменя
- •2.3.1. Процессы, происходящие при замачивании
- •2.3.1.1. Водопоглощение
- •2.3.1.2. Снабжение кислородом
- •2.3.1.3. Очистка
- •2.3.2. Замочные чаны
- •2.3.3. Проведение замачивания
- •2.4. Проращивание ячменя
- •2.4.1. Процессы, происходящие при проращивании
- •2.4.1.1. Процессы роста
- •2.4.1.2. Образование ферментов
- •2.4.1.2.1. Ферменты,
- •2.4.1.2.2. Прочие группы ферментов
- •2.4.1.3. Превращения веществ при проращивании
- •2.4.1.3.1. Растворение и расщепление β-глюкана
- •2.4.1.3.2. Расщепление крахмала
- •2.4.1.3.3. Расщепление белковых веществ
- •2.4.1.3.4. Расщепление жиров (липидов)
- •2.4.1.3.5. Образование
- •2.4.1.3.6. Регуляторы прорастания
- •2.4.2. Способы проращивания
- •2.4.2.1. Токовая солодовня
- •2.4.2.2. Системы
- •2.4.2.2.1. Кондиционирование аэрационного воздуха
- •2.4.2.2.2. Солодовня барабанного типа
- •2.4.2.2.3. Солодовня ящичного типа
- •2.4.2.2.3.1. Прямоугольные
- •158 Рис. 2.52. Принцип работы башенной солодовни:
- •2.4.2.2.4. Системы с ежесуточным перемещением
- •2.4.2.3. Контроль
- •2.5. Сушка солода
- •2.5.1. Изменения, происходящие при сушке
- •2.5.1.1. Понижение влажности
- •2.5.1.2. Прерывание процессов прорастания и растворения
- •2.5.1.3. Образование красящих и ароматических веществ (реакции Майяра)
- •2.5.1.4. Образование дмс при сушке
- •2.5.1.5. Образование нитрозаминов
- •2.5.1.6. Инактивация ферментов
- •2.5.2. Устройство сушилок
- •2.5.2.1. Отопление и вентиляция сушилки
- •2.5.2.2. Двухъярусные сушилки (старая конструкция)
- •2.5.2.3. Сушилки
- •2.5.2.4. Высокопроизводительные сушилки с погрузочно-разгрузочными устройствами
- •2.5.2.5. Вертикальные сушилки
- •2.5.3. Процесс сушки
- •2.5.3.1. Производство светлого солода (пильзенского типа)
- •2.5.3.2. Производство темного солода (мюнхенского типа)
- •2.5.3.3. Выгрузка солода из сушилки
- •2.5.3.4. Контроль за процессом сушки
- •2.6. Обработка солода после сушки
- •2.6.1. Охлаждение
- •2.6.2. Очистка солода
- •2.6.3. Хранение солода
- •2.6.4. Полировка солода
- •2.7. Выход солода в производстве
- •2.8.2.5. Стекловидность
- •2.8.2.6. Рыхлость
- •2.8.2.7. Длина зародышевого листка
- •2.8.2.8. Всхожесть
- •2.8.2.9. Плотность
- •2.8.2.10. Метод окрашивания среза зерна (модификация Carlsberg)
- •2.8.3. Технохимический контроль
- •2.8.3.1. Влажность
- •2.8.3.2. Конгрессный способ затирания
- •2.8.4. Договор на поставку солода
- •2.9. Специальные типы солода и солод из прочих зерновых
- •2.9.1. Светлый солод пильзенского типа
- •2.9.2. Темный солод (мюнхенский тип)
- •2.9.3. Темный солод венского типа
- •2.9.4. Карамельный солод
- •2.9.5. Томленый солод
- •2.9.6. Жженый солод
- •2.9.7. Кислый солод
- •2.9.8. Солод короткого ращения
- •2.9.9. Пшеничный солод
- •2.9.10. Солод из прочих хлебных злаков
- •2.9.11. Солод из сорго
- •2.9.12. Красящее пиво
- •2.9.13. Применение
- •2.10. Техника безопасности в солодовенном предприятии (цехе)
- •3. Производство сусла
- •3.1. Дробление солода
- •3.1.1. Подработка солода
- •3.1.1.1. Удаление из солода пыли и камней
- •3.1.1.2. Взвешивание засыпи
- •3.1.1.2.1. Весы с опрокидывающимся ковшом
- •3.1.1.2.2. Весы с открывающимся днищем
- •3.1.2. Основы дробления
- •3.1.3. Сухое дробление
- •3.1.3.1. Шестивальцовые дробилки
- •206 Рис. 3.7. Шестивальцовая
- •3.1.3.2. Пятивальцовые дробилки
- •3.1.3.3. Четырехвальцовые дробилки
- •3.1.3.4. Двухвальцовые дробилки
- •3.1.3.5. Вальцы дробилки
- •3.1.3.6. Кондиционированное сухое дробление
- •3.1.3.7. Бункер для дробленых зернопродуктов
- •3.1.3.8. Молотковые дробилки
- •3.1.4. Мокрое дробление
- •Откачка замочной воды.
- •3.1.5. Замочное
- •3.1.6. Оценка качества помола
- •3.2. Затирание
- •3.2.1. Превращения веществ при затирании
- •3.2.1.1. Цель затирания
- •3.2.1.2. Свойства ферментов
- •3.2.1.3. Расщепление крахмала
- •3.2.1.3.1. Влияние температуры
- •3.2.1.3.2. Влияние длительности
- •3.2.1.3.3. Влияние величины рН
- •3.2.1.3.4. Влияние концентрации затора на расщепление крахмала
- •3.2.1.3.5. Контроль расщепления крахмала
- •3.2.1.4. Расщепление β-глюкана
- •3.2.1.5. Расщепление белковых веществ
- •3.2.1.6. Превращения жиров (липидов)
- •3.2.1.8. Биологическое подкисление
- •3.2.1.8.1. Добавление неорганических кислот
- •3 .2.1.9. Состав экстрактивных веществ сусла
- •3.2,1.10. Заключительные рекомендации по проведению затирания
- •3.2.2. Заторные аппараты
- •3.2.3. Начало затирания
- •3.2.3.1. Гидромодуль затора
- •3.2.3.2. Температура начала затирания
- •3.2.4. Способы затирания
- •3.2.4.1. Различные точки
- •3.2.4.2. Настойные способы
- •3.2.4.3. Отварочные способы затирания
- •3.2.4.3.1. Одноотварочные способы
- •3.2.4.3.2. Двухотварочные способы
- •3.2.4.3.3. Трехотварочные способы
- •3.2.4.2.4. Специальные способы затирания
- •3.2.4.3.5. Способы затирания
- •3.2.5. Продолжительность затирания
- •3.2.6. Контроль затирания
- •3.3. Фильтрование затора
- •3.3.1. Первое сусло
- •3.3.2. Последняя промывная вода
- •3.3.3. Фильтрационный чан
- •3.3.3.1. Фильтрчан старой конструкции (рис. 3.46)
- •3.3.3.2. Фильтрационные чаны новой конструкции (рис. 3.48 и 3.48а)
- •3.3.3.3. Последовательность операций при работе на фильтрчане
- •3.3.4. Фильтрование
- •3.3.4.1. Фильтр-пресс старой конструкции
- •3.3.4.2.2.Последовательность операций при работе на фильтр-прессе 2001 (рис. 3.61а)
- •2. Фильтрование
- •3. Первое сжатие
- •4. Промывка дробины
- •5. Последнее сжатие
- •3.3.4.2.3.Прочие современные фильтр-прессы
- •3.3.5. Дробина
- •3.3.5.1. Транспортирование дробины
- •3.3.5.2. Анализ дробины
- •3.3.6. Солодовый экстракт
- •3.4. Кипячение сусла
- •3.4.1. Процессы, происходящие при кипячении сусла
- •I растворение и превращение компонентов хмеля;
- •I выпаривание воды;
- •I стерилизация сусла;
- •3.4.1.3. Испарение воды
- •3.4.1.4. Стерилизация сусла
- •3.4.1.5. Разрушение всех ферментов
- •3.4.1.6. Повышение цветности сусла
- •3.4.1.7. Повышение кислотности сусла
- •3.4.1.8. Образование редуцирующих веществ (редуктонов)
- •3.4.1.9. Изменение содержания диметилсульфида во время и после кипячения сусла
- •3.4.1.10. Содержание цинка в сусле
- •3.4.1.11. Неохмеленное сусло
- •3.4.2. Устройство и обогрев сусловарочного котла
- •3.4.2.1. Сусловарочный котел с прямым обогревом
- •3.4.2.2. Сусловарочный котел с паровым обогревом
- •3.4.2.2.1. Температура
- •3.4.2.2.2. Оснащение сусловарочного котла с паровой рубашкой в виде двойного дна
- •3.4.2.2.3. Форма и материал
- •Описание котла (выборочно)
- •3.4.2.2.4. Кипячение с использованием горячей воды (гидрокипячение)
- •3.4.2.3. Сусловарочные котлы
- •3.4.2.3.1. Кипячение при низком избыточном давлении с выносным кипятильником
- •3.4.2.4. Высокотемпературное кипячение сусла
- •3.4.2.5.1. Конденсация
- •3.4.2.6. Потребление энергии при кипячении сусла
- •3 .4.2.7. Конденсат вторичного пара
- •3.4.2.8. Сборник сусла
- •3.4.3. Технология кипячения сусла
- •3.4.3.1. Кипячение сусла
- •3.4.3.2. Внесение хмеля
- •3.4.3.2.1. Расчет дозировки хмеля
- •3.4.3.2.2. Состав и момент внесения хмеля
- •3.4.3.2.3. Способы внесения хмеля
- •3.4.4. Контроль готового сусла
- •3.5. Выход экстракта в варочном цехе
- •3 .5.1. Расчет выхода экстракта в варочном цехе
- •3.5.1.1. Определение массовой доли сухих веществ
- •3.5.1.2. Определение объемно-массовой доли сухих веществ в сусле (содержание экстракта в 1 гл сусла)
- •3.5.1.3. Пересчет объема горячего охмеленного сусла на холодное сусло
- •3.5.1.4. Расчет массы экстракта, полученного в варочном цехе
- •3.5.1.5. Определение выхода
- •3.5.2. Факторы, оказывающие влияние на выход экстракта в варочном цехе
- •3.5.3. Пример расчета выхода экстракта в варочном цехе
- •3.6. Состав оборудования варочного цеха
- •3.6.1. Количество аппаратов и их размещение
- •3.6.2. Размеры аппаратов варочного цеха
- •3.6.3. Материал для
- •3.6.4. Производственная
- •3.6.5. Варочные агрегаты
- •3.6.5.1. Варочные агрегаты мини-пивзаводов ресторанного типа
- •3.6.5.2. Интегральный варочный агрегат
- •3.6.5.3. Экспериментальные и учебные варочные агрегаты
- •3.7. Перекачка горячего охмеленного сусла
- •3.8. Отделение взвесей горячего сусла
- •3.8.1. Холодильная тарелка
- •3.8.2. Отстойный чан
- •3.8.3. Вирпул
- •3.8.3.1. Принцип действия вирпула
- •3.8.3.2. Конструкция вирпула
- •3.8.3.3. Технология осветления сусла в вирпуле
- •3.8.4. Сепараторы
- •3.8.4.1. Принцип
- •3.8.4.3. Устройство и способ действия
- •3.8.4.3.1. Принцип работы тарельчатых барабанов
- •3.8.5. Получение сусла из белкового отстоя
- •3 .9. Охлаждение
- •3.9.1. Процессы при охлаждении
- •3.9.1.1. Охлаждение сусла
- •3.9.1.2. Оптимальное удаление образующихся взвесей холодного сусла
- •3.9.1.3. Аэрация сусла
- •3.9.1.4. Изменения экстрактивности сусла
- •3.9.2. Аппараты
- •3.9.2.1. Устройство пластинчатого теплообменника
- •I очень тонкие металлические пластины;
- •3.9.2.2. Принцип работы пластинчатого холодильника
- •3.9.2.3. Преимущества пластинчатого холодильника
- •3.9.3. Аэрация сусла
- •3.9.3.1. Устройства для аэрации сусла
- •3.9.3.2. Момент проведения аэрации дрожжей.
- •3.9.4. Аппараты для удаления взвесей холодного сусла
- •3.9.4.1. Кизельгуровый
- •3.9.4.2. Флотация
- •3.9.4.3. Сепарирование холодного сусла
- •3.9.5. Компоновка оборудования линии охлаждения сусла
- •3.10. Управление и контроль за технологическими процессами производства сусла
- •3.11. Техника безопасности при производстве сусла
- •3.11.1. Предупреждение несчастных случаев вблизи дробилки
- •3.11.2. Предупреждение несчастных случаев при работах в аппаратах варочного цеха
- •3.11.3. Предупреждение несчастных случаев при работе с сепараторами
- •4. Производство пива (брожение, созревание и фильтрование)
- •4.1. Превращения при брожении и созревании
- •4.1.1. Дрожжи
- •4.1.2. Метаболизм дрожжей
- •4.1.2.1. Сбраживание Сахаров
- •4.1.2.1.2. Получение энергии при брожении
- •4.1.2.2. Метаболизм азотистых веществ
- •4.1.2.5. Метаболизм минеральных веществ
- •4.1.3. Образование и расщепление побочных продуктов брожения
- •4.1.3.1. Диацетил (вицинальные дикетоны)
- •4.1.3.2. Альдегиды (карбонилы)
- •4.1.3.3. Высшие спирты
- •4.1.3.4. Эфиры
- •4.1.3.5. Сернистые соединения
- •4.1.3.6. Органические кислоты
- •4.1.4. Другие процессы и превращения
- •4.1.4.1. Изменения азотистого состава
- •4.1.4.2. Понижение рН
- •4.1.4.3. Изменение
- •4.1.4.4. Изменение цветности пива
- •4.1.4.5. Выделение горьких
- •4.1.4.6. Насыщенность пива со2.
- •4.1.4.7. Осветление и коллоидная стабилизация пива
- •4.1.5. Влияние на дрожжи различных факторов
- •4.1.6. Флокуляция дрожжей (хлопьеобразование)
- •4.2. Разведение чистой культуры дрожжей
- •4.2.1. Факторы,
- •4.2.2. Выделение пригодных дрожжевых клеток
- •4.2.3. Разведение чистой культуры в лаборатории
- •4.2.4. Разведение
- •4.2.4.1. Установки для
- •4.2.4.2. Ассимиляционный способ
- •4.2.4.3. Способ разведения
- •4.2.4.4. Выращивание дрожжей открытым способом
- •25 Л молодого пива для пересева;
- •4.3. Классическое брожение и созревание
- •4.3.1. Бродильные чаны и оснащение бродильного отделения
- •4.3.1.1. Бродильные чаны
- •4.3.1.2. Оснащение открытого бродильного отделения
- •Дрожжевое отделение, где хранятся дрожжи.
- •4.3.2. Выход экстракта в бродильном отделении
- •4.3.3. Главное брожение в открытых чанах
- •4.3.3.1. Внесение дрожжей
- •4.3.3.1.1. Перемешивание и аэрация дрожжей
- •4.3.3.2. Технология брожения в чане
- •4.3.3.2.1. Стадии брожения
- •4.3.3.2.2. Температура брожения
- •4.3.3.3. Степень сбраживания
- •4.3.3.4. Перекачка пива из бродильного отделения
- •4.3.4. Сбор дрожжей из чана
- •4.3.5. Процессы, протекающие при созревании пива в танках традиционной конструкции
- •4.3.5.1. Насыщение пива диоксидом углерода под избыточным давлением
- •4.3.5.2. Осветление пива
- •4.3.6. Устройство классического отделения дображивания
- •4.3.6.1. Устройство отделения дображивания
- •4.3.6.2. Лагерные танки (танки дображивания)
- •4.3.7. Дображивание в лагерных танках
- •4.3.7.1. Перекачка пива
- •4.3.8. Соединение лагерного танка с линией розлива
- •4.3.8.1. Установление соединения
- •4.3.8.2. Давление при опорожнении танка
- •4.3.9. Перекачка из танков
- •4.3.9.1. Смеситель
- •4.3.9.2. Регулятор давления (друкреглер)
- •4.3.9.3. Получение пива
- •4.3.9.4. Глубокое охлаждение пива
- •4.3.9.5. Фильтрационные остатки
- •4.4. Брожение и созревание в цилиндроконических танках (цкт)
- •4.4.1. Конструкция и установка
- •4.4.1.1. Изготовление, форма и материал цкт
- •4.4.1.2. Размер цкт
- •4.4.1.2.1. Высота сусла в цктб
- •4.4.1.3. Установка и
- •4.4.2. Оборудование цкт
- •4.4.2.1. Контрольные приборы, элементы для обслуживания танка и предохранительная арматура
- •4.4.2.1.1. Оборудование для наполнения и опорожнения цкт
- •4.4.2.1.2. Арматура, устанавливаемая на куполе танка
- •4.4.2.1.3. Контрольные приборы
- •4.4.2.2. Охлаждение цкт
- •4.4.2.2.1. Потребность в холоде
- •4.4.2.2.2. Варианты охлаждения
- •4.4.2.2.3. Теплопередача
- •4.4.2.2.5. Теплоизоляция
- •4.4.2.3. Автоматизация и управление охлаждением
- •I Измерение количества со2.
- •4.4.3. Брожение
- •4.4.3.1. Некоторые аспекты брожения и созревания в цкт
- •4.4.3.2. Холодное брожение — холодное созревание
- •4.4.3.3. Холодное брожение
- •4.4.3.4. Теплое брожение без давления — холодное созревание
- •4.4.3.5. Брожение под давлением
- •4.4.3.6. Холодное брожение — теплое созревание
- •4.4.3.7. Холодное главное брожение
- •4.4.3.8. Теплое главное брожение с нормальным или форсированным созреванием
- •4.4.4. Сбор дрожжей из цкт
- •4.4.4.1. Момент сбора дрожжей
- •4.4.4.2. Методы сбора дрожжей
- •4.4.4.3. Обработка и хранение семенных дрожжей
- •4.4.4.3.1. Аэрация семенных дрожжей
- •4.4.4.3.2. Температура хранения дрожжей
- •4.4.4.3.3 Способы хранения дрожжей
- •4.4.4.4. Контроль семенных дрожжей
- •4.4.5. Качество пива перед фильтрованием
- •4.4.6. Рекуперация пива из избыточных дрожжей (пиво из дрожжевого осадка)
- •4.4.6.1. Прессование дрожжей
- •4.4.6.2. Сепарация дрожжей
- •4.4.6.3. Мембранное фильтрование дрожжей
- •4.4.6.4. Обработка пива, рекуперированного из дрожжей
- •4.4.7. Мойка цкт
- •4.4.8. Рекуперация с02
- •4.4.9. Иммобилизованные дрожжи
- •4.5. Фильтрование пива
- •4.5.1. Виды фильтрования
- •4.5.1.1. Механизмы осаждения
- •4.5.1.2. Фильтрующие перегородки
- •4.5.1.3. Вспомогательные
- •1000Х). (Фото: Schenk Filterbau GmbH, г. Вальд-
- •4.5.2. Виды фильтров
- •4.5.2.1. Масс-фильтр
- •4.5.2.2. Намывные фильтры
- •4.5.2.2.1. Намывка фильтрующих слоев
- •4.5.2.2.1.3. Роль кислорода
- •4.5.2.2.1.4. Дозаторы
- •4.5.2.2.2 Намывной рамный фильтр-пресс
- •4.5.2.2.3. Намывной свечной (патронный) фильтр
- •4.5.2.2.4. Намывной дисковый фильтр (фильтр с горизонтальными ситами)
- •4.5.2.2.5. Технические проблемы при фильтровании
- •4.5.2.2.6. Переработка разбавленных фильтрационных остатков
- •4.5.2.2.7. Кизельгуровая фильтрационная установка
- •4.5.2.3. Пластинчатый фильтр-пресс
- •4.5.2.4. Мембранные фильтры
- •4.5.2.4.1. Фильтр с модульными элементами
- •4.5.2.4.2. Мембранный свечной фильтр
- •4.5.2.5. Фильтрационная
- •4.5.2.6. Тонкость фильтрования
- •4.5.2.7. Тангенциально-поточное (Cross-flow) фильтрование
- •4.6. Стабилизация пива
- •4.6.1. Биологическая стабилизация пива
- •4.6.1.1. Пастеризация
- •4.6.1.2. Пастеризация в потоке
- •4.6.1.2.1. Пластинчатый пастеризатор
- •4.6.1.2.2. Температура и длительность термической обработки
- •4.6.1.2.3. Влияние пастеризации в потоке на качество пива
- •4.6.1.3. Горячий розлив пива
- •4.6.1.4. Пастеризация в туннель ном пастеризаторе
- •4.6.1.5. Холодно-стерильный розлив пива
- •4.6.2. Коллоидная
- •4.6.2.1. Характер коллоидного помутнения
- •4.6.2.2. Улучшение коллоидной стойкости пива
- •4.6.2.3. Технологические пути улучшения коллоидной стойкости пива
- •4 .6.2.4. Использование стабилизирующих средств
- •4.6.2.4.1. Силикагели
- •4.6.2.4.2. Поливинилполипирролидон (пвпп)
- •4.6.3. Фильтрационная линия
- •4.6.4. Вкусовая стойкость пива
- •4.6.4.1. Карбонилы, вызывающие старение вкуса (карбонилы старения)
- •1Дёлер - 100%-ная концентрация качества!
- •4.6.4.3. Приемы, позволяющие исключить попадание кислорода на пути от лагерного танка до розлива
- •4.6.4.4. Приемы, позволяющие исключить отрицательное изменение вкуса после розлива
- •4.7. Карбонизация пива
- •4.8. Особые способы приготовления пива
- •4.8.1. Высокоплотное пивоварение
- •4.8.2. Изготовление ледяного пива (Eisbier)
- •4.8.3. Методы удаления спирта из пива
- •4.8.3.1. Мембранные методы
- •4.8.3.1.1, Обратный осмос
- •4.8.3.1.2. Диализ
- •4.8.3.2. Термические способы удаления спирта/ дистилляция
- •4.8.8.3. Подавление образования спирта
- •4.9. Техника безопасности в отделениях брожения, дображивания и фильтрования
- •4.9.1. Несчастные случаи из-за углекислоты брожения
- •4.9.2. Техника безопасности при работе с цкт
- •4.9.3. Техника безопасности при работе с кизельгуром
- •5.1.1.2. Изготовление стеклянных бутылок
- •5.1.1.3. Формы бутылок
- •5.1.1.4. Цвет бутылки
- •5.1.1.5. Обработка поверхности бутылки
- •5.1.1.6. Износ (скаффинг)
- •5.1.1.7. Дополнительная защитная обработка бутылок
- •5.1.1.8. Бутылки многоразового использования
- •5.1.1.9. Последовательность технологических операций при использовании стеклянных бутылок многоразового использования
- •5.1.2. Мойка бутылок многоразового использования
- •5.1.2.1. Факторы, влияющие на чистоту бутылок
- •5.1.2.2. Бутылкомоечные машины
- •5.1.2.2.1. Конструкции
- •5.1.2.2.2. Основные
- •5.1.2.3. Моющий щелочной раствор
- •5.1.2.3.1. Требования к моющему щелочному расвору
- •5 .1.2.3.2. Состав моющего
- •5.1.2.3.3. Поддержание
- •5.1.2.3.4. Подготовка моющего щелочного раствора
- •5.1.2.3.5. Расход воды
- •5 .1.2.4. Техническое
- •5.1.4. Наполнение бутылок
- •5.1.4.1. Основные принципы розлива
- •5.1.4.2. Принципиальные конструктивные решения разливочно-укупорочных блоков
- •5.1.4.3. Основные узлы разливочно-укупорочного блока
- •5.1.4.4. Конструкция
- •5.1.4.5. Способ вспрыска воды под высоким давлением
- •5.1.5. Укупоривание бутылок
- •5.1.5.1. Укупоривание бутылок кронен-пробками
- •5.1.5.2. Укупоривание пробкой с пружинным хомутом
- •5.1.6. Промывка
- •5.1.7. Контроль наполненных и укупоренных бутылок
- •5.1.7.1. Контроль уровня наполнения
- •5.1.7.2. Кислород в горлышке бутылки
- •5.1.8. Пастеризация в бутылках
- •5.1.8.1. Обоснование пастеризации в бутылках
- •5.1.8.2. Важнейшие
- •5.1.8.3. Система обеспечения необходимого количества пе
- •5.1.9. Нанесение этикеток и фольги на бутылки
- •5.1.9.2. Этикеточный клей
- •5.1.9.3. Основной принцип нанесения этикеток
- •5.1.9.4. Конструктивные элементы этикетировочного автомата
- •5.1.9.5. Нанесение фольги на головку бутылки
- •5.1.10. Датирование
- •5.2. Особенности розлива в стеклянные одноразовые бутылки
- •5.2.1. Распаковка новых стеклянных бутылок
- •5.2.2. Ополаскивание
- •5.3. Розлив напитков в многоразовые пэт-бутылки
- •5.3.1. Пластиковые бутылки
- •5.3.1.2. Прочие виды
- •5.3.2. Изготовление пэт-бутылок
- •5.3.3. Транспортировка пустых пэт-бутылок
- •5.3.4. Мойка пэт-бутылок многоразового использования
- •5.3.5. Инспектирование
- •5.3.6. Процесс розлива в пэт-бутылки
- •5.3.7. Укупоривание пэт-бутылок
- •5.3.7.1. Алюминиевые колпачки
- •5.3.7.2. Пластмассовые
- •5.3.8. Этикетирование пэт-бутылок
- •5.4. Особенности наполнения одноразовых пэт-бутылок
- •5.5. Розлив пива в банки
- •5.5.1. Банки и их укупоривание
- •5.5.2. Складирование,
- •5.5.3. Инспектирование пустых банок
- •5.5.4. Ополаскивание банок
- •5.5.5. Наполнение банок
- •5.5.5.1. Разливочный автомат с дозированием по уровню
- •5.5.5.2. Разливочный автомат с дозированием по объему
- •5.5.6. Укупоривание банок
- •5.5.7. Мойка блоков розлива и укупоривания банок
- •5.5.8. Виджеты
- •5.5.9. Инспектирование полных банок
- •5.5.10. Пастеризация
- •5.5.11. Круговое
- •5.5.12. Датирование банок
- •5.6. Розлив в бочки, кеги, специальные бочонки и большие жестяные банки
- •5.6.2. Кеги и фитинги
- •5.6.3. Мойка и наполнение кегов
- •5.6.3.2. Наполнение кегов
- •5.6.4. Линия розлива в кеги
- •5.6.5. Розлив в малые
- •5.6.6. Розлив в большие банки
- •5.7. Упаковка
- •5.7.1. Транспортировка бутылок и банок
- •5.7.2. Обработка новых стеклянных бутылок и банок
- •5.7.3. Виды упаковки, транспортировка
- •5.7.3.1. Виды упаковки
- •5.7.3.2. Транспортировка единиц упаковки
- •5.7.3.4. Складирование ящиков
- •5.7.3.5. Мойка ящиков
- •5.7.4. Выемка и укладка
- •5.7.4.1. Захватные головки и захватные патроны
- •5.7.4.2. Виды укладчиков
- •5.7.4.2.1. Укладчик с прерывистым движением
- •5.7.4.2.2. Мультипакер
- •5.7.4.2.3. Круговой укладчик
- •5.7.4.3. Переориентирующие машины для бутылок
- •5.7.4.4. Специальные машины для укладки и сортировки упаковочных единиц
- •5.7.5. Формирование
- •5.7.5.2. Конструкция и принцип действия пакетосборщиков и пакеторазборщиков
- •5.7.5.3. Штабелирование
- •5.7.5.4. Транспортные средства для механизации погрузочно- разгрузочных работ
- •5.7.5.5. Складирование поддонов
- •5.7.5.6. Устройства для подачи и отвода пакетов- поддонов
- •5.8. Комплектная линия розлива
- •5.9. Потери пива
- •5.9.1. Расчет объема товарного пива
- •5.9.2. Снятие остатков и пересчет на товарное пиво
- •5.9.3. Расчет потерь по жидкой фазе
- •5.9.4. Расчет расхода солода в кг на гл пива
- •5.9.5. Оценка потерь и возможности их снижения
- •6. Мойка и дезинфекция
- •6.1. Материалы, используемые для изготовления емкостей и трубопроводов, и их устойчивость по отношению к моющим средствам
- •6.1.1. Емкости из алюминия
- •6.1.2. Емкости и трубопроводы из нержавеющей стали
- •6.1.3. Шланги и уплотнения
- •6.2. Моющие средства
- •6.3. Дезинфицирующие средства
- •6.4. Проведение мойки и дезинфекции в системе cip
- •6.5. Процесс мойки
- •6.6. Механическая мойка
- •6.7. Контроль мойки и дезинфекции
- •6.8. Меры безопасности при проведении мойки и дезинфекции
- •7. Готовое пиво
- •7.1. Химический состав пива
- •7.1.1. Компоненты пива
- •7.1.2. Пиво и здоровье
- •7.2. Органолептические показатели пива
- •7.2.1. Аромат и вкус пива
- •7.2.1.1. Аромат пива
- •7.2.1.2. Полнота вкуса
- •7.2.1.3. Игристость
- •7.2.1.4. Горечь пива
- •7.2.2. Пенистость и
- •7.3. Типы пива и их особенности
- •7.3.1. Пиво верхового брожения
- •7.3.1.1. Особенности
- •7.3.1.2. Пшеничное пиво типа Вайцен
- •7.3.1.3. «Белое» пиво типа Вайсе (Weipe)
- •7.3.1.4. «Старое» пиво типа Альт (Alt)
- •7.3.2. Типы и сорта пива низового брожения
- •7.3.2.1. Пиво типа Пилзнер (Pilsner)
- •7.3.2.3. Пиво типа «Export»
- •7.3.2.4. Пиво типа «Шварц» (Schwarzbiere, Черное пиво)
- •7.3.2.5. Пиво типа Фест (Festbiere, «Праздничное пиво»)
- •7.3.2.6. Пиво Айс (Eisbier, Ледяное пиво)
- •7.3.2.7. Пиво типа
- •7.3.2.8. Пиво типа Бок (Bockbier)
- •7.3.2.9. Пиво Двойной Бок (Doppelbock)
- •7.3.2.10. Безалкогольное пиво
- •7.3.2.11. Диетическое пиво
- •7.3.2.14. Типы пива,
- •7.3.2.15. Смешанные
- •7.3.3. Тенденции развития типов пива, приготовляемых без учета немецкого Закона о чистоте пивоварения
- •7.4. Контроль качества
- •7.4.1. Дегустация пива
- •7.4.2. Микробиологическое исследование
- •7.4.3. Анализ пива
- •7.4.3.2. Определение цветности пива
- •7.4.3.3. Определение величины рН
- •7.4.3.4. Определение содержания кислорода в пиве
- •7.4.3.5. Определение содержания диацетила в пиве
- •7.4.3.6. Определение пеностойкости
- •7.4.3.7. Определение
- •7.4.3.8. Определение
- •7.4.3.9. Определение склонности
- •7.4.3.10. Прочие методы анализа
- •7.5. Лабораторное оборудование и измерительная техника
- •7.5.1. Приборы
- •7.5.2. Расходомеры
- •7.5.3. Измерительные преобразователи уровня
- •7.5.4. Измерительные преобразователи плотности
- •7.5.5. Измерительные преобразователи мутности
- •7.5.6. Приборы для измерения содержания кислорода
- •7.5.7. Измерение величины рН
- •7.5.8. Измерение электрической проводимости
- •7.5.9. Датчики сигнализации предельного уровня
- •7.5.10. Измерение давления
- •8. Малые пивоваренные производства
- •8.1. Барные
- •8.2. Производственный мини-пивзавод
- •8.3. Любительское пивоварение
- •25 Кг ячменя (с 15%-ной влажностью)
- •9. Утилизация отходов и охрана окружающей среды
- •9.1. Законодательство об охране окружающей среды
- •9.2. Сточные воды
- •9.2.1. Расходы
- •9.2.2. Основные понятия, имеющие отношение к сточным водам
- •9.2.3. Очистка сточных вод
- •9.2.3.2. Установки для анаэробной очистки сточных вод
- •9.2.3.3. Объемы и состав
- •9.2.3.4. Очистка стоков с использованием смесительных и распределительных бассейнов
- •9.3. Остатки материалов и отходы
- •9.3.1. Пивная и хмелевая дробина
- •9.3.2. Взвеси
- •9.3.3. Остаточные дрожжи
- •9.3.4. Кизельгуровый шлам
- •9.3.5. Этикетки
- •9.3.6. Бой стекла
- •9.3.7. Банки для пива
- •9.3.8. Небольшие по объемам отходы
- •9.4. Промышленные выбросы
- •9.4.1. Пыль и пылевые выбросы
- •9.4.2. Выбросы из варочного цеха
- •9.4.3. Выбросы продуктов сгорания
- •9.4.4. Шумы
- •10. Энергетическое хозяйство на пивоваренных и солодовенных предприятиях
- •10.1. Потребление энергии
- •10.2. Паровые котельные агрегаты
- •10.2.1. Виды топлива
- •10.2.2.1.Теплота
- •10.2.2.2. Влажный пар
- •10.2.2.3. Перегретый пар
- •10.2.2.4. Горячая вода
- •10.2.3. Паровой котел
- •10.2.3.1. Классификация паровых котлов
- •10.2.3.2. Типы конструкций паровых котлов
- •10.2.3.3. Трехходовой котел
- •10.2.3.4. Рекуперация энергии и повышение кпд
- •10.2.4. Паросиловые установки
- •10.2.5. Блочные
- •10.3. Холодильные установки
- •10.3.1. Хладагенты
- •10.3.1.1. Хладагенты
- •10.3.1.2. Хладоносители
- •10.3.2. Компрессионные холодильные установки
- •10.3.2.1. Принцип действия
- •10.3.2.1. Испарители
- •10.3.2.2. Компрессор
- •10.3.2.3. Конденсаторы
- •10.3.2.4. Регулирующий клапан
- •1, 2, 3, 4 — Впускной, выпускной, спускной и воздушный
- •10.3.2.5. Накопитель ледяной воды (рис. 10.19)
- •10.3.3. Абсорбционная холодильная установка
- •10.3.4. Охлаждение помещений и жидкостей
- •10.3.4.2. Современные
- •10.3.4.3. Охлаждение жидкостей
- •10.3.5. Рекомендации по повышению экономичности эксплуатации холодильной установки
- •10.4. Электроборудование
- •10.4.1. Получение
- •1 0.4.2. Коэффициент мощности cos φ
- •10.4.3. Преобразование (трансформация) электрического тока
- •1 0.4.4. Меры безопасности
- •10.4.5. Рекомендации по экономичному расходу электроэнергии
- •10.5. Насосы,
- •10.5.1. Насосы
- •10.5.1.1. Лопастные насосы
- •10.5.1.1.2. Вихревые насосы
- •10.5.1.2. Объемные насосы
- •10.5.1.2.1.1. Эксцентриковый винтовой насос
- •10.5.1.2.2. Объемные насосы
- •10.5.1.3. Расчет параметров насосов
- •1 0.5.1.4. Регулирование числа оборотов насосов
- •10.5.2. Вентиляторы
- •10.5.2.1. Осевые вентиляторы
- •10.5.2.2. Центробежные вентиляторы
- •10.5.3. Компрессорные установки для сжатого воздуха
- •10.5.3.1.4. Винтовые
- •10.5.3.1.5. Турбокомпрессоры
- •10.5.3.2. Осушители воздуха
- •10.5.3.4. Трубопроводы высокого давления
- •10.5.3.5. Воздушные фильтры
- •11. От автоматизации —
- •X. О. Мит (н. О. Mieth), г. Гамбург
- •11.1. История развития и технические предпосылки автоматизации пивоваренного производства — высокие технологии в повседневной жизни
- •11.1.1. Устойчивые к коррозии и совместимые с пищевыми продуктами материалы
- •11.1.2. Автоматическая мойка и дезинфекция cip (Cleaning In Place)
- •11.1.3. Оборудование, отвечающие требованиям автоматизации и безразборной мойки (cip)
- •11.1.4. Технология пивоварения, отвечающая задачам автоматизации
- •11.1.5. Системы
- •11.1.6. Интеграция технологического процесса — «ноу-хау»
- •11.1.7. Искусственный интеллект и киПиА
- •11.1.8. Роль пивовара в автоматизации пивоваренного производства
- •11.2. Обозначения и системный подход к проектированию систем автоматизации пивоварения в соответствии с общими нормативами обозначения технологических процессов
- •11.2.1. Введение в принципы обозначения процессов и аппаратов
- •11.2.1.1. Стандартизированные обозначения типовых аппаратов и основных операций
- •11.2.1.2. Символы для обозначения специальных аппаратов с учетом
- •11.2.1.3. Стандарты din по технологии производства, имеющие значение для автоматизации
- •11.2.1.4. Необходимость действий
- •11.2.2. Основы
- •11.2.2.1. Этап проектирования 1: базовая схема технологического процесса или «блок- схема»
- •11.2.2.2. Этап проектирования 2: принципиальная технологическая схема процесса
- •835 Рис. 11.3. Блок-схема технологического процесса: маршрут сусла
- •11.2.2.3. Этап проектирования 3: формулировка задания на киПиА в соответствии с принципиальной схемой технологического процесса
- •11.2.2.4. Этап проектирования 4: словесное описание процесса к технологической схеме
- •11.2.2.5. Этап проектирования 5: функциональная схема трубопроводов и арматуры
- •11.2.2.6. Этап проектирования 6: функциональный план в соответствии с din 40 719 и iec 848
- •11.3. КиПиА согласно din и в практике автоматизации пивоваренного предприятия
- •11.3.1. К вопросу
- •11.3.1.1. Последствия
- •11.3.1.2. Полезность
- •11.3.2. Основы аппаратного обеспечения (ао) автоматизации пивоваренного производства. Функции ао
- •11.3.2.1. Система управления производственным процессом
- •11.3.2.2.1.2. Входы двоичных сигналов от датчиков предельных значений.Технические особенности коммутирования
- •11.3.2.2.2. Аналоговые сигналы
- •11.3.2.2.3. Аналогово-цифровые гибридные схемы
- •11.4. Задачи и средства интеграции технологических процессов
- •11.4.1. Задачи, стоящие
- •11.4.1.1. Шаг проектирования 5.1: определение производительности оборудования и гибкости процесса при составлении плана производства
- •11.4.1.2. Подэтап проектирования 5.2: составление диаграммы занятости
- •11.4.1.3. Подэтап проектирования 5.3: составление функциональной схемы
- •11.4.1.4. Методы интеграции стандартизированных производственных линий в проекте автоматизации пивоваренного предприятия
- •11.4.1.4.2. Вся производственная линия «в одних руках»
- •11.4.2. Системы и компоненты трубопроводов, обеспечивающие несмешиваемость сред и отвечающие требованиям безразборной мойки cip
- •11.4.2.1. Трубное соединение
- •11.4.2.2. Измерительные
- •11.4.2.3. Исполнительные органы
- •11.4.2.3.3. Поворотные заслонки (типа «бабочка»)
- •11.4.2.4. Необходимость стандартизации систем трубопроводов в автоматизированных установках для пищевых продуктов
- •11.4.3. Концепции надежности разделения сред
- •11.4.3.1. Системы жесткой трубной обвязки с перекидными калачами
- •11.4.3.2. Системы жесткой
- •11.4.3.3. Системы жесткой трубной обвязки с двухседельными клапанами
- •Isbn 5-93913-006-2
3.2.1.3.4. Влияние концентрации затора на расщепление крахмала
В относительно жидких заторах в раствор переходит больше экстракта, однако более плот-
© 224
ные заторы защищают ферменты от слишком быстрой термической инактивации (благодаря защитному действию коллоидных частиц затора и растворенных веществ). Благодаря этому в более плотных заторах повышается количество сбраживаемых Сахаров и тем самым — конечная степень сбраживания.
Однако концентрация затора влияет на расщепление крахмала меньше, чем другие факторы.
3.2.1.3.5. Контроль расщепления крахмала
Обобщим еще раз сказанное до сих пор применительно к контролю расщепления крахмала:
■ При затирании крахмал должен быть без остатка расщеплен до нормальной реакции на йод.
■ Контроль расщепления крахмала осуществляют в конце затирания посредством йодной пробы. Поскольку окрашивание крахмала и высокомолекулярных декстринов йодом происходит только в холодном заторе, пробу затора охлаждают. При этом на фарфоровой или гипсовой пластинке смешивают холодную пробу затора с каплей раствора йода, причем не должно происходить изменения цвета желтоватого 0,02-н раствора йода.
■ Осахаривание контролируют еще раз в конце кипячения сусла (*доо-сахаривание»).
Если сусло еще дает окрашивание с йодом, то оно не полностью осахарено. В этом случае говорят о синей варке, в результате которой получается пиво с клейстерным помутнением, так как высокомолекулярные декстрины остались не растворенными. Такую синюю варку можно впоследствии подготовить к брожению только путем добавления солодовой вытяжки или первого сусла.
3.2.1.4. Расщепление β-глюкана
Известно, что стенки клеток ячменного зерна состоят из прочного переплетения белковых веществ, целлюлозы и гемицеллюлозы, пронизанного цепочками β-глюкана. Высокомолекулярный (i-глюкан при определенных
условиях склонен к гелеобразованию, а значит, к повышению вязкости пива и с ним — к затрудненному фильтрованию. Поэтому следует рассмотреть β-глюкан несколько подробнее.
Из вышеизложенного известно, что в ходе солодоращения высокомолекулярный β-глю-кан большей частью расщепляется. Для этого требуется:
переработка сортов ячменя с низким содер жанием β-глюкана;
солод с высоким содержанием эндо-β-глю- каназы (минимум 120 единиц эндо-β-глю- каназы/кг солода);
хорошее растворение содержимого зерна (выше 80% рыхлых зерен по фриабилли- метру).
В отличие от закрученных молекул крахмала (α-глюкан, см. раздел 1.1.4.1.1) молекулы β-глюкана не ветвятся и вытянуты. Многие из этих молекул связаны водородными мостиками, то есть они ассоциированы (ас-социаты). Из-за их нерегулярного внешнего вида они называются бахромчатыми мицеллами (рис. 3.27а, 1).
В этом виде они растворимы. Многие из этих бахромчатых мицелл связаны друг с другом в поперечном направлении (2) и частично — белком (3) в стенках клетки; особенно это характерно для еще не полностью растворенных частей зерна в солоде, например, кончиков зерна (4). Это состояние характерно также для начала затирания [122, 123, 124].
Во время клейстеризации структура зерен крахмала разрушается, и частично связанные в поперечном направлении бахромчатые мицеллы освобождаются. Эндо-β-глюканаза может расщепить эти сшитые бахромчатые мицеллы на β -глюкан (5), причем оптимальная для эндо-β-глюканазы температура составляет 45-50 °С. Благодаря удлиненной паузе при этой температуре, хорошо растворенному солоду и высокой активности эндо-β-глюкана-зы, большая часть β-глюкана переводится в растворенную форму, в связи с чем опасность гелеобразования уменьшается.
Как только температура повышается, термочувствительная эндо-β-глюканаза инакти-вируется и прекращает свое действие. Здесь действует термостабильная (до 70 °С) β-глю-кан-солюбилаза (6), высвобождая высокомолекулярные соединения β-глюкана из белка и нерастворенных кончиков зерен, но не расщеп-
225 ©
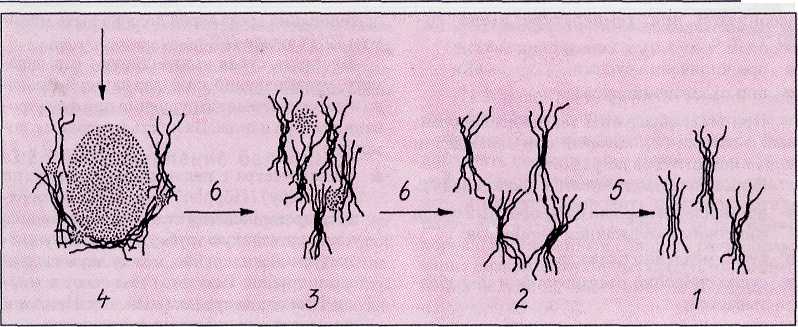
Рис. 3.27а. Расщепление β-глюкана при затирании:
1 — бахромчатые мицеллы; 2 — сшитые бахромчатые мицеллы; 3 — бахромчатые мицеллы, зафиксированные белком; 4 — нерастворенные области; 5 — расщепление эндо-β-глкжаназой; 6 — расщепление β-глюкан-солюбилазой
ляя их дальше. Так как эндо-β-глюканаза при этой температуре давно инактивировалась, всегда следует считаться с тем, что в плохо растворенном, бедном ферментами солоде содержатся высокомолекулярные соединения
β-глюкана, но не следует отождествлять эти соединения с гелем β-глюкана.
Проблема проявляется лишь после того, как произошло частичное разрушение водородных мостиков (рис. 3.27б, 1) внутри

Рис. 3.27б. Изменения в структуре и поведении β-глюкана в горячей среде и при охлаждении:
1 — разрушение водородных мостиков; 2 — термоактивированный β-глкжан; 3— касательные напряжения; 4 — отсутствие касательных напряжений
226
ассоциатов при температуре выше 70-80 °С, т. е.
при кипячении сусла и
при охлаждении сусла.
При этом образуется термоактивированный 3-глюкан (2), который при охлаждении может повести себя по-разному.
Если при проведении этих процессов (4):
применяется хорошо растворенный солод с высоким содержанием ферментов;
сусло медленно охлаждается;
сусло спокойно отстаивается и не взбал тывается;
исключается возникновение касательных напряжений,
то водородные мостики в молекуле не появляются и опасность образования геля невелика.
Но если при обработке сусла (3):
■ возникают большие касательные напря жения в области высоких температур сус ла, например:
из-за высоких скоростей течения и многократного изменения направле ния потока в выносном кипятильнике;
из-за возникновения в насосах силь ных вихревых явлений;
из-за возникновения сильных вихре вых явлений в вирпуле;
из-за слишком узких или часто изме няющихся поперечных сечений трубо проводов;
из-за центробежных сил в сепараторе,
то водородные мостики глюкановых нитей сшиваются и путем вытягивания молекул может начаться образование геля, а с ним — повышение вязкости и затруднения при фильтровании пива.
Существенными контрольными признаками, по которым можно предположительно выявить низкие значения высокомолекулярного β -глюкана, являются показания фриа-биллиметра, метод окрашивания среза зерна по Карлсбергу (см. раздел 2.8.2.10) и вязкость лабораторного сусла. У двух первых показателей существует высокая корреляция с содержанием β-глюкана сусла, а у последнего—с фильтруемостью пива. Необходимый показатель фриабиллиметра — рыхлых зерен свыше 80%. Однородность солода по методу
окрашивания среза зерна должна быть минимум 70% (лучше 75%).
Вязкость сусла контролируют как параметр, указывающий на содержание β-глюкана и на ожидаемые затруднения при фильтровании затора и пива. Вязкость измеряют с помощью
■ вискозиметра с падающим шариком (по Хопплеру) (Hoppler) (рис. 3.28). Измеря ется время падения стандартного шарика через стеклянную трубку, наполненную ис пытуемой жидкостью, между двумя штри хами трубки. Результат получают в мил- ли-Паскаль-секундах (мПас· с). При этом нормативные значения составляют:
|у конгрессного сусла (в пересчете на 8,6%) 1,51-1,63 мПас·с; у готового сусла (в пересчете на 12%) 1,73-2,20 мПас·с; у светлого пива (в пересчете на 12%) 1,78-1,95 мПас • с; или с помощью
Рис. 3.28. Вискозиметр с падающим шариком по Хопплеру

■ капиллярного вискозиметра Уббелоде (Ubbelohde), который применим и для автоматических измерений. (В отечествен-
ном пивоварении вязкость принято измерять с помощью вискозиметра Оствальда, представляющего собой U-образную трубку с расширениями и узким капиллярным коленом. — Прим. ред.)
