
- •Глава 11 написана г. О. Митом, г. Гамбург
- •Сырье 37
- •Визуальное и ручное обследование 180
- •2.10. Техника безопасности в солодовенном предприятии (цехе) 192
- •Кипячение сусла 312
- •3 .9.3. Аэрация сусла 347
- •Управление и контроль за технологическими процессами производства сусла 351
- •Техника безопасности при производстве сусла 353
- •4.2. Разведение чистой культуры дрожжей 380
- •Комплектная линия розлива 656
- •6.1. Материалы, используемые для изготовления емкостей и трубопроводов, и их устойчивость по отношению
- •Проведение мойки и дезинфекции в системе cip 685
- •11. От автоматизации - к интеграции технологических
- •11.2. Обозначения и системный подход к проектированию систем автоматизации пивоварения в соответствии с общими
- •11.3. КиПиА согласно din и в практике автоматизации
- •25 Балтика
- •0. Пиво — древнейший народный напиток
- •1. Сырье
- •1.1. Ячмень
- •1.1.1. Группы и сорта ячменя
- •1.1.1.1. Группы ячменя
- •1.1.1.2. Сорта ячменя
- •1.1.2. Возделывание ячменя
- •1.1.3. Строение
- •1.1.3.1. Наружное строение
- •1.1.3.2. Внутреннее строение
- •1.1.4. Состав и свойства отдельных частей ячменя
- •1.1.4.1.2. Сахар
- •1.1.4.1. Углеводы
- •1.1.4.2. Белковые вещества
- •1.1.4.2.2. Продукты
- •1.1.4.3. Жиры (липиды)
- •1.1.4.4. Минеральные вещества
- •1.1.4.5. Прочие вещества
- •1.1.5. Оценка качества ячменя
- •1.1.5.1. Визуальное и ручное обследование
- •1.1.5.2. Технохимический анализ
- •1.1.5.2.2. Масса 1000 зерен
- •1.1.5.2.3. Масса гектолитра
- •1.1.5.2.4. Проба на срез
- •1.1.5.2.5. Технохимический анализ
- •1.1.5.3. Физиологические исследования
- •1.1.5.3.1. Прорастаемость
- •1.1.5.3.2. Энергия и способность прорастания
- •1 .2. Хмель
- •1.2.1. Области возделывания хмеля
- •1.2.2. Сбор, сушка и предохранение хмеля от порчи
- •1.2.2.1. Сбор хмеля
- •1.2.2.2. Сушка хмеля
- •1.2.2.3. Стабилизирующая обработка
- •1.2.3. Строение хмелевой шишки
- •1.2.4. Состав и свойства компонентов хмеля
- •1.2.4.1. Горькие вещества или хмелевые смолы
- •1.2.4.2. Хмелевое эфирное масло
- •1.2.4.3. Дубильные вещества (полифенолы)
- •1.2.4.4. Белковые вещества
- •1.2.5. Оценка качества хмеля
- •1.2.5.1. Ручная оценка качества хмеля в шишках
- •1.2.5.2. Содержание в хмеле горьких веществ
- •1.2.6. Сорта хмеля
- •1.2.7. Хмелепродукты
- •1.2.7.1. Гранулированный хмель
- •1.2.7.2. Экстракты хмеля
- •1.3. Вода
- •1.3.1. Круговорот воды
- •1.3.2. Потребление воды в пивоваренном производстве
- •1.3.3. Забор воды
- •1.3.3.1. Забор подземных вод
- •1.3.3.2. Забор поверхностных вод
- •1.3.3.3. Значение собственного водоснабженния
- •1.3.4. Требования к воде
- •1.3.4.1. Требования к питьевой воде
- •1.3.4.2. Требования к воде для пивоварения
- •1.3.5. Способы улучшения состава воды
- •1.3.5.1. Способы удаления взвешенных частиц
- •1.3.5.2. Удаление растворенных в воде веществ
- •1.3.5.3. Способы улучшения
- •1.3.5.3.1. Декарбонизация
- •1.3.5.4. Обеззараживание воды
- •1.3.5.4.1. Обеззараживание фильтрованием
- •1.3.5.4.2. Обеззараживание ультрафиолетом
- •1.3.5.4.3. Обеззараживание озоном
- •1.3.5.4.4. Обеззараживание
- •1.3.5.4.5. Обеззараживание двуокисью хлора
- •1.3.5.4.6. Обеззараживание ионами серебра
- •1.3.5.5. Способы деаэрации воды
- •1.4. Дрожжи
- •1.4.1. Строение и состав дрожжевой клетки
- •1.4.2. Обмен веществ дрожжевой клетки
- •1.4.3. Размножение и рост дрожжей
- •1.4.4. Характеристики
- •1.4.4.1. Морфологические признаки
- •1.4.4.2. Физиологические различия
- •1.4.4.3. Технологические различия при сбраживании
- •1.4.4.4. Систематическая классификация
- •1.5. Несоложеное сырье
- •1.5.1. Кукуруза
- •1.5.3. Ячмень
- •1.5.4. Сорго
- •1.5.5. Пшеница
- •1.5.6. Сахарный колер
- •1.5.7. Сахар
- •105 Балтика
- •2. Производство солода
- •2.1. Приемка, очистка, сортирование и транспортирование ячменя
- •2.1.1. Приемка ячменя
- •2.1.1.1. Приемка ячменя с рельсового или автомобильного транспорта
- •2.1.1.2. Приемка ячменя
- •2.1.2. Очистка
- •2.1.2.1. Предварительная очистка ячменя
- •2.1.2.2. Магнитные сепараторы
- •2.1.2.3. Камнеотборник
- •2.1.2.4. Обоечная машина
- •2.1.2.5. Триер
- •2.1.2.6. Сортирование ячменя
- •2.1.2.6.1. Основа
- •2.1.2.6.2. Сортировочный цилиндр
- •2.1.2.6.3. Планзихтер
- •2.1.3. Транспортирование ячменя и солода
- •2.1.3.1. Механические
- •2.1.3.1.1. Нория или элеватор
- •2.1.3.1.2. Шнековый транспортер
- •2.1.3.1.3. Скребковый цепной транспортер
- •2.1.3.1.4. Ленточный транспортер
- •2.1.3.2. Пневматические
- •2.1.3.2.1. Всасывающая
- •2.1.3.2.2. Нагнетательная
- •2.1.4.1. Циклоны
- •2.1.4.2. Пылеотделительный фильтр
- •2.1.4.2.1. Пылеотделительный фильтр старой конструкции
- •2.1.4.2.2. Пылеотделительный фильтр новой конструкции
- •2.1.4.2.2.1. Рукавный фильтр
- •2.1.4.2.2.2. Прочие
- •2.2. Сушка и хранение ячменя
- •2.2.1. Дыхание ячменя
- •2.2.2. Сушка ячменя
- •2.2.3. Охлаждение ячменя
- •2.2.4. Хранение ячменя
- •2.2.4.1. Хранение в силосах
- •2.2.4.2. Хранение на складах
- •2.2.4.3. Заражение вредителями
- •2.2.4.3.1. Насекомые-вредители
- •2.2.4.3.2. Плесени
- •2.3. Замачивание ячменя
- •2.3.1. Процессы, происходящие при замачивании
- •2.3.1.1. Водопоглощение
- •2.3.1.2. Снабжение кислородом
- •2.3.1.3. Очистка
- •2.3.2. Замочные чаны
- •2.3.3. Проведение замачивания
- •2.4. Проращивание ячменя
- •2.4.1. Процессы, происходящие при проращивании
- •2.4.1.1. Процессы роста
- •2.4.1.2. Образование ферментов
- •2.4.1.2.1. Ферменты,
- •2.4.1.2.2. Прочие группы ферментов
- •2.4.1.3. Превращения веществ при проращивании
- •2.4.1.3.1. Растворение и расщепление β-глюкана
- •2.4.1.3.2. Расщепление крахмала
- •2.4.1.3.3. Расщепление белковых веществ
- •2.4.1.3.4. Расщепление жиров (липидов)
- •2.4.1.3.5. Образование
- •2.4.1.3.6. Регуляторы прорастания
- •2.4.2. Способы проращивания
- •2.4.2.1. Токовая солодовня
- •2.4.2.2. Системы
- •2.4.2.2.1. Кондиционирование аэрационного воздуха
- •2.4.2.2.2. Солодовня барабанного типа
- •2.4.2.2.3. Солодовня ящичного типа
- •2.4.2.2.3.1. Прямоугольные
- •158 Рис. 2.52. Принцип работы башенной солодовни:
- •2.4.2.2.4. Системы с ежесуточным перемещением
- •2.4.2.3. Контроль
- •2.5. Сушка солода
- •2.5.1. Изменения, происходящие при сушке
- •2.5.1.1. Понижение влажности
- •2.5.1.2. Прерывание процессов прорастания и растворения
- •2.5.1.3. Образование красящих и ароматических веществ (реакции Майяра)
- •2.5.1.4. Образование дмс при сушке
- •2.5.1.5. Образование нитрозаминов
- •2.5.1.6. Инактивация ферментов
- •2.5.2. Устройство сушилок
- •2.5.2.1. Отопление и вентиляция сушилки
- •2.5.2.2. Двухъярусные сушилки (старая конструкция)
- •2.5.2.3. Сушилки
- •2.5.2.4. Высокопроизводительные сушилки с погрузочно-разгрузочными устройствами
- •2.5.2.5. Вертикальные сушилки
- •2.5.3. Процесс сушки
- •2.5.3.1. Производство светлого солода (пильзенского типа)
- •2.5.3.2. Производство темного солода (мюнхенского типа)
- •2.5.3.3. Выгрузка солода из сушилки
- •2.5.3.4. Контроль за процессом сушки
- •2.6. Обработка солода после сушки
- •2.6.1. Охлаждение
- •2.6.2. Очистка солода
- •2.6.3. Хранение солода
- •2.6.4. Полировка солода
- •2.7. Выход солода в производстве
- •2.8.2.5. Стекловидность
- •2.8.2.6. Рыхлость
- •2.8.2.7. Длина зародышевого листка
- •2.8.2.8. Всхожесть
- •2.8.2.9. Плотность
- •2.8.2.10. Метод окрашивания среза зерна (модификация Carlsberg)
- •2.8.3. Технохимический контроль
- •2.8.3.1. Влажность
- •2.8.3.2. Конгрессный способ затирания
- •2.8.4. Договор на поставку солода
- •2.9. Специальные типы солода и солод из прочих зерновых
- •2.9.1. Светлый солод пильзенского типа
- •2.9.2. Темный солод (мюнхенский тип)
- •2.9.3. Темный солод венского типа
- •2.9.4. Карамельный солод
- •2.9.5. Томленый солод
- •2.9.6. Жженый солод
- •2.9.7. Кислый солод
- •2.9.8. Солод короткого ращения
- •2.9.9. Пшеничный солод
- •2.9.10. Солод из прочих хлебных злаков
- •2.9.11. Солод из сорго
- •2.9.12. Красящее пиво
- •2.9.13. Применение
- •2.10. Техника безопасности в солодовенном предприятии (цехе)
- •3. Производство сусла
- •3.1. Дробление солода
- •3.1.1. Подработка солода
- •3.1.1.1. Удаление из солода пыли и камней
- •3.1.1.2. Взвешивание засыпи
- •3.1.1.2.1. Весы с опрокидывающимся ковшом
- •3.1.1.2.2. Весы с открывающимся днищем
- •3.1.2. Основы дробления
- •3.1.3. Сухое дробление
- •3.1.3.1. Шестивальцовые дробилки
- •206 Рис. 3.7. Шестивальцовая
- •3.1.3.2. Пятивальцовые дробилки
- •3.1.3.3. Четырехвальцовые дробилки
- •3.1.3.4. Двухвальцовые дробилки
- •3.1.3.5. Вальцы дробилки
- •3.1.3.6. Кондиционированное сухое дробление
- •3.1.3.7. Бункер для дробленых зернопродуктов
- •3.1.3.8. Молотковые дробилки
- •3.1.4. Мокрое дробление
- •Откачка замочной воды.
- •3.1.5. Замочное
- •3.1.6. Оценка качества помола
- •3.2. Затирание
- •3.2.1. Превращения веществ при затирании
- •3.2.1.1. Цель затирания
- •3.2.1.2. Свойства ферментов
- •3.2.1.3. Расщепление крахмала
- •3.2.1.3.1. Влияние температуры
- •3.2.1.3.2. Влияние длительности
- •3.2.1.3.3. Влияние величины рН
- •3.2.1.3.4. Влияние концентрации затора на расщепление крахмала
- •3.2.1.3.5. Контроль расщепления крахмала
- •3.2.1.4. Расщепление β-глюкана
- •3.2.1.5. Расщепление белковых веществ
- •3.2.1.6. Превращения жиров (липидов)
- •3.2.1.8. Биологическое подкисление
- •3.2.1.8.1. Добавление неорганических кислот
- •3 .2.1.9. Состав экстрактивных веществ сусла
- •3.2,1.10. Заключительные рекомендации по проведению затирания
- •3.2.2. Заторные аппараты
- •3.2.3. Начало затирания
- •3.2.3.1. Гидромодуль затора
- •3.2.3.2. Температура начала затирания
- •3.2.4. Способы затирания
- •3.2.4.1. Различные точки
- •3.2.4.2. Настойные способы
- •3.2.4.3. Отварочные способы затирания
- •3.2.4.3.1. Одноотварочные способы
- •3.2.4.3.2. Двухотварочные способы
- •3.2.4.3.3. Трехотварочные способы
- •3.2.4.2.4. Специальные способы затирания
- •3.2.4.3.5. Способы затирания
- •3.2.5. Продолжительность затирания
- •3.2.6. Контроль затирания
- •3.3. Фильтрование затора
- •3.3.1. Первое сусло
- •3.3.2. Последняя промывная вода
- •3.3.3. Фильтрационный чан
- •3.3.3.1. Фильтрчан старой конструкции (рис. 3.46)
- •3.3.3.2. Фильтрационные чаны новой конструкции (рис. 3.48 и 3.48а)
- •3.3.3.3. Последовательность операций при работе на фильтрчане
- •3.3.4. Фильтрование
- •3.3.4.1. Фильтр-пресс старой конструкции
- •3.3.4.2.2.Последовательность операций при работе на фильтр-прессе 2001 (рис. 3.61а)
- •2. Фильтрование
- •3. Первое сжатие
- •4. Промывка дробины
- •5. Последнее сжатие
- •3.3.4.2.3.Прочие современные фильтр-прессы
- •3.3.5. Дробина
- •3.3.5.1. Транспортирование дробины
- •3.3.5.2. Анализ дробины
- •3.3.6. Солодовый экстракт
- •3.4. Кипячение сусла
- •3.4.1. Процессы, происходящие при кипячении сусла
- •I растворение и превращение компонентов хмеля;
- •I выпаривание воды;
- •I стерилизация сусла;
- •3.4.1.3. Испарение воды
- •3.4.1.4. Стерилизация сусла
- •3.4.1.5. Разрушение всех ферментов
- •3.4.1.6. Повышение цветности сусла
- •3.4.1.7. Повышение кислотности сусла
- •3.4.1.8. Образование редуцирующих веществ (редуктонов)
- •3.4.1.9. Изменение содержания диметилсульфида во время и после кипячения сусла
- •3.4.1.10. Содержание цинка в сусле
- •3.4.1.11. Неохмеленное сусло
- •3.4.2. Устройство и обогрев сусловарочного котла
- •3.4.2.1. Сусловарочный котел с прямым обогревом
- •3.4.2.2. Сусловарочный котел с паровым обогревом
- •3.4.2.2.1. Температура
- •3.4.2.2.2. Оснащение сусловарочного котла с паровой рубашкой в виде двойного дна
- •3.4.2.2.3. Форма и материал
- •Описание котла (выборочно)
- •3.4.2.2.4. Кипячение с использованием горячей воды (гидрокипячение)
- •3.4.2.3. Сусловарочные котлы
- •3.4.2.3.1. Кипячение при низком избыточном давлении с выносным кипятильником
- •3.4.2.4. Высокотемпературное кипячение сусла
- •3.4.2.5.1. Конденсация
- •3.4.2.6. Потребление энергии при кипячении сусла
- •3 .4.2.7. Конденсат вторичного пара
- •3.4.2.8. Сборник сусла
- •3.4.3. Технология кипячения сусла
- •3.4.3.1. Кипячение сусла
- •3.4.3.2. Внесение хмеля
- •3.4.3.2.1. Расчет дозировки хмеля
- •3.4.3.2.2. Состав и момент внесения хмеля
- •3.4.3.2.3. Способы внесения хмеля
- •3.4.4. Контроль готового сусла
- •3.5. Выход экстракта в варочном цехе
- •3 .5.1. Расчет выхода экстракта в варочном цехе
- •3.5.1.1. Определение массовой доли сухих веществ
- •3.5.1.2. Определение объемно-массовой доли сухих веществ в сусле (содержание экстракта в 1 гл сусла)
- •3.5.1.3. Пересчет объема горячего охмеленного сусла на холодное сусло
- •3.5.1.4. Расчет массы экстракта, полученного в варочном цехе
- •3.5.1.5. Определение выхода
- •3.5.2. Факторы, оказывающие влияние на выход экстракта в варочном цехе
- •3.5.3. Пример расчета выхода экстракта в варочном цехе
- •3.6. Состав оборудования варочного цеха
- •3.6.1. Количество аппаратов и их размещение
- •3.6.2. Размеры аппаратов варочного цеха
- •3.6.3. Материал для
- •3.6.4. Производственная
- •3.6.5. Варочные агрегаты
- •3.6.5.1. Варочные агрегаты мини-пивзаводов ресторанного типа
- •3.6.5.2. Интегральный варочный агрегат
- •3.6.5.3. Экспериментальные и учебные варочные агрегаты
- •3.7. Перекачка горячего охмеленного сусла
- •3.8. Отделение взвесей горячего сусла
- •3.8.1. Холодильная тарелка
- •3.8.2. Отстойный чан
- •3.8.3. Вирпул
- •3.8.3.1. Принцип действия вирпула
- •3.8.3.2. Конструкция вирпула
- •3.8.3.3. Технология осветления сусла в вирпуле
- •3.8.4. Сепараторы
- •3.8.4.1. Принцип
- •3.8.4.3. Устройство и способ действия
- •3.8.4.3.1. Принцип работы тарельчатых барабанов
- •3.8.5. Получение сусла из белкового отстоя
- •3 .9. Охлаждение
- •3.9.1. Процессы при охлаждении
- •3.9.1.1. Охлаждение сусла
- •3.9.1.2. Оптимальное удаление образующихся взвесей холодного сусла
- •3.9.1.3. Аэрация сусла
- •3.9.1.4. Изменения экстрактивности сусла
- •3.9.2. Аппараты
- •3.9.2.1. Устройство пластинчатого теплообменника
- •I очень тонкие металлические пластины;
- •3.9.2.2. Принцип работы пластинчатого холодильника
- •3.9.2.3. Преимущества пластинчатого холодильника
- •3.9.3. Аэрация сусла
- •3.9.3.1. Устройства для аэрации сусла
- •3.9.3.2. Момент проведения аэрации дрожжей.
- •3.9.4. Аппараты для удаления взвесей холодного сусла
- •3.9.4.1. Кизельгуровый
- •3.9.4.2. Флотация
- •3.9.4.3. Сепарирование холодного сусла
- •3.9.5. Компоновка оборудования линии охлаждения сусла
- •3.10. Управление и контроль за технологическими процессами производства сусла
- •3.11. Техника безопасности при производстве сусла
- •3.11.1. Предупреждение несчастных случаев вблизи дробилки
- •3.11.2. Предупреждение несчастных случаев при работах в аппаратах варочного цеха
- •3.11.3. Предупреждение несчастных случаев при работе с сепараторами
- •4. Производство пива (брожение, созревание и фильтрование)
- •4.1. Превращения при брожении и созревании
- •4.1.1. Дрожжи
- •4.1.2. Метаболизм дрожжей
- •4.1.2.1. Сбраживание Сахаров
- •4.1.2.1.2. Получение энергии при брожении
- •4.1.2.2. Метаболизм азотистых веществ
- •4.1.2.5. Метаболизм минеральных веществ
- •4.1.3. Образование и расщепление побочных продуктов брожения
- •4.1.3.1. Диацетил (вицинальные дикетоны)
- •4.1.3.2. Альдегиды (карбонилы)
- •4.1.3.3. Высшие спирты
- •4.1.3.4. Эфиры
- •4.1.3.5. Сернистые соединения
- •4.1.3.6. Органические кислоты
- •4.1.4. Другие процессы и превращения
- •4.1.4.1. Изменения азотистого состава
- •4.1.4.2. Понижение рН
- •4.1.4.3. Изменение
- •4.1.4.4. Изменение цветности пива
- •4.1.4.5. Выделение горьких
- •4.1.4.6. Насыщенность пива со2.
- •4.1.4.7. Осветление и коллоидная стабилизация пива
- •4.1.5. Влияние на дрожжи различных факторов
- •4.1.6. Флокуляция дрожжей (хлопьеобразование)
- •4.2. Разведение чистой культуры дрожжей
- •4.2.1. Факторы,
- •4.2.2. Выделение пригодных дрожжевых клеток
- •4.2.3. Разведение чистой культуры в лаборатории
- •4.2.4. Разведение
- •4.2.4.1. Установки для
- •4.2.4.2. Ассимиляционный способ
- •4.2.4.3. Способ разведения
- •4.2.4.4. Выращивание дрожжей открытым способом
- •25 Л молодого пива для пересева;
- •4.3. Классическое брожение и созревание
- •4.3.1. Бродильные чаны и оснащение бродильного отделения
- •4.3.1.1. Бродильные чаны
- •4.3.1.2. Оснащение открытого бродильного отделения
- •Дрожжевое отделение, где хранятся дрожжи.
- •4.3.2. Выход экстракта в бродильном отделении
- •4.3.3. Главное брожение в открытых чанах
- •4.3.3.1. Внесение дрожжей
- •4.3.3.1.1. Перемешивание и аэрация дрожжей
- •4.3.3.2. Технология брожения в чане
- •4.3.3.2.1. Стадии брожения
- •4.3.3.2.2. Температура брожения
- •4.3.3.3. Степень сбраживания
- •4.3.3.4. Перекачка пива из бродильного отделения
- •4.3.4. Сбор дрожжей из чана
- •4.3.5. Процессы, протекающие при созревании пива в танках традиционной конструкции
- •4.3.5.1. Насыщение пива диоксидом углерода под избыточным давлением
- •4.3.5.2. Осветление пива
- •4.3.6. Устройство классического отделения дображивания
- •4.3.6.1. Устройство отделения дображивания
- •4.3.6.2. Лагерные танки (танки дображивания)
- •4.3.7. Дображивание в лагерных танках
- •4.3.7.1. Перекачка пива
- •4.3.8. Соединение лагерного танка с линией розлива
- •4.3.8.1. Установление соединения
- •4.3.8.2. Давление при опорожнении танка
- •4.3.9. Перекачка из танков
- •4.3.9.1. Смеситель
- •4.3.9.2. Регулятор давления (друкреглер)
- •4.3.9.3. Получение пива
- •4.3.9.4. Глубокое охлаждение пива
- •4.3.9.5. Фильтрационные остатки
- •4.4. Брожение и созревание в цилиндроконических танках (цкт)
- •4.4.1. Конструкция и установка
- •4.4.1.1. Изготовление, форма и материал цкт
- •4.4.1.2. Размер цкт
- •4.4.1.2.1. Высота сусла в цктб
- •4.4.1.3. Установка и
- •4.4.2. Оборудование цкт
- •4.4.2.1. Контрольные приборы, элементы для обслуживания танка и предохранительная арматура
- •4.4.2.1.1. Оборудование для наполнения и опорожнения цкт
- •4.4.2.1.2. Арматура, устанавливаемая на куполе танка
- •4.4.2.1.3. Контрольные приборы
- •4.4.2.2. Охлаждение цкт
- •4.4.2.2.1. Потребность в холоде
- •4.4.2.2.2. Варианты охлаждения
- •4.4.2.2.3. Теплопередача
- •4.4.2.2.5. Теплоизоляция
- •4.4.2.3. Автоматизация и управление охлаждением
- •I Измерение количества со2.
- •4.4.3. Брожение
- •4.4.3.1. Некоторые аспекты брожения и созревания в цкт
- •4.4.3.2. Холодное брожение — холодное созревание
- •4.4.3.3. Холодное брожение
- •4.4.3.4. Теплое брожение без давления — холодное созревание
- •4.4.3.5. Брожение под давлением
- •4.4.3.6. Холодное брожение — теплое созревание
- •4.4.3.7. Холодное главное брожение
- •4.4.3.8. Теплое главное брожение с нормальным или форсированным созреванием
- •4.4.4. Сбор дрожжей из цкт
- •4.4.4.1. Момент сбора дрожжей
- •4.4.4.2. Методы сбора дрожжей
- •4.4.4.3. Обработка и хранение семенных дрожжей
- •4.4.4.3.1. Аэрация семенных дрожжей
- •4.4.4.3.2. Температура хранения дрожжей
- •4.4.4.3.3 Способы хранения дрожжей
- •4.4.4.4. Контроль семенных дрожжей
- •4.4.5. Качество пива перед фильтрованием
- •4.4.6. Рекуперация пива из избыточных дрожжей (пиво из дрожжевого осадка)
- •4.4.6.1. Прессование дрожжей
- •4.4.6.2. Сепарация дрожжей
- •4.4.6.3. Мембранное фильтрование дрожжей
- •4.4.6.4. Обработка пива, рекуперированного из дрожжей
- •4.4.7. Мойка цкт
- •4.4.8. Рекуперация с02
- •4.4.9. Иммобилизованные дрожжи
- •4.5. Фильтрование пива
- •4.5.1. Виды фильтрования
- •4.5.1.1. Механизмы осаждения
- •4.5.1.2. Фильтрующие перегородки
- •4.5.1.3. Вспомогательные
- •1000Х). (Фото: Schenk Filterbau GmbH, г. Вальд-
- •4.5.2. Виды фильтров
- •4.5.2.1. Масс-фильтр
- •4.5.2.2. Намывные фильтры
- •4.5.2.2.1. Намывка фильтрующих слоев
- •4.5.2.2.1.3. Роль кислорода
- •4.5.2.2.1.4. Дозаторы
- •4.5.2.2.2 Намывной рамный фильтр-пресс
- •4.5.2.2.3. Намывной свечной (патронный) фильтр
- •4.5.2.2.4. Намывной дисковый фильтр (фильтр с горизонтальными ситами)
- •4.5.2.2.5. Технические проблемы при фильтровании
- •4.5.2.2.6. Переработка разбавленных фильтрационных остатков
- •4.5.2.2.7. Кизельгуровая фильтрационная установка
- •4.5.2.3. Пластинчатый фильтр-пресс
- •4.5.2.4. Мембранные фильтры
- •4.5.2.4.1. Фильтр с модульными элементами
- •4.5.2.4.2. Мембранный свечной фильтр
- •4.5.2.5. Фильтрационная
- •4.5.2.6. Тонкость фильтрования
- •4.5.2.7. Тангенциально-поточное (Cross-flow) фильтрование
- •4.6. Стабилизация пива
- •4.6.1. Биологическая стабилизация пива
- •4.6.1.1. Пастеризация
- •4.6.1.2. Пастеризация в потоке
- •4.6.1.2.1. Пластинчатый пастеризатор
- •4.6.1.2.2. Температура и длительность термической обработки
- •4.6.1.2.3. Влияние пастеризации в потоке на качество пива
- •4.6.1.3. Горячий розлив пива
- •4.6.1.4. Пастеризация в туннель ном пастеризаторе
- •4.6.1.5. Холодно-стерильный розлив пива
- •4.6.2. Коллоидная
- •4.6.2.1. Характер коллоидного помутнения
- •4.6.2.2. Улучшение коллоидной стойкости пива
- •4.6.2.3. Технологические пути улучшения коллоидной стойкости пива
- •4 .6.2.4. Использование стабилизирующих средств
- •4.6.2.4.1. Силикагели
- •4.6.2.4.2. Поливинилполипирролидон (пвпп)
- •4.6.3. Фильтрационная линия
- •4.6.4. Вкусовая стойкость пива
- •4.6.4.1. Карбонилы, вызывающие старение вкуса (карбонилы старения)
- •1Дёлер - 100%-ная концентрация качества!
- •4.6.4.3. Приемы, позволяющие исключить попадание кислорода на пути от лагерного танка до розлива
- •4.6.4.4. Приемы, позволяющие исключить отрицательное изменение вкуса после розлива
- •4.7. Карбонизация пива
- •4.8. Особые способы приготовления пива
- •4.8.1. Высокоплотное пивоварение
- •4.8.2. Изготовление ледяного пива (Eisbier)
- •4.8.3. Методы удаления спирта из пива
- •4.8.3.1. Мембранные методы
- •4.8.3.1.1, Обратный осмос
- •4.8.3.1.2. Диализ
- •4.8.3.2. Термические способы удаления спирта/ дистилляция
- •4.8.8.3. Подавление образования спирта
- •4.9. Техника безопасности в отделениях брожения, дображивания и фильтрования
- •4.9.1. Несчастные случаи из-за углекислоты брожения
- •4.9.2. Техника безопасности при работе с цкт
- •4.9.3. Техника безопасности при работе с кизельгуром
- •5.1.1.2. Изготовление стеклянных бутылок
- •5.1.1.3. Формы бутылок
- •5.1.1.4. Цвет бутылки
- •5.1.1.5. Обработка поверхности бутылки
- •5.1.1.6. Износ (скаффинг)
- •5.1.1.7. Дополнительная защитная обработка бутылок
- •5.1.1.8. Бутылки многоразового использования
- •5.1.1.9. Последовательность технологических операций при использовании стеклянных бутылок многоразового использования
- •5.1.2. Мойка бутылок многоразового использования
- •5.1.2.1. Факторы, влияющие на чистоту бутылок
- •5.1.2.2. Бутылкомоечные машины
- •5.1.2.2.1. Конструкции
- •5.1.2.2.2. Основные
- •5.1.2.3. Моющий щелочной раствор
- •5.1.2.3.1. Требования к моющему щелочному расвору
- •5 .1.2.3.2. Состав моющего
- •5.1.2.3.3. Поддержание
- •5.1.2.3.4. Подготовка моющего щелочного раствора
- •5.1.2.3.5. Расход воды
- •5 .1.2.4. Техническое
- •5.1.4. Наполнение бутылок
- •5.1.4.1. Основные принципы розлива
- •5.1.4.2. Принципиальные конструктивные решения разливочно-укупорочных блоков
- •5.1.4.3. Основные узлы разливочно-укупорочного блока
- •5.1.4.4. Конструкция
- •5.1.4.5. Способ вспрыска воды под высоким давлением
- •5.1.5. Укупоривание бутылок
- •5.1.5.1. Укупоривание бутылок кронен-пробками
- •5.1.5.2. Укупоривание пробкой с пружинным хомутом
- •5.1.6. Промывка
- •5.1.7. Контроль наполненных и укупоренных бутылок
- •5.1.7.1. Контроль уровня наполнения
- •5.1.7.2. Кислород в горлышке бутылки
- •5.1.8. Пастеризация в бутылках
- •5.1.8.1. Обоснование пастеризации в бутылках
- •5.1.8.2. Важнейшие
- •5.1.8.3. Система обеспечения необходимого количества пе
- •5.1.9. Нанесение этикеток и фольги на бутылки
- •5.1.9.2. Этикеточный клей
- •5.1.9.3. Основной принцип нанесения этикеток
- •5.1.9.4. Конструктивные элементы этикетировочного автомата
- •5.1.9.5. Нанесение фольги на головку бутылки
- •5.1.10. Датирование
- •5.2. Особенности розлива в стеклянные одноразовые бутылки
- •5.2.1. Распаковка новых стеклянных бутылок
- •5.2.2. Ополаскивание
- •5.3. Розлив напитков в многоразовые пэт-бутылки
- •5.3.1. Пластиковые бутылки
- •5.3.1.2. Прочие виды
- •5.3.2. Изготовление пэт-бутылок
- •5.3.3. Транспортировка пустых пэт-бутылок
- •5.3.4. Мойка пэт-бутылок многоразового использования
- •5.3.5. Инспектирование
- •5.3.6. Процесс розлива в пэт-бутылки
- •5.3.7. Укупоривание пэт-бутылок
- •5.3.7.1. Алюминиевые колпачки
- •5.3.7.2. Пластмассовые
- •5.3.8. Этикетирование пэт-бутылок
- •5.4. Особенности наполнения одноразовых пэт-бутылок
- •5.5. Розлив пива в банки
- •5.5.1. Банки и их укупоривание
- •5.5.2. Складирование,
- •5.5.3. Инспектирование пустых банок
- •5.5.4. Ополаскивание банок
- •5.5.5. Наполнение банок
- •5.5.5.1. Разливочный автомат с дозированием по уровню
- •5.5.5.2. Разливочный автомат с дозированием по объему
- •5.5.6. Укупоривание банок
- •5.5.7. Мойка блоков розлива и укупоривания банок
- •5.5.8. Виджеты
- •5.5.9. Инспектирование полных банок
- •5.5.10. Пастеризация
- •5.5.11. Круговое
- •5.5.12. Датирование банок
- •5.6. Розлив в бочки, кеги, специальные бочонки и большие жестяные банки
- •5.6.2. Кеги и фитинги
- •5.6.3. Мойка и наполнение кегов
- •5.6.3.2. Наполнение кегов
- •5.6.4. Линия розлива в кеги
- •5.6.5. Розлив в малые
- •5.6.6. Розлив в большие банки
- •5.7. Упаковка
- •5.7.1. Транспортировка бутылок и банок
- •5.7.2. Обработка новых стеклянных бутылок и банок
- •5.7.3. Виды упаковки, транспортировка
- •5.7.3.1. Виды упаковки
- •5.7.3.2. Транспортировка единиц упаковки
- •5.7.3.4. Складирование ящиков
- •5.7.3.5. Мойка ящиков
- •5.7.4. Выемка и укладка
- •5.7.4.1. Захватные головки и захватные патроны
- •5.7.4.2. Виды укладчиков
- •5.7.4.2.1. Укладчик с прерывистым движением
- •5.7.4.2.2. Мультипакер
- •5.7.4.2.3. Круговой укладчик
- •5.7.4.3. Переориентирующие машины для бутылок
- •5.7.4.4. Специальные машины для укладки и сортировки упаковочных единиц
- •5.7.5. Формирование
- •5.7.5.2. Конструкция и принцип действия пакетосборщиков и пакеторазборщиков
- •5.7.5.3. Штабелирование
- •5.7.5.4. Транспортные средства для механизации погрузочно- разгрузочных работ
- •5.7.5.5. Складирование поддонов
- •5.7.5.6. Устройства для подачи и отвода пакетов- поддонов
- •5.8. Комплектная линия розлива
- •5.9. Потери пива
- •5.9.1. Расчет объема товарного пива
- •5.9.2. Снятие остатков и пересчет на товарное пиво
- •5.9.3. Расчет потерь по жидкой фазе
- •5.9.4. Расчет расхода солода в кг на гл пива
- •5.9.5. Оценка потерь и возможности их снижения
- •6. Мойка и дезинфекция
- •6.1. Материалы, используемые для изготовления емкостей и трубопроводов, и их устойчивость по отношению к моющим средствам
- •6.1.1. Емкости из алюминия
- •6.1.2. Емкости и трубопроводы из нержавеющей стали
- •6.1.3. Шланги и уплотнения
- •6.2. Моющие средства
- •6.3. Дезинфицирующие средства
- •6.4. Проведение мойки и дезинфекции в системе cip
- •6.5. Процесс мойки
- •6.6. Механическая мойка
- •6.7. Контроль мойки и дезинфекции
- •6.8. Меры безопасности при проведении мойки и дезинфекции
- •7. Готовое пиво
- •7.1. Химический состав пива
- •7.1.1. Компоненты пива
- •7.1.2. Пиво и здоровье
- •7.2. Органолептические показатели пива
- •7.2.1. Аромат и вкус пива
- •7.2.1.1. Аромат пива
- •7.2.1.2. Полнота вкуса
- •7.2.1.3. Игристость
- •7.2.1.4. Горечь пива
- •7.2.2. Пенистость и
- •7.3. Типы пива и их особенности
- •7.3.1. Пиво верхового брожения
- •7.3.1.1. Особенности
- •7.3.1.2. Пшеничное пиво типа Вайцен
- •7.3.1.3. «Белое» пиво типа Вайсе (Weipe)
- •7.3.1.4. «Старое» пиво типа Альт (Alt)
- •7.3.2. Типы и сорта пива низового брожения
- •7.3.2.1. Пиво типа Пилзнер (Pilsner)
- •7.3.2.3. Пиво типа «Export»
- •7.3.2.4. Пиво типа «Шварц» (Schwarzbiere, Черное пиво)
- •7.3.2.5. Пиво типа Фест (Festbiere, «Праздничное пиво»)
- •7.3.2.6. Пиво Айс (Eisbier, Ледяное пиво)
- •7.3.2.7. Пиво типа
- •7.3.2.8. Пиво типа Бок (Bockbier)
- •7.3.2.9. Пиво Двойной Бок (Doppelbock)
- •7.3.2.10. Безалкогольное пиво
- •7.3.2.11. Диетическое пиво
- •7.3.2.14. Типы пива,
- •7.3.2.15. Смешанные
- •7.3.3. Тенденции развития типов пива, приготовляемых без учета немецкого Закона о чистоте пивоварения
- •7.4. Контроль качества
- •7.4.1. Дегустация пива
- •7.4.2. Микробиологическое исследование
- •7.4.3. Анализ пива
- •7.4.3.2. Определение цветности пива
- •7.4.3.3. Определение величины рН
- •7.4.3.4. Определение содержания кислорода в пиве
- •7.4.3.5. Определение содержания диацетила в пиве
- •7.4.3.6. Определение пеностойкости
- •7.4.3.7. Определение
- •7.4.3.8. Определение
- •7.4.3.9. Определение склонности
- •7.4.3.10. Прочие методы анализа
- •7.5. Лабораторное оборудование и измерительная техника
- •7.5.1. Приборы
- •7.5.2. Расходомеры
- •7.5.3. Измерительные преобразователи уровня
- •7.5.4. Измерительные преобразователи плотности
- •7.5.5. Измерительные преобразователи мутности
- •7.5.6. Приборы для измерения содержания кислорода
- •7.5.7. Измерение величины рН
- •7.5.8. Измерение электрической проводимости
- •7.5.9. Датчики сигнализации предельного уровня
- •7.5.10. Измерение давления
- •8. Малые пивоваренные производства
- •8.1. Барные
- •8.2. Производственный мини-пивзавод
- •8.3. Любительское пивоварение
- •25 Кг ячменя (с 15%-ной влажностью)
- •9. Утилизация отходов и охрана окружающей среды
- •9.1. Законодательство об охране окружающей среды
- •9.2. Сточные воды
- •9.2.1. Расходы
- •9.2.2. Основные понятия, имеющие отношение к сточным водам
- •9.2.3. Очистка сточных вод
- •9.2.3.2. Установки для анаэробной очистки сточных вод
- •9.2.3.3. Объемы и состав
- •9.2.3.4. Очистка стоков с использованием смесительных и распределительных бассейнов
- •9.3. Остатки материалов и отходы
- •9.3.1. Пивная и хмелевая дробина
- •9.3.2. Взвеси
- •9.3.3. Остаточные дрожжи
- •9.3.4. Кизельгуровый шлам
- •9.3.5. Этикетки
- •9.3.6. Бой стекла
- •9.3.7. Банки для пива
- •9.3.8. Небольшие по объемам отходы
- •9.4. Промышленные выбросы
- •9.4.1. Пыль и пылевые выбросы
- •9.4.2. Выбросы из варочного цеха
- •9.4.3. Выбросы продуктов сгорания
- •9.4.4. Шумы
- •10. Энергетическое хозяйство на пивоваренных и солодовенных предприятиях
- •10.1. Потребление энергии
- •10.2. Паровые котельные агрегаты
- •10.2.1. Виды топлива
- •10.2.2.1.Теплота
- •10.2.2.2. Влажный пар
- •10.2.2.3. Перегретый пар
- •10.2.2.4. Горячая вода
- •10.2.3. Паровой котел
- •10.2.3.1. Классификация паровых котлов
- •10.2.3.2. Типы конструкций паровых котлов
- •10.2.3.3. Трехходовой котел
- •10.2.3.4. Рекуперация энергии и повышение кпд
- •10.2.4. Паросиловые установки
- •10.2.5. Блочные
- •10.3. Холодильные установки
- •10.3.1. Хладагенты
- •10.3.1.1. Хладагенты
- •10.3.1.2. Хладоносители
- •10.3.2. Компрессионные холодильные установки
- •10.3.2.1. Принцип действия
- •10.3.2.1. Испарители
- •10.3.2.2. Компрессор
- •10.3.2.3. Конденсаторы
- •10.3.2.4. Регулирующий клапан
- •1, 2, 3, 4 — Впускной, выпускной, спускной и воздушный
- •10.3.2.5. Накопитель ледяной воды (рис. 10.19)
- •10.3.3. Абсорбционная холодильная установка
- •10.3.4. Охлаждение помещений и жидкостей
- •10.3.4.2. Современные
- •10.3.4.3. Охлаждение жидкостей
- •10.3.5. Рекомендации по повышению экономичности эксплуатации холодильной установки
- •10.4. Электроборудование
- •10.4.1. Получение
- •1 0.4.2. Коэффициент мощности cos φ
- •10.4.3. Преобразование (трансформация) электрического тока
- •1 0.4.4. Меры безопасности
- •10.4.5. Рекомендации по экономичному расходу электроэнергии
- •10.5. Насосы,
- •10.5.1. Насосы
- •10.5.1.1. Лопастные насосы
- •10.5.1.1.2. Вихревые насосы
- •10.5.1.2. Объемные насосы
- •10.5.1.2.1.1. Эксцентриковый винтовой насос
- •10.5.1.2.2. Объемные насосы
- •10.5.1.3. Расчет параметров насосов
- •1 0.5.1.4. Регулирование числа оборотов насосов
- •10.5.2. Вентиляторы
- •10.5.2.1. Осевые вентиляторы
- •10.5.2.2. Центробежные вентиляторы
- •10.5.3. Компрессорные установки для сжатого воздуха
- •10.5.3.1.4. Винтовые
- •10.5.3.1.5. Турбокомпрессоры
- •10.5.3.2. Осушители воздуха
- •10.5.3.4. Трубопроводы высокого давления
- •10.5.3.5. Воздушные фильтры
- •11. От автоматизации —
- •X. О. Мит (н. О. Mieth), г. Гамбург
- •11.1. История развития и технические предпосылки автоматизации пивоваренного производства — высокие технологии в повседневной жизни
- •11.1.1. Устойчивые к коррозии и совместимые с пищевыми продуктами материалы
- •11.1.2. Автоматическая мойка и дезинфекция cip (Cleaning In Place)
- •11.1.3. Оборудование, отвечающие требованиям автоматизации и безразборной мойки (cip)
- •11.1.4. Технология пивоварения, отвечающая задачам автоматизации
- •11.1.5. Системы
- •11.1.6. Интеграция технологического процесса — «ноу-хау»
- •11.1.7. Искусственный интеллект и киПиА
- •11.1.8. Роль пивовара в автоматизации пивоваренного производства
- •11.2. Обозначения и системный подход к проектированию систем автоматизации пивоварения в соответствии с общими нормативами обозначения технологических процессов
- •11.2.1. Введение в принципы обозначения процессов и аппаратов
- •11.2.1.1. Стандартизированные обозначения типовых аппаратов и основных операций
- •11.2.1.2. Символы для обозначения специальных аппаратов с учетом
- •11.2.1.3. Стандарты din по технологии производства, имеющие значение для автоматизации
- •11.2.1.4. Необходимость действий
- •11.2.2. Основы
- •11.2.2.1. Этап проектирования 1: базовая схема технологического процесса или «блок- схема»
- •11.2.2.2. Этап проектирования 2: принципиальная технологическая схема процесса
- •835 Рис. 11.3. Блок-схема технологического процесса: маршрут сусла
- •11.2.2.3. Этап проектирования 3: формулировка задания на киПиА в соответствии с принципиальной схемой технологического процесса
- •11.2.2.4. Этап проектирования 4: словесное описание процесса к технологической схеме
- •11.2.2.5. Этап проектирования 5: функциональная схема трубопроводов и арматуры
- •11.2.2.6. Этап проектирования 6: функциональный план в соответствии с din 40 719 и iec 848
- •11.3. КиПиА согласно din и в практике автоматизации пивоваренного предприятия
- •11.3.1. К вопросу
- •11.3.1.1. Последствия
- •11.3.1.2. Полезность
- •11.3.2. Основы аппаратного обеспечения (ао) автоматизации пивоваренного производства. Функции ао
- •11.3.2.1. Система управления производственным процессом
- •11.3.2.2.1.2. Входы двоичных сигналов от датчиков предельных значений.Технические особенности коммутирования
- •11.3.2.2.2. Аналоговые сигналы
- •11.3.2.2.3. Аналогово-цифровые гибридные схемы
- •11.4. Задачи и средства интеграции технологических процессов
- •11.4.1. Задачи, стоящие
- •11.4.1.1. Шаг проектирования 5.1: определение производительности оборудования и гибкости процесса при составлении плана производства
- •11.4.1.2. Подэтап проектирования 5.2: составление диаграммы занятости
- •11.4.1.3. Подэтап проектирования 5.3: составление функциональной схемы
- •11.4.1.4. Методы интеграции стандартизированных производственных линий в проекте автоматизации пивоваренного предприятия
- •11.4.1.4.2. Вся производственная линия «в одних руках»
- •11.4.2. Системы и компоненты трубопроводов, обеспечивающие несмешиваемость сред и отвечающие требованиям безразборной мойки cip
- •11.4.2.1. Трубное соединение
- •11.4.2.2. Измерительные
- •11.4.2.3. Исполнительные органы
- •11.4.2.3.3. Поворотные заслонки (типа «бабочка»)
- •11.4.2.4. Необходимость стандартизации систем трубопроводов в автоматизированных установках для пищевых продуктов
- •11.4.3. Концепции надежности разделения сред
- •11.4.3.1. Системы жесткой трубной обвязки с перекидными калачами
- •11.4.3.2. Системы жесткой
- •11.4.3.3. Системы жесткой трубной обвязки с двухседельными клапанами
- •Isbn 5-93913-006-2
3.2. Затирание
Затирание — важнейший процесс при производстве сусла. При затирании помол и вода перемешиваются (затираются), компоненты солода переходят в раствор и становятся веществами экстракта.
При затирании решающее значение приобретает процесс превращения веществ.
3.2.1. Превращения веществ при затирании
3.2.1.1. Цель затирания
Большинство компонентов дробленого солода не растворимы сами по себе, а в пиво могут перейти только растворимые вещества. Поэтому при затирании необходимо перевести нерастворимые вещества помола в растворимые.
Все вещества, переходящие в раствор, называются экстрактом.
Р астворимыми веществами являются, например, сахара, декстрины, минеральные вещества и определенные белки. К нерастворимым веществам относятся крахмал, целлюлоза, часть высокомолекулярных белков и другие соединения, которые по окончании процесса фильтрования остаются в виде дробины.
По экономическим соображениям большинство нерастворимых соединений пытаются перевести в растворимые, чтобы получить как можно больше экстракта. Это выражается такими параметрами, как выход варочного цеха (см. разд. 3.5) и содержание экстракта в дробине (см. разд. 3.3.5.2).
Однако имеет значение не только количественное содержание, но и качество экстракта, так как присутствие определенных соединений (например, дубильных веществ из оболочек) весьма нежелательно, тогда как другие соединения (например, определенные сахара или продукты расщепления белков) совершенно необходимы.
Цель затирания состоит в том, чтобы расщепить крахмал в сахара и растворимые декстрины без остатка. При этом образуются и другие экстрактивные вещества. Основное количество экстракта образуется при затирании прежде всего благодаря действию ферментов, которые могут действовать при оптимальных для них температурах.
3.2.1.2. Свойства ферментов
Важнейшее свойство ферментов — их активность при расщеплении субстратов, которая зависит от различных факторов.
Зависимость активности ферментов от температуры
Активность ферментов возрастает с подъемом температуры и достигает оптимальной для каждого фермента величины при некоторой оптимальной температуре (рис. 3.22).
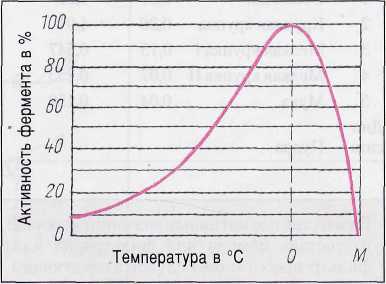
Рис. 3.22. Зависимость активности фермента от температуры:
О — оптимальная температура; М — максимальная температура
При более высоких температурах из-за раскрытия клубковых структур фермента (денатурации) происходит прогрессирующая инактивация. Эта инактивация и последующее исчезновение активности ферментов тем сильнее, чем значительнее превышение оптимальной температуры.
Уровень активности, характерный для фермента при определенной температуре, не оста-

 ется
неизменным. Если при более низких
температурах
активность со временем почти полностью
сохраняется, то при более высоких
температурах она быстро падает (рис.
3.23).
ется
неизменным. Если при более низких
температурах
активность со временем почти полностью
сохраняется, то при более высоких
температурах она быстро падает (рис.
3.23).
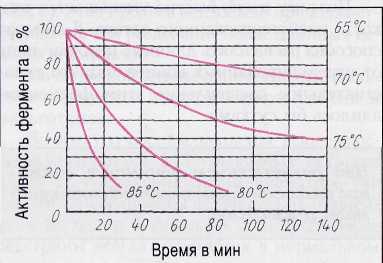
Рис. 3.23. Зависимость активности фермента от длительности термического воздействия
Зависимость активности ферментов от величины рН
Поскольку клубковая структура ферментов изменяется также в зависимости от величины рН, то существует и зависимость от нее активности ферментов. Эта активность достигает оптимальной величины при определенной, специфической для каждого фермента величине рН, и снижается при более низкой и более высокой величине рН (рис. 3.24). В общем, влияние рН на активность ферментов не так велико, как влияние температуры.
219 ©
Для пивоваренного производства среди многообразных процессов расщепления веществ имеют значение прежде всего следующие:
расщепление крахмала; расщепление (β-глюкана (гумми-веществ);
расщепление белковых веществ; превращение жирных кислот, а также ряд других процессов расщепления.
