- •1.Критерии аналитической надежности лабораторных исследований
- •6.Устройство, основные характеристики и правила настройки микроскопа. Основные микроскопические технологии.
- •7.Приготовление цитологического мазка, правила фиксации и окраски. Теория цитологических окрасок.
- •9.Основные этапы созревания гранулоцитов и моноцитов, опишите морфологические и цитохимические признаки клеток миелопоэза. Клиническое значение цитологического исследования клеток миелопоэза.
- •20.2.5.1. Фрагмент общей схемы
- •20.2.5.2. Антигеннезависимая дифференцировка
- •20.2.5.3. Антигензависимая дифференцировка
- •II. Проплазмоцит и плазмоцит
- •III. Активированные т-лимфоциты
- •14.Хронические миелопролиферативные заболевания. Патогенез, диагностика. Современные возможности лечения.
- •16.Острый миелолейкоз. Методы цитохимического анализа миелобластов.
- •18.Современные методы клинического исследования крови. Сравнительная характеристика и клиническое значение микроскопии мазка и исследования крови в гематологическом анализаторе.
- •20.Цитологические характеристики и клиническое значение исследования бластов в крови и препарате костного мозга.
- •25.Анемия хронических заболеваний. Этиология, патогенез, диагностика.
- •31.Стадии созревания мегакариоцитов, морфологические и иммунофенотипические характеристики. Структура и функция рецепторов тромбоцитов, роль арахидоновой кислоты, простациклин, тромбоксан.
- •33.Клиническое исследование мочи. Возможности визуальной колориметрии мочи в сравнении со стандартным клиническим исследованием.
- •3. Анализ мочи по Нечипоренко Процедура анализа :
- •4.1. Активированное парциальное (частичное) тромбопластиновое время (аптв)
- •4.2. Протромбиновое время
- •4.3. Тромбиновое время
- •51 . Ионометрия. Ионоселективные электроды. Кислотность среды и ее измерение. Индикаторы.
- •53.Нарушения обмена калия. Причины, методы диагностики. Гипокалиемия.
- •Диагностика
- •63.Диагностика сахарного диабета. Значение определения гликозилированного гемоглобина.
- •Лабораторные исследования : 1.Исследование уровня глюкозы в крови натощак Нормальным считается уровень глюкозы в пределах 3,5-5,5 ммоль/л.
- •6.Исследование гликированного гемоглобина
- •7.Исследование уровня фруктозамина в крови
- •8.Исследование липидов в крови
- •9.Исследование креатинина и мочевины
- •10 .Определение белка в моче
- •11.Исследование на кетоновые тела
- •Изменения фракции α2-глобулинов.
- •Изменения фракции β-глобулинов.
- •Изменения фракции γ-глобулинов.
- •Метод – колориметрический электрофорез Показания к назначению анализа - белковые фракции:
- •Лабораторная диагностика
- •2.Функциональная геномика
- •3.Сравнительная геномика
- •1.Обнаружение биомаркеров биологических процессов
- •2.Применения в медицине
- •3.Уточнение аннотации генома
- •4.Сравнительная протеомика
- •Основные методы Масс-спектрометрия
53.Нарушения обмена калия. Причины, методы диагностики. Гипокалиемия.
В клинической практике к гипокалиемии приводят следующие ситуации:
• потеря желудочно-кишечных жидкостей;
• длительное лечение осмотическими диуретиками или салуретиками (маннитол, мочевина, фуросемид), а также диабетическая глюкозурия;
• стрессовые состояния, сопровождающиеся повышенной адреналовой активностью, болезнь Иценко–Кушинга;
• уменьшение потребления калия в послеоперационном и посттравматическом пе- риодах в сочетании с задержкой натрия в организме (ятрогенная, т.е. вызванная медицинскими мероприятиями, гипокалиемия);
• продолжительный ацидоз или алкалоз, в результате которых нарушается функция почек и возникает калийурия;
• предшествующий дефицит калия, вызванный тяжелым хроническим заболеванием и усиленный послеоперационным периодом;
• длительное применение стероидных лекарственных препаратов;
• диллюционная гипокалиемия в фазе регидратации после острой или хронической дегидратации;
• хроническая почечная недостаточность;
• синдром Барттера;
• гиперальдостеронизм.
В основе всех приведенных причин гипокалиемии лежат четыре основных механизма: уменьшенное поступление калия в организм, усиленный переход калия из внеклеточной жидкости внутрь клетки, уменьшенный выход калия из клетки и увеличенная потеря калия. Основным механизмом гипокалиемии является повышенная потеря калия. Существует два главных пути потери калия – желудочно-кишечный тракт и почки. Кишечные и желчные свищи, а также обширные ожоги – это два второстепенных канала потерь калия. Наиболее массивные потери калия происходят при многократной рвоте (вот почему часто у больных с почечной недостаточностью нет гиперкалиемии), кишечной непроходимости, а также при всех заболеваниях, сопровождающихся диареей. Основными причинами усиленного перехода калия из внеклеточного пространства внутрь клетки является лечение инсулином или наличие инсулиномы, тиреотоксикоза, алкалоза. Гипокалиемия, связанная с алкалозом, обусловлена, во-первых, тем, что калий переходит из внеклеточной жидкости (плазмы) во внутриклеточную в обмен на ионы 206 водорода, для снижения рН крови; во-вторых, происходит усиленная экскреция калия с мочой, при этом калий теряется, а ионы водорода реабсорбируются для «борьбы» с алкалозом. Сниженное поступление калия в организм встречается у пациентов с несбалансированным питанием (алкоголики, пациенты с анорексией нервного происхождения), а также при длительном внутривенном введении бескалиевых растворов. Симптомы недостаточности калия у человека – тошнота, рвота, мышечная слабость (в том числе дыхательной мускулатуры – поверхностное дыхание), атония кишечника и мочевого пузыря, сердечная слабость. При концентрации калия в сыворотке крови ниже 3 ммоль/л на ЭКГ отмечаются изменения, свидетельствующие об ослаблении возбудимости и нарушении проводимости в сердечной мышце. В ряде случаев зависимости между уровнем калия в крови и возникновением таких серьезных последствий, как нарушение ритма сердца, не обнаруживается.
Гиперкалиемия
. К гиперкалиемии могут привести: • почечная недостаточность вследствие понижения экскреции калия почками; • острая дегидратация (обезвоживание); • обширные травмы, ожоги или крупные операции на фоне предшествующих тяжелых заболеваний; • тяжелый метаболический ацидоз и шок; • хроническая надпочечниковая недостаточность (гипоальдостеронизм); • быстрая инфузия концентрированного раствора калия, содержащего более 50 ммоль/л калия (приблизительно 0,4%-ный раствор хлорида калия); • олигурия или анурия любого происхождения; • диабетическая кома до начала инсулинотерапии; • развитие гиперкалиемии, возможное при приеме калийсберегающих диуретиков, например триамтерена (птерофена), спиронолактона (верошпирона). В основе приведенных причин гиперкалиемии лежат три основных механизма: усиленное поступление калия в организм, переход калия из внутриклеточного во внеклеточное пространство и сниженная его потеря. Усиленное поступление калия в организм обычно только способствует развитию гиперкалиемии. Наиболее часто это носит ятрогенный характер и встречается у пациентов, получающих внутривенные вливания растворов с высоким содержанием калия, и/или у пациентов с нарушениями функции почек. К этой группе причин относятся применение диеты с высоким содержанием калия, бесконтрольное применение калиевой соли пенициллина в больших дозах, переливание длительно хранившейся крови. Патогенетический механизм, связанный с усиленным переходом калия из внутриклеточного во внеклеточное пространство, имеет место при ацидозе, синдроме длительного сдавливания, тканевой гипоксии, недостатке инсулина и при передозировке препаратов дигиталиса. Потери калия уменьшаются при почечной недостаточности, гипоальдостеронизме, приеме диуретиков, блокирующих секрецию калия дистальными канальцами, и при первичных дефектах тубулярной секреции калия почками. Гепарин, даже в низких дозах используемый, для лечения и профилактики нарушений свертываемости крови, частично блокирует синтез альдостерона и может вызвать гиперкалиемию (вероятно, вследствие нарушения чувствительности канальцев к альдостерону).207 Особенно высокое содержание калия в сыворотке крови наблюдается при острой почечной недостаточности (ОПН), в частности, при некронефрозах, вызванных отравлениями и синдромом длительного сдавливания, что обусловливается резким снижением (практически до полного прекращения) ренальной экскреции калия, ацидозом, усиленным катаболизмом белка, гемолизом, при синдроме длительного сдавливания – повреждениями мышечной ткани. При этом содержание калия может достигать 7,0– 9,7 ммоль/л. Важное значение в клинической практике имеет динамика повышения калия в крови у больных с ОПН. В неосложненных случаях ОПН концентрация калия в плазме крови возрастает на 0,3–0,5 ммоль/л в сутки, после травмы или сложной операции – на 1– 2 ммоль/л в сутки, однако может наблюдаться и очень быстрый его подъем на 1–2 ммоль/л. Поэтому контроль за динамикой калиемии у больных с ОПН имеет большое значение и должен проводиться не реже 1 раза в сутки, а в осложненных случаях – чаще. Псевдогиперкалиемия (ложно повышенный уровень калия в сыворотке крови) может быть обусловлена гемолизом при взятии крови на анализ (наиболее часто вследствие наложения жгута более 1 мин.). Если кровь берут в стеклянную пробирку, что также способствует гемолизу, то такие изменения могут быть обнаружены в 20% взятых образцов крови. При лейкоцитозе (более 50,0·109 /л) и тромбоцитозе (1000·109 /л) также может наблюдаться псевдогиперкалиемия, вследствие высвобождения калия во время свертывания крови в пробирке. Гиперкалиемия клинически проявляется парестезиями, сердечными аритмиями. Угрожающими симптомами калиевой интоксикации являются коллапс, брадикардия, помрачение сознания. Изменения на ЭКГ наступают при концентрации калия выше 7 ммоль/л, а при увеличении концентрации его до 10 ммоль/л наступает внутрижелудочковая блокада с мерцанием желудочков, при концентрации 13 ммоль/л сердце останавливается в диастоле. По мере возрастания уровня калия в сыворотке постепенно меняется характер ЭКГ. Сначала появляются высокие заостренные зубцы Т. Затем развивается депрессия сегмента ST, атриовентрикулярная блокада 1-й степени и расширение комплекса QRS. Наконец, дальнейшее расширение комплекса QRS и слияние его с зубцом Т образуют двухфазную кривую, указывающую на приближающуюся асистолию желудочков. Скорость таких изменений непредсказуема, и от начальных изменений ЭКГ до опасных нарушений проводимости или аритмий иногда проходят считанные минуты.
54 . Центрифугирование. Принцип метода, основные определения, конструктивные особенности центрифуг. Препаративное и аналитическое центрифугирование. Аналитические ультрацентрифуги и их применение. С помощью центрифуги можно разделить жидкие смеси с компонентами разнойудельной плотности, так как при очень быстром вращении смеси расслаиваются и частицы разных компонентов в центробежном поле осаждаются с разной скоростью, которая зависит от их
размера и плотности.
Например, при центрифугировании крови в пробирке образуются несколько слоев: верхний желтый слой - плазма, нижний темный слой - клетки крови (эритроциты, лейкоциты и тромбоциты). При этом у границы жидкости можно заметить тонкий сероватый слой тромбоцитов.
Вещества, имеющие диагностическое значение, могут находиться в клетках крови или в плазме, некоторые химические элементы и вещества определяются и там, и там, поэтому разделение крови по фракциям позволяет провести точную диагностику.
Центрифугированию можно подвергнуть любые неоднородные жидкие среды, при этом оно подразделяется на препаративное и аналитическое.
Препаративное центрифугирование
Проводят с целью получения определенных компонентов из биологического материала для дальнейшего биохимического анализа. Такими компонентами могут быть клетки, их органеллы (митохондрии, рибосомы, ядра и др.) и макромолекулы (белки, ДНК и др.). Этот вид подготовки материала к дальнейшему исследованию применяют более часто, чем последующий.
Аналитическое центрифугирование
Проводят для выявления характеристик однородного материала, например, макромолекул. Материал центрифугируют, вследствие чего под контролем оптических систем происходит осаждение частиц. При этом можно определить их однородность, молекулярную массу, структуру, так как форма и масса частиц оказывают влияние на скорость осаждения. Проводя расчеты по стандартным формулам, можно вычислить эти параметры и составить характеристики исследуемого материала.
Центрифугирование. принцип метода, основные определения и формулы. Центрифугирование применяется для разделения неоднородных жидких сред. Центрифугирование позволяет разделить смесь, состоящую из двух или более компонентов с разной удельной плотностью, если по крайней мере один из этих компонентов — жидкость. Разделение веществ с помощью центрифугирования основано на разном поведении частиц в центробежном поле. В центробежном поле частицы, имеющие разную плотность, форму или размеры, осаждаются с разной скоростью. Скорость осаждения, или седиментации, зависит от центробежного ускорения (G), прямо пропорционального угловой скорости ротора (w,в рад/с) и расстоянию между частицей и осью вращения (г, в см) : G = v2 • г. Поскольку один оборот ротора составляет 2л радиан, угловую скорость ротора в оборотах в минуту (об. /мин) можно записать так: v = 2p/60 (об. /мин) , а центробежное ускорение тогда будет равно: G =4p2*r/3600 (об. /мин) 2. Центробежное ускорение обычно выражается в единицах g {гравитационная постоянная, равная 980 см*с-1) и называется относительным центробежным, ускорением (ОЦУ) , т. е. ОЦУ=4p2*r/3600*980 (об. /мин) 2 или ОЦУ = 1,11*10-5*r (об. /мин) 2 (*) На основании уравнения (*) Доулом и Котциасом была составлена номограмма, выражающая зависимость ОЦУ от скорости вращения ротора и радиуса г — среднего радиуса вращения столбика жидкости в центрифужной пробирке (т. е. расстояния от оси вращения до середины столбика жидкости) .
Центрифу́га — устройство, (машина или прибор) , служащее для разделения сыпучих тел или жидкостей различного удельного веса и отделения жидкостей от твердых тел путем использования центробежной силы. При вращении в центрифуге частицы с наибольшим удельным весом располагаются на периферии, а частицы с меньшим удельным весом — ближе к оси вращения.
Ультрацентрифуга Ультрацентрифуга с охлаждением серии Ultra – это оборудование для создания с помощью вращающегося ротора поля центробежных сил, значительно превосходящего поле земного тяготения (в сотни тысяч раз). Лабораторную ультрацентрифугу применяют для изучения седиментации, разделения частиц размером менее 100 нм (коллоидных систем, молекул белков, нуклеиновых кислот, синтетических полимеров). В специальных ультрацентрифугах ускорения превышают 106g.
Ультрацентрифуги серии Ultra могут применяться в научно-исследовательских центрах, лабораториях институтов и университетов. Ультрацентрифуги Hanil серии Ultra являются незаменимым оборудованием практически во всех медицинских учреждениях и центрах.
Аналитические ультрацентрифуги имеют оптическую систему, которая позволяет регистрировать на фотопленках результаты ультрацентрифугирования. В аналитических ультрацентрифугах производится также определение констант седиментации частиц, что позволяет затем рассчитывать их молекулярные веса. [c.125]
Еще одна область применения аналитического ультрацентрифугирования — исследование конформационных изменений макромолекул. Молекула ДНК, например, может быть одно- или двухцепочечной, линейной или кольцевой. Под действием различных соединений (таких, например, как органические растворители) или при повышенных температурах ДНК претерпевает ряд обратимых и необратимых конформационных изменений, которые можно установить по изменению скорости седиментации образца. Чем компактнее молекула, тем меньше ее коэффициент трения в растворе и наоборот чем менее она компактна, тем больше коэффициент трения и, следовательно, тем медленнее будет она седиментировать. Таким образом, различия в скорости седиментации образца до. и после различных воздействий на него позволяют обнаруживать конфор-мационные изменения, происходящие в макромолекулах. [c.63]
Индивидуальность полученных препаратов гликопротеинов контролируется чаще всего аналитическим ультрацентрифугированием (см., например, ), электрофорезом с подвижной границей или на носителях, хроматографией на ДЭАЭ-целлюлозе. Как и в случае полисахаридов, критерием однородности выделенного гликопротеина может служить неизменность его мономерного состава (моносахаридов и аминокислот) и физико-химических свойств при применении нескольких способов очистки. Для определения нативности выделенных веществ особое значение имеет контроль их биологической активности, в первую очередь иммунологических свойств.
55.Хроматографические методы разделения веществ, их применение в клинической диагностике Хроматография - это метод установления химического состава смеси, основанный на определенном распределении веществ, находящихся в разном агрегатном состоянии (газ, жидкость, твердые частицы) между двумя фазами (подвижной или неподвижной). К подвижной фазе относятся газы и жидкости, а к неподвижной - твердые вещества. В определенных условиях вещества в смеси начинают распределяться по фазам: газы перемещаются вверх, твердые частицы осаждаются, между ними скапливается слой жидкости, некоторые жидкости тоже могут расслаиваться. Вещества подвижной фазы перемещаются с различной скоростью, что тоже позволяет судить о составе смеси. Распределяясь в анализаторе по фазам, компоненты смеси образуют цветовой столб, при этом для каждого вещества существуют свои цветовые характеристики.
Основоположник метода - русский биолог М. С. Цвет, который, пропуская смеси красящих веществ растительного происхождения через бесцветное впитывающее вещество, обнаружил, что оно окрашивается слоями с различными цветовыми характеристиками. Такой цветовой столбик был назван хромограммой.
В настоящее время существуют множество видов хроматографии. Например, адсорбционная хроматография основана на использовании адсорбентов (твердых впитывающих веществ). Разные вещества впитываются адсорбентами по-разному, именно выявление этих особенностей и позволяет оценить качественный состав исследуемой смеси. Распределительная хроматография основана на разной растворимости веществ, находящихся в разной фазе.
Ионообменная хроматография основана на проникновении ионов подвижной фазы (исследуемой жидкости) в вещество неподвижной фазы, которое происходит за счет электростатического взаимодействия между ионами этих веществ. Способность твердых веществ выпадать в осадок позволяет проводить осадочную хроматографию.
Существует еще эксклюзионная хроматография, при которой распределение веществ обеспечивается за счет разной проницаемости молекул жидкой фазы в гель (неподвижную фазу).
56.Электрофоретические методы разделения биоматериалов. Примеры применения в клинической практике. Значение электрофореза в протеомном анализе. Биохимические анализы, основанные на принципе электрофореза, в медицинской практике используют очень широко, так как одновременно информативны и экономичны. Метод электрофореза, разработанный в 1937 г. шведским биохимиком А. Тиселиусом, позволяет разделять макромолекулы по фракциям и основан на свойствах макромолекул при растворении в воде приобретать электрический заряд. При воздействии на раствор электрического поля молекулы притягиваются к электроду с противоположным зарядом. Скорость перемещения молекул зависит от их размера и электрического заряда. Так, молекулы белка амфотерны, т. е. имеют положительный заряд на одном конце и отрицательный на другом, поэтому их скорость и направление перемещения зависят от среды (кислая или щелочная). На заряд белковых молекул в средах с одинаковой кислотностью влияют аминокислоты, входящие в их состав. При распаде белковой молекулы образуются цепи аминокислот с разным электрическим зарядом, которые под воздействием электрического поля притягиваются к противоположно заряженному электроду и таким образом разделяются. Гель - это смесь нескольких веществ, обладающая свойствами твердых тел (сохраняет форму), но очень пластичных (деформируется). Одно вещество при этом всегда состоит из крупных молекул, образующих сетку (каркас), заполненную молекулами малого размера второго вещества. Для упрощения разделения веществ электрофорез проводят на фильтровальной бумаге, целлюлозе, гелях и агарозе, в этом случае гели выступают в качестве ионного фильтра: мелкие ионы проникают в поры геля, а крупные - нет, что дает дополнительную информацию для исследования. Наиболее часто электрофорез применяют для разделения белков по фракциям (все белки крови подразделяются на альбумины и несколько видов глобулинов). При многих заболеваниях изменяется не только общее количество белка в крови, но и соотношение его различных фракций. Результаты таких исследований важны для диагностики заболеваний печени, почек, злокачественных опухолей, нарушений иммунитета, инфекционных заболеваний и наследственных болезней.
57.Лимфоплазмаклеточные дискразии. Клинические формы, диагностические критерии, методы лабораторной диагностики. Плазмоклеточные дискразии — это синдром (устойчивая совокупность симптомов), выражающийся накоплением в сыворотке крови и/или моче больных парапротеинов (однородных белков, выработанных плазматическими клетками, то есть зрелыми В-лимфоцитами – особым видом лейкоцитов (белых клеток крови)).
При плазмоклеточных дискразиях в костном мозге увеличивается количество одинаковых плазматических клеток.
Парапротеины могут повышать вязкость крови, способствовать развитию тромбозов (закрытия просвета сосудов) и кровотечений.
Основные симптомы плазмоклеточных дискразий объединены в один синдром (устойчивая совокупность симптомов, объединенных единым развитием). Это синдром белковой патологии, связанный с выработкой парапротеинов (однородных белков) плазматическими клетками (то есть зрелыми В-лимфоцитами – особым видом лейкоцитов (белых клеток крови)).
Симптомы.
Поражение почек за счет отложения в них парапротеина:
ложные позывы к мочеиспусканию;
частое мочеиспускание ночью при редком мочеиспускании днем;
уменьшение объема выделяемой мочи.
Параамилоидоз – отложение парапротеинов в различных органах, приводящее к нарушению их функций:
сердцебиение, перебои в работе сердца;
нарушение подвижности языка и увеличение его размера;
снижение подвижности суставов;
боли и неприятные ощущения в различных частях тела (связаны с повреждением нервов).
Формы
Плазмоклеточные дискразии подразделяются на несколько форм.
Злокачественные (то есть растущие с повреждением окружающих тканей) плазмоклеточные дискразии, клинически выраженные, прогресирующие плазмоклеточные дискразии, парапротеинемические гемобластозы. Встречаются в каждом четвертом случае плазмоклеточных дискразий.
Множественная миелома (злокачественное разрастание плазматических клеток, то есть зрелых В-лимфоцитов – особого вида лейкоцитов (белых клеток крови)).
Cолитарные плазмоцитомы (то есть единичные опухоли из плазматических клеток), которые бывают костные и внекостные (то есть располагающиеся внутри костей или вне их, например, в толще мышц или во внутренних органах).
Макроглобулинемия Вальденстрема (опухоль костного мозга, состоящая из лимфоцитов (особого варианта лейкоцитов) или лимфоцитов и плазматических клеток).
Ненаследственный первичный системный амилоидоз (нарушение белкового обмена, сопровождающееся образованием в тканях амилоида – специфического белково-полисахаридного комплекса).
Болезни тяжелых цепей (опухоли из зрелых лимфоцитов, производящих тяжелые цепи иммуноглобулинов – особый вид белков).
Дискразии неясного значения (их значение и влияние на прогноз неизвестны), бессимптомные, чаще всего непрогрессирующие. Связаны с:
опухолевыми заболеваниями (в особенности с раком (злокачественная опухоль, состоящая из клеток, покрывающих тело или выстилающих полые органы) толстой кишки, желчевыводящих путей, молочной железы);
хроническим воспалением и инфекциями (хронический холецистит – воспаление желчного пузыря, остеомиелит – воспаление костей, туберкулез – особый вид инфекции, вызванной микобактериями туберкулеза, пиелонефрит – воспаление лоханок почек, ревматоидный артрит – особый вид воспаления суставов);
различными другими патологическими (ненормальными) состояниями (болезни печени, тиреотоксикоз – усиление выработки гормонов (особых веществ, управляющих работой организма) щитовидной железы, дефицит витамина В12, семейная гиперхолестеринемия – передающееся по наследству нарушение обмена жироподобных веществ).
Данные три формы плазмоклеточных дискразий неясного значения обычно относят к « симптоматическим», или « доброкачественным» (то есть не укорачивающим продолжительность жизни пациента).
У внешне здоровых людей – « идиопатическая», или « эссенциальная» форма (то есть возникающая по неизвестной причине). Встречается у каждого сотого человека в возрасте до 25 лет и у каждого двадцать пятого человека в возрасте старше 70 лет. Самый частый вид плазмоклеточных дискразий.
Транзиторные (то есть периодически появляющиеся и исчезающие) плазмоклеточные дискразии (связаны с лекарственной аллергией, вирусными инфекциями, операциями на сердце). Встречаются примерно в каждом десятом случае плазмоклеточных дискразий.
Причины
Причины большинства плазмоклеточных дискразий до настоящего времени неизвестны. Иногда они возникают вследствие других заболеваний (например, опухолей кишечника, молочной железы, воспаления желчного пузыря, заболевания печени и др.).
Предрасполагающие факторы различны в зависимости от варианта плазмоклеточных дискразий, в большинстве случаев они также неизвестны.
Диагностика
Анализ анамнеза заболевания и жалоб (когда (как давно) появились нарушения мочеиспускания, боли в различных частях тела, нарушение подвижности суставов и другие симптомы, с чем пациент связывает их возникновение).
Анализ анамнеза жизни. Есть ли у пациента какие-либо хронические заболевания, отмечаются ли наследственные заболевания, имеет ли пациент вредные привычки, принимал ли длительно какие-нибудь препараты, выявлялись ли у него опухоли, контактировал ли он с токсическими (отравляющими) веществами.
Физикальный осмотр. Определяется цвет кожных покровов (возможна бледность). При пальпации (прощупывании) могут выявляться опухоли различных органов, в том числе мышц и костей. При перкуссии (простукивании) может выявляться увеличение печени и селезенки. Пульс может быть учащенным, артериальное давление — сниженным.
Анализ крови. Может определяться снижение количества эритроцитов (красных клеток крови, норма 4,0-5,5х109г/л), уменьшение уровня гемоглобина (особого соединения внутри эритроцитов, переносящего кислород, норма 130-160 г/л). Цветной показатель (отношение уровня гемоглобина, умноженного на 3, к первым трем цифрам количества эритроцитов) обычно остается нормальным: в норме этот показатель 0,86-1,05. Количество лейкоцитов (белых клеток крови, норма 4-9х109г/л) может быть нормальным или сниженным. Количество тромбоцитов (кровяных пластинок, склеивание которых обеспечивает свертывание крови) становится сниженным, реже – повышенным или нормальным (норма 150-400х109г/л). Скорость оседания эритроцитов (СОЭ, неспецифический лабораторный показатель, отражающий соотношение разновидностей белков крови) значительно повышается с самого начала заболевания.
Анализ мочи. В моче появляется белок. Может появляться кровь при развитии почечного кровотечения или кровотечения из мочевыводящих путей. Могут появляться бактерии и повышаться количество лейкоцитов при развитии инфекции почек или мочевыводящих путей.
Исследование мочи по Зимницкому – определение плотности мочи, собранной отдельными порциями за каждые три часа в течение суток. Позволяет оценить функцию почек.
Определение содержания белка в суточной моче. Позволяет оценить потери белка организмом за сутки.
Биохимический анализ крови. Определяется уровень холестерина (жироподобное вещество), глюкозы (простой углевод), креатинина (продукт распада белка), мочевой кислоты (продукт распада веществ из ядра клетки), электролитов (калий, натрий, кальций) для выявления сопутствующего поражения органов.
Определение общего количества белка и его состава при исследовании крови и суточной мочи методом электрофореза (разделения белков на составляющие при движении под воздействием электрического тока) выявляет повышение количества белка в крови и моче и значительное преобладание одной из его разновидностей.
Исследование костного мозга, полученного при помощи пункции (прокалывания с извлечением внутреннего содержимого) кости, чаще всего грудины (центральной кости передней поверхности грудной клетки, к которой крепятся ребра), позволяет оценить кроветворение и выявить характер его нарушений.
Трепанобиопсия (исследование костного мозга в его соотношении с окружающими тканями) выполняется при взятии на исследование столбика костного мозга с костью и надкостницей, обычно из крыла подвздошной кости (область таза человека, расположенная наиболее близко к коже) с помощью специального приборы – трепана. Наиболее точно характеризует состояние костного мозга.
Люмбальная пункция (взятие для исследования ликвора – спинномозговой жидкости) позволяет определить поражение нервной системы.
Ультразвуковое исследование внутренних органов оценивает размеры печени, селезенки, почек, их структуру на предмет поражения опухолевыми клетками и наличия кровоизлияний.
Рентгенография органов грудной клетки позволяет оценить состояние внутригрудных лимфоузлов, легких и сердца.
Спиральная компьютерная томография (СКТ) – метод, основанный на проведении серии рентгеновских снимков на разной глубине – позволяет получить точное изображение исследуемых органов и оценить распространенность опухолевого процесса.
Магнитно-резонансная томография (МРТ) – метод, основанный на выстраивании цепочек воды при воздействии на тело человека сильных магнитов – позволяет получить точное изображение исследуемых органов и оценить распространенность опухолевого процесса.
Биопсия (взятие небольшого кусочка для исследования) кожи, слизистой полости рта, прямой кишки, мышц выявляет отложение в них парапротеинов (однородных белков, выработанных плазматическими клетками – особым видом лейкоцитов – белых клеток крови).
Электрокардиография (ЭКГ). Определяется увеличение частоты сердечных сокращений, нарушение питания мышцы сердца, реже – нарушения ритма сердца.
Возможна также консультация терапевта.
Лечение плазмоклеточные дискразий
Лечение зависит от формы плазмоклеточной дискразии.
При эссенциальной (то есть причина которой неизвестна) плазмоклеточной дискразии лечение обычно не требуется.
Если плазмоклеточная дискразия развилась вследствие другого заболевания, то проводится лечение этого заболевания.
При злокачественной плазмоклеточной дискразии лечение проводится только врачом-гематологом по схемам, различным для каждого варианта опухоли крови.
Экстракорпоральные методы лечения (методы механической очистки крови вне организма при помощи специальных приборов), например, плазмаферез, гемосорбция, гемодиализ. Могут использоваться при значительном повышении уровня белка крови при любом варианте плазмоклеточных дискразий. Способствуют удалению из организма избытка белка, снижают риск возникновения кровотечений и почечной недостаточности, препятствуют развитию парапротеинемической комы (утрата сознания с отсутствием реакции на внешние раздражители при закрытии просвета сосудов мозга белком).
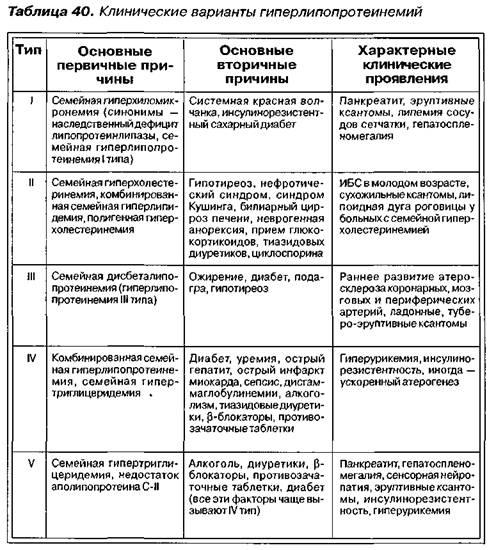
58.Диагностика и клиническое значение семейных и приобретенных гиперлипидемий. Гиперлипидемия (гиперлипопротеинемия, дислипидемия) — аномально повышенный уровень липидов и/илилипопротеинов в крови человека. Классификация :
|
Гиперлипопротеинемия |
Синонимы |
Этиология |
Выявляемое нарушение |
Лечение |
|
Тип I |
Первичная гиперлипопротеинемия, Наследственная гиперхиломикронемия |
Пониженная липопротеинлипаза(ЛПЛ) или нарушение активатора ЛПЛ - апоС2 |
Повышенныехиломикроны |
Диета |
|
Тип IIa |
Полигенная гиперхолестеринемия, Наследственная гиперхолестеринемия |
Недостаточность ЛПНП-рецептора |
Повышенные ЛПНП |
Статины,Никотиновая кислота |
|
Тип IIb |
Комбинированная гиперлипидемия |
Снижение ЛПНП-рецептора и повышенный апоВ |
Повышенные ЛПНП,ЛПОНП итриглицериды |
Статины,Никотиновая кислота,Гемфиброзил |
|
Тип III |
Наследственная дис-бета-липопротеинемия |
Дефект апоЕ (гомозиготы апоЕ 2/2) |
Повышенные ЛППП |
Преимущественно:Гемфиброзил |
|
Тип IV |
Эндогенная гиперлипемия |
Усиленное образование ЛПОНП и их замедленный распад |
ПовышенныеЛПОНП |
Преимущественно:Никотиновая кислота |
|
Тип V |
Наследственная гипертриглицеридемия |
Усиленное образование ЛПОНП и пониженная липопротеинлипаза |
ПовышенныеЛПОНП ихиломикроны |
Никотиновая кислота,Гемфиброзил |
Патоморфология • Атеросклероз • Панкреатит • Инфильтрация внутренних органов, костного мозга и кожи пенистыми клетками — макрофагами, содержащими большое количество липидов (хиломикронемический синдром).
Метаболизм липидов. Липиды, поступающие с пищей, транспортируются в жировую ткань в составе ЛПОНП и хиломикронов. Липопротеин липаза гидролизует эти липиды до жирных кислот. Свободные жирные кислоты проникают в адипоциты и запасаются в жировых капельках в виде триглицеридов (ТГ). Запасаемые ТГ гидролизуются гормон - чувствительной липазой, активируемой цАМФ. Далее свободные жирные кислоты поступают в просвет капилляров, где нековалентно связываются с альбуминами и транспортируются в печень.
Типы
гиперлипопротеинемий
• Приобретённая
(спорадическая) развивается как следствие
основной болезни (например, гипотиреоза)
• Семейная. Группа заболеваний,
характеризующихся изменением
концентрации b -
липопротеинов, пре - b -
липопротеинов и соответствующих липидов
(сюда же включены гиперлипидемии в
рамках общей классификации)