
- •2. Значения, которые принимают квантовые числа.
- •3. Обозначение состояния электрона в атоме.
- •4. Форма и знаки орбиталей.
- •5. Энергия электрона в многоэлектронном атоме.
- •1.2. Периодический закон и Периодическая система химических элементов д.И. Менделеева
- •1.2.1. Закономерности изменения свойств элементов и их соединений по периодам и группам
- •1.2.2. Общая характеристика металлов iа – iiiа групп в связи с их положением в Периодической системе химических элементов д.И. Менделеева и особенностями строения их атомов
- •1.2.3. Характеристика переходных металлов (меди, цинка, хрома, железа) по их положению в Периодической системе химических элементов д.И. Менделеева и особенностями строения их атомов
- •1.2.4. Общая характеристика неметаллов ivа – viiа групп в связи с их положением в Периодической системе химических элементов д.И. Менделеева и особенностями строения их атомов
- •Химические свойства.
- •1.3.1. Ковалентная химическая связь, ее разновидности и механизмы образования. Характеристики ковалентной связи (полярность и энергия связи. Ионная, металлическая и водородная связь.
- •Ионная связь
- •Металлическая связь
- •Водородная связь
- •Водородная связь в молекуле воды
- •Виды химической связи
- •1.3.2. Электроотрицательность. Степень окисления и валентность химических элементов.
- •1.3.3. Вещества молекулярного и немолекулярного строения. Тип кристаллической решетки. Зависимость свойств веществ от их состава и строения.
- •1.4. Химическая реакция.
- •1.4.1. Классификация химических реакций в неорганической и органической химии.
- •Классификация органических реакций
- •1.4.2. Тепловой эффект химической реакции. Термохимические уравнения.
- •1.4.3. Скорость реакции, ее зависимость от различных факторов.
- •1.4.4. Обратимые и необратимые химические реакции. Химическое равновесие. Смещение химического равновесия под действием различных факторов.
- •1.4.5. Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты.
- •Сильные электролиты
- •Слабые электролиты
- •1.4.6. Реакции ионного обмена.
- •1.4.7. Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная.
- •1.4.8. Реакции окислительно-восстановительные. Коррозия металлов и способы защиты от нее.
- •Коррозия металлов и способы защиты от нее.
- •Защита металлов от коррозии
- •1.4.9. Электролиз расплавов и растворов (солей, щелочей, кислот).
- •Закономерности катодного восстановления
- •Закономерности анодного окисления
- •2. Неорганическая химия
- •2.1. Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная)
- •Бинарные соединения
- •Сложные соединения
- •2.2. Характерные химические свойства простых веществ – металлов: щелочных, щелочноземельных, алюминия; переходных металлов (меди, цинка, хрома, железа) Щелочные металлы
- •Щелочноземельные металлы
- •Взаимодействие алюминия с серой при нагревании.
- •2.3. Характерные химические свойства простых веществ – неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния.
- •2.4. Характерные химические свойства оксидов: основных, амфотерных, кислотных.
- •2.5. Характерные химические свойства оснований и амфотерных гидроксидов.
- •Свойства оснований
- •2.6. Характерные химические свойства кислот.
- •2.7. Характерные химические свойства солей: средних, кислых, основных, комплексных (на примере соединений алюминия и цинка)
- •2.8. Взаимосвязь различных классов неорганических веществ.
1.3.2. Электроотрицательность. Степень окисления и валентность химических элементов.
Электроотрицательностью называется свойство химического элемента притягивать к своему атому электроны от атомов других элементов, с которыми данный элемент образует химическую связь в соединениях.
При образовании химической связи между атомами разных элементов общее электронное облако смещается к более электроотрицательному атому, из-за чего связь становится ковалентно-полярной, а при большой разности электроотрицательностей – ионной.
Электроотрицательность учитывается при написании химических формул: в бинарных соединениях сзади записывается символ наиболее электроотрицательного элемента.
Электроотрицательность возрастает в направлении слева направо для элементов каждого периода и уменьшается в направлении сверху вниз для элементов одной и той же группы ПС.
Валентностью элемента называется свойство его атомов соединяться с определенным числом других атомов.
Различают стехиометрическую, электронную валентность и координационное число. Мы рассмотрим только стехиометрическую валентность.
Стехиометрическая валентность показывает, сколько атомов другого элемента присоединяет атом данного элемента. За единицу валентности принята валентность водорода, т.к. водород всегда одновалентен. Например, в соединениях HCl, H2O, NH3 (правильное написание аммиака Н3N уже используется в современных пособиях), СН4 хлор одновалентен, кислород двухвалентен, азот трехвалентен и углерод четырехвалентен.
Стехиометрическая валентность кислорода обычно равна 2. Так как почти все элементы образуют соединения с кислородом, то удобно его использовать в качестве эталона для определения валентности другого элемента. Например, в соединениях Na2O, CoO, Fe2O3, SO3 натрий одновалентен, кобальт двухвалентен, железо трехвалентно, сера шестивалентна.
В окислительно-восстановительных реакциях нам важно будет определять степени окисления элементов.
Степенью окисления элемента в веществе называется его стехиометрическая валентность, взятая со знаком плюс или минус.
Химические элементы подразделяются на элементы постоянной валентности элементы переменной валентности.
1.3.3. Вещества молекулярного и немолекулярного строения. Тип кристаллической решетки. Зависимость свойств веществ от их состава и строения.
В зависимости от того, в каком состоянии соединения находятся в природе, они делятся на молекулярные и немолекулярные. В молекулярных веществах мельчайшими структурными частицами являются молекулы. Эти вещества имеют молекулярную кристаллическую решетку. В немолекулярных веществах мельчайшими структурными частицами являются атомы или ионы. Кристаллическая решетка у них атомная, ионная или металлическая.
Тип кристаллической решетки во многом определяет свойства веществ. Например, металлы, имеющие металлический тип кристаллической решетки, отличаются от всех остальных элементов высокой пластичностью, электро- и теплопроводностью. Эти свойства, а также и многие другие – ковкость, металлический блеск и т.п. обусловлены особым видом связи между атомами металла -- металлической связью. Необходимо отметить, что свойства, присущие металлам, проявляются только в конденсированном состоянии. Например, серебро в газообразном состоянии не обладает физическими свойствами металлов.
Особый тип связи в металлах – металлическая – обусловлен дефицитом валентных электронов, поэтому они общие для всей структуры металла. Наиболее простая модель строения металлов предполагала, что кристаллическая решетка металлов состоит из положительных ионов, окруженных свободными электронами, движение электронов происходит хаотически, подобно молекулам газа. Однако такая модель, качественно объясняя многие свойства металлов, при количественной проверке оказывается недостаточной. Дальнейшая разработка теории металлического состояния привела к созданию зонной теории металлов, которая основывается на представлениях квантовой механики.
В узлах кристаллической решетки находятся катионы и атомы металла, а электроны свободно перемещаются по кристаллической решетке.
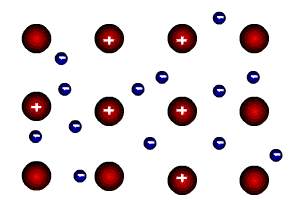
Характерным механическим свойством металлов является пластичность, обусловленная особенностями внутреннего строения их кристаллов. Под пластичностью понимают способность тел под действием внешних сил подвергаться деформации, которая остается и после прекращения внешнего воздействия. Это свойство металлов позволяет придавать им различную форму при ковке, прокатывать металл в листы или вытягивать в проволоку.
Пластичность металлов обусловлена тем, что при внешнем воздействии слои ионов, образующих кристаллическую решетку, сдвигаются относительно друг друга без разрыва. Это происходит в результате того, что переместившиеся электроны благодаря свободному перераспределению продолжают осуществлять связь межу ионными слоями. При механическом воздействии на твердое вещество с атомной решеткой смещаются отдельные ее слои и сцепление между ними нарушается из-за разрыва ковалентных связей.
Если в узлах кристаллической решетки находятся ионы, то эти вещества образуют ионный тип кристаллической решетки.


Это соли, а также оксиды и гидроксиды типичных металлов. Это твердые, хрупкие вещества, но основное их качество: растворы и расплавы этих соединений проводят электрический ток.
Если в узлах кристаллической решетки находятся атомы, то эти вещества образуют атомный тип кристаллической решетки (алмаз, бор, кремний оксиды алюминия и кремния). По свойствам очень твердые и тугоплавкие, нерастворимы в воде.
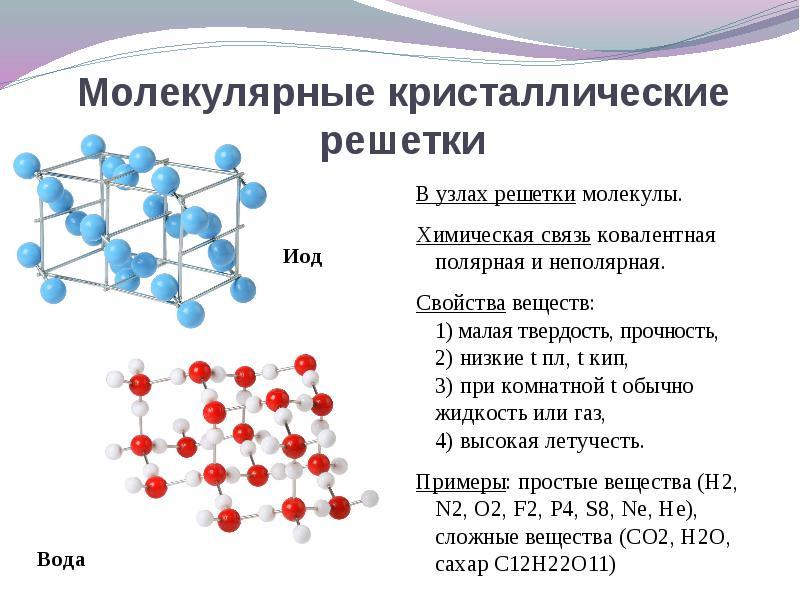
Если в узлах кристаллической решетки находятся молекулы, то эти вещества образуют молекулярный тип кристаллической решетки (при обычных условиях газы и жидкости: О2, HCl; I2 органические вещества).
Интересно отметить металл галлий, который плавится при температуре 30оС. Эта его аномалия объясняется тем, что в узлах кристаллической решетки находятся молекулы Ga2 и его свойства в чем становятся схожи с веществами, имеющие молекулярную кристаллическую решетку.
Пример. Немолекулярное строение имеют все неметаллы группы:
1) углерод, бор, кремний; 2) фтор, бром, иод;
3)кислород, сера, азот; 4) хлор, фосфор, селен.
В немолекулярных веществах мельчайшими структурными частицами являются атомы или ионы. Кристаллическая решетка у них атомная, ионная или металлическая
При решении этого вопроса проще идти от противного. Если в узлах кристаллической решетки находятся молекулы, то эти вещества образуют молекулярный тип кристаллической решетки (при обычных условиях газы и жидкости: О2, HCl; также I2, ромбическая сера S8, белый фосфор Р4, органические вещества). По свойствам это непрочные легкоплавкие соединения.
Во втором ответе есть газ фтор, в третьем – газы кислород, азот, в четвертом – газ хлор. Значит, эти вещества имеют молекулярную кристаллическую решетку и молекулярное строение.
В первом ответе все вещества – твердые соединения при обычных условиях и образуют атомную решетку, значит, имеют немолекулярное строение.
Правильный ответ: 1) углерод, бор, кремний
