
- •2. Значения, которые принимают квантовые числа.
- •3. Обозначение состояния электрона в атоме.
- •4. Форма и знаки орбиталей.
- •5. Энергия электрона в многоэлектронном атоме.
- •1.2. Периодический закон и Периодическая система химических элементов д.И. Менделеева
- •1.2.1. Закономерности изменения свойств элементов и их соединений по периодам и группам
- •1.2.2. Общая характеристика металлов iа – iiiа групп в связи с их положением в Периодической системе химических элементов д.И. Менделеева и особенностями строения их атомов
- •1.2.3. Характеристика переходных металлов (меди, цинка, хрома, железа) по их положению в Периодической системе химических элементов д.И. Менделеева и особенностями строения их атомов
- •1.2.4. Общая характеристика неметаллов ivа – viiа групп в связи с их положением в Периодической системе химических элементов д.И. Менделеева и особенностями строения их атомов
- •Химические свойства.
- •1.3.1. Ковалентная химическая связь, ее разновидности и механизмы образования. Характеристики ковалентной связи (полярность и энергия связи. Ионная, металлическая и водородная связь.
- •Ионная связь
- •Металлическая связь
- •Водородная связь
- •Водородная связь в молекуле воды
- •Виды химической связи
- •1.3.2. Электроотрицательность. Степень окисления и валентность химических элементов.
- •1.3.3. Вещества молекулярного и немолекулярного строения. Тип кристаллической решетки. Зависимость свойств веществ от их состава и строения.
- •1.4. Химическая реакция.
- •1.4.1. Классификация химических реакций в неорганической и органической химии.
- •Классификация органических реакций
- •1.4.2. Тепловой эффект химической реакции. Термохимические уравнения.
- •1.4.3. Скорость реакции, ее зависимость от различных факторов.
- •1.4.4. Обратимые и необратимые химические реакции. Химическое равновесие. Смещение химического равновесия под действием различных факторов.
- •1.4.5. Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты.
- •Сильные электролиты
- •Слабые электролиты
- •1.4.6. Реакции ионного обмена.
- •1.4.7. Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная.
- •1.4.8. Реакции окислительно-восстановительные. Коррозия металлов и способы защиты от нее.
- •Коррозия металлов и способы защиты от нее.
- •Защита металлов от коррозии
- •1.4.9. Электролиз расплавов и растворов (солей, щелочей, кислот).
- •Закономерности катодного восстановления
- •Закономерности анодного окисления
- •2. Неорганическая химия
- •2.1. Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная)
- •Бинарные соединения
- •Сложные соединения
- •2.2. Характерные химические свойства простых веществ – металлов: щелочных, щелочноземельных, алюминия; переходных металлов (меди, цинка, хрома, железа) Щелочные металлы
- •Щелочноземельные металлы
- •Взаимодействие алюминия с серой при нагревании.
- •2.3. Характерные химические свойства простых веществ – неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния.
- •2.4. Характерные химические свойства оксидов: основных, амфотерных, кислотных.
- •2.5. Характерные химические свойства оснований и амфотерных гидроксидов.
- •Свойства оснований
- •2.6. Характерные химические свойства кислот.
- •2.7. Характерные химические свойства солей: средних, кислых, основных, комплексных (на примере соединений алюминия и цинка)
- •2.8. Взаимосвязь различных классов неорганических веществ.
1.4.9. Электролиз расплавов и растворов (солей, щелочей, кислот).
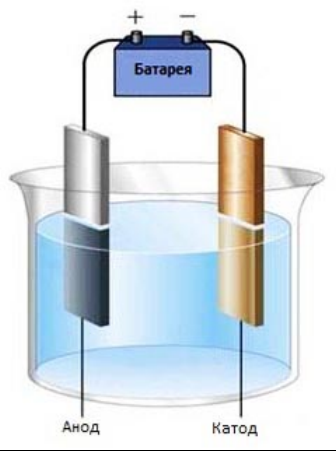
Электролизом называется несамопроизвольная химическая реакция, протекающая при пропускании постоянного тока через раствор или расплав электролита.
Простейшая установка для проведения реакции электролиза. Через раствор электролита пропускается постоянный электрический ток
К катоду (-) движутся катионы, а к аноду (+) – анионы
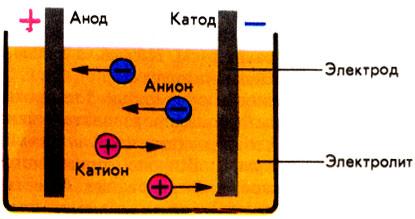
Закономерности катодного восстановления
Так как на катоде идет реакция восстановления, то в первую очередь должны реагировать наиболее сильные окислители, т.е. имеющие наиболее положительный электродный потенциал.
Для катодного восстановления при электролизе водного раствора электролита все окислители можно разделить на три группы.
1. Если соль содержит катион активного металла, электродный потенциал которых существенно более отрицателен, чем потенциал водородного электрода (в ряду напряжений до Аl). В водных растворах разряд этих ионов практически не происходит, так как на катоде происходит разложение только воды.
Kатод: 2H2O + 2e = H2 + 2OH‑
2. Если соль образована катионом неактивного металла (в ряду напряжений за водородом), то на катоде выделяется сам металл, а разряд катионов водорода не происходит.
Катод: Cu2+ + 2e = Cu
3. Если соль образована катионом металла, электродный потенциал которого мало отличается от водородного (они стоят в ряду напряжения между алюминием и водородом), то идут оба процесса, которые в сильной степени зависят от условий электролиз (плотности тока и т.д.). На катоде в этом случае мы будем писать оба процесса: и разложение воды, и выделение металла.
Kатод: 2H2O + 2e = H2 + 2OH‑
Ni2+ +2e=Ni
Кроме того, выделение водорода на многих катодах идет с более высоким перенапряжением, чем перенапряжение разряда многих металлов. Так, например, для солей цинка сначала выделяется водород, а при больших плотностях тока только цинк.
В данном случае высокое водородное перенапряжение – явление положительное, т.к. из водных растворов удается выделить многие металлы, которые более активны, чем водород.
Закономерности анодного окисления
Характер реакций, протекающих на аноде, зависит как от присутствия молекул воды, так и от вещества, из которого сделан анод. Нерастворимые аноды (графит, платина) при электролизе сами не посылают электроны во внешнюю цепь, электроны посылаются в результате окисления анионов и молекул воды.
На аноде протекают реакции окисления восстановителей, поэтому в первую очередь на аноде должны реагировать наиболее сильные восстановители (имеющие меньший электродный потенциал).
1. На аноде разряжаются простые анионы (Cl‑, Br‑, I‑, S2-), кроме F‑.
Анод: 2Cl‑ ‑ 2e = Cl2
2. Сложные анионы и F‑ сами не разряжаются, а происходит анодное окисление воды:
Анод: 2Н2О – 4е = О2 + 4Н+
3. Если анод растворимый, то конкурируют три процесса:
а) Ме – ne = Men+ ‑ растворение (окисление) металла;
б) 2Н2О – 4е = О2 + 4Н+ окисление воды =1,23 В;
в) Окисление анионов.
Наименьшим потенциалом обладает окисление металла, поэтому на аноде будет происходить именно этот процесс.
В случае электролиза CuCl2 с растворимым медным анодом будут происходить следующие процессы:
на аноде: Cu – 2e = Cu2+
на катоде: Cu2+ + 2e = Cu
Суммарная реакция 0=0, т.е. просто происходит перенос меди с анода на катод. Этот процесс называется рафинированием (очисткой) меди.
При электролизе расплавов воды нет, и будут разряжаться сами катионы и анионы.
Примеры
1. Электролиз СuSO4 Cur2+ + SO42-
Медь – металл неактивный (φо= +0,34 В), поэтому на катоде идет только: разрядка катиона, а на аноде разрядка воды, т.к. анион SO42- сложный.
на катоде (-): Cu2+ + 2е Cu;
Cu2+ и Н2О
на аноде (+): 2Н2О - 4е О2 + 4Н+
SO42- и Н2О
Схема
электролиза:
![]()
Для СuSO4 на аноде выделяется кислород, а на катоде медь.
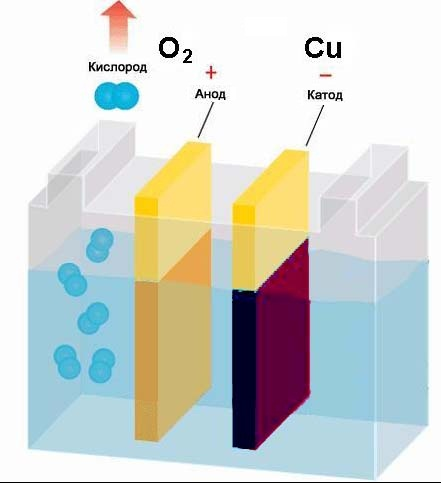
2. Электролиз HCl
Н+ можно отнести к неактивным, поэтому на катоде идет разрядка катиона, а на аноде идет разрядка хлорид иона, т.к. анион простой.
На катоде: 2Н+ + 2е Н2
Н+ и Н2О
На аноде: 2Cl- - 2e Cl2
Cl- и Н2О
Схема электролиза
2HCl Н2 + Cl2
3. Электролиз NaOH
Натрий – активный металл (φо= -2,71 В), поэтому на катоде идет только разрядка вода, а на аноде тоже разрядка воды, т.к. анион ОН- сложный.
на катоде (-): 2Н2О + 2е Н2 + 2ОН-
Na+ и Н2О
на аноде (+): 2Н2О - 4е О2 + 4Н+
OH- и Н2О
Схема электролиза
2Н2О 2Н2 + О2
При электролизе гидроксида натрия на катоде выделяется в 2 раза больше газа (водорода), чем на аноде (кислорода).

