
- •2. Значения, которые принимают квантовые числа.
- •3. Обозначение состояния электрона в атоме.
- •4. Форма и знаки орбиталей.
- •5. Энергия электрона в многоэлектронном атоме.
- •1.2. Периодический закон и Периодическая система химических элементов д.И. Менделеева
- •1.2.1. Закономерности изменения свойств элементов и их соединений по периодам и группам
- •1.2.2. Общая характеристика металлов iа – iiiа групп в связи с их положением в Периодической системе химических элементов д.И. Менделеева и особенностями строения их атомов
- •1.2.3. Характеристика переходных металлов (меди, цинка, хрома, железа) по их положению в Периодической системе химических элементов д.И. Менделеева и особенностями строения их атомов
- •1.2.4. Общая характеристика неметаллов ivа – viiа групп в связи с их положением в Периодической системе химических элементов д.И. Менделеева и особенностями строения их атомов
- •Химические свойства.
- •1.3.1. Ковалентная химическая связь, ее разновидности и механизмы образования. Характеристики ковалентной связи (полярность и энергия связи. Ионная, металлическая и водородная связь.
- •Ионная связь
- •Металлическая связь
- •Водородная связь
- •Водородная связь в молекуле воды
- •Виды химической связи
- •1.3.2. Электроотрицательность. Степень окисления и валентность химических элементов.
- •1.3.3. Вещества молекулярного и немолекулярного строения. Тип кристаллической решетки. Зависимость свойств веществ от их состава и строения.
- •1.4. Химическая реакция.
- •1.4.1. Классификация химических реакций в неорганической и органической химии.
- •Классификация органических реакций
- •1.4.2. Тепловой эффект химической реакции. Термохимические уравнения.
- •1.4.3. Скорость реакции, ее зависимость от различных факторов.
- •1.4.4. Обратимые и необратимые химические реакции. Химическое равновесие. Смещение химического равновесия под действием различных факторов.
- •1.4.5. Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты.
- •Сильные электролиты
- •Слабые электролиты
- •1.4.6. Реакции ионного обмена.
- •1.4.7. Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная.
- •1.4.8. Реакции окислительно-восстановительные. Коррозия металлов и способы защиты от нее.
- •Коррозия металлов и способы защиты от нее.
- •Защита металлов от коррозии
- •1.4.9. Электролиз расплавов и растворов (солей, щелочей, кислот).
- •Закономерности катодного восстановления
- •Закономерности анодного окисления
- •2. Неорганическая химия
- •2.1. Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная)
- •Бинарные соединения
- •Сложные соединения
- •2.2. Характерные химические свойства простых веществ – металлов: щелочных, щелочноземельных, алюминия; переходных металлов (меди, цинка, хрома, железа) Щелочные металлы
- •Щелочноземельные металлы
- •Взаимодействие алюминия с серой при нагревании.
- •2.3. Характерные химические свойства простых веществ – неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния.
- •2.4. Характерные химические свойства оксидов: основных, амфотерных, кислотных.
- •2.5. Характерные химические свойства оснований и амфотерных гидроксидов.
- •Свойства оснований
- •2.6. Характерные химические свойства кислот.
- •2.7. Характерные химические свойства солей: средних, кислых, основных, комплексных (на примере соединений алюминия и цинка)
- •2.8. Взаимосвязь различных классов неорганических веществ.
1.4.5. Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты.
Электролитами называют вещества, которые в растворах проводят электрический ток. К электролитам относятся кислоты, основания и растворимые соли. При растворении в воде они распадаются на ионы движение которых обеспечивает электропроводность растворов этих веществ. Этим вопросом много занимался Аррениус. Он пришел к выводу, что диссоциация молекул растворенных электролитов на ионы происходит не под действием тока, как считали до него, а уже в процессе растворения, независимо от того пропускают через раствор электрический ток или нет.

Для количественной характеристики соотношения диссоциированных и недиссоциированных молекул электролита пользуются степенью электролитической диссоциации .

Основные положения теории электролитической диссоциации были разработана Гунде Сван Аррениусом (1887) и сводятся к следующему.
1. Электролиты при растворении в воде распадаются (диссоциируют) на ионы – частицы с положительным (катионы) и отрицательным (анионы) зарядом. Ионы могут быть простыми (Na+, S2- и т.д.), сложными (NH4+, SO42- и т.д.) или комплексными ([Fe(CN)6]4-, [Cu(NH3)4]2+ и т.д.). «Ион» в переводе с греческого означает «странствующий»: в растворе ионы беспорядочно передвигаются в различных направлениях.
2. Под действием электрического тока движение ионов становится направленным: катионы движутся к катоду, а анионы к аноду. По этому признаку все соединения делятся на электролиты и неэлектролиты.
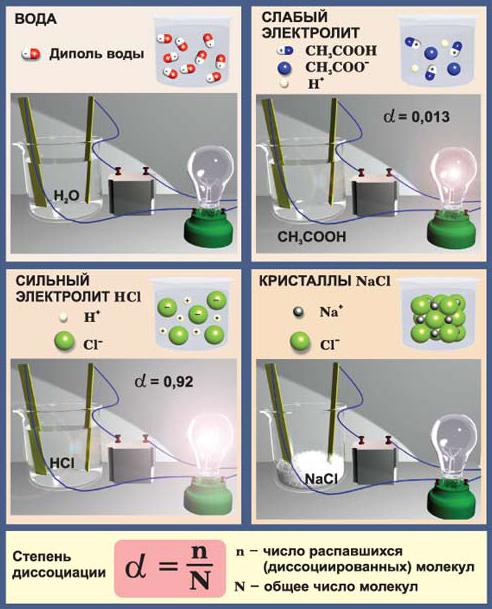
Чистая вода очень слабый электролит – лампочка не горит; Уксусная кислота слабый электролит – лампочка горит слабо; соляная кислота (HCl) сильный электролит – лампочка горит ярко; кристаллический NaCl не содержит ионы – лампочка не горит. Ионы у хлорида натрия появляются только в растворе или в расплаве.
3. Диссоциация – обратимый процесс, поэтому в уравнениях ставится знак обратимости.
NaCl Na+ + Cl-; H2SO4 2H+ + SO42-
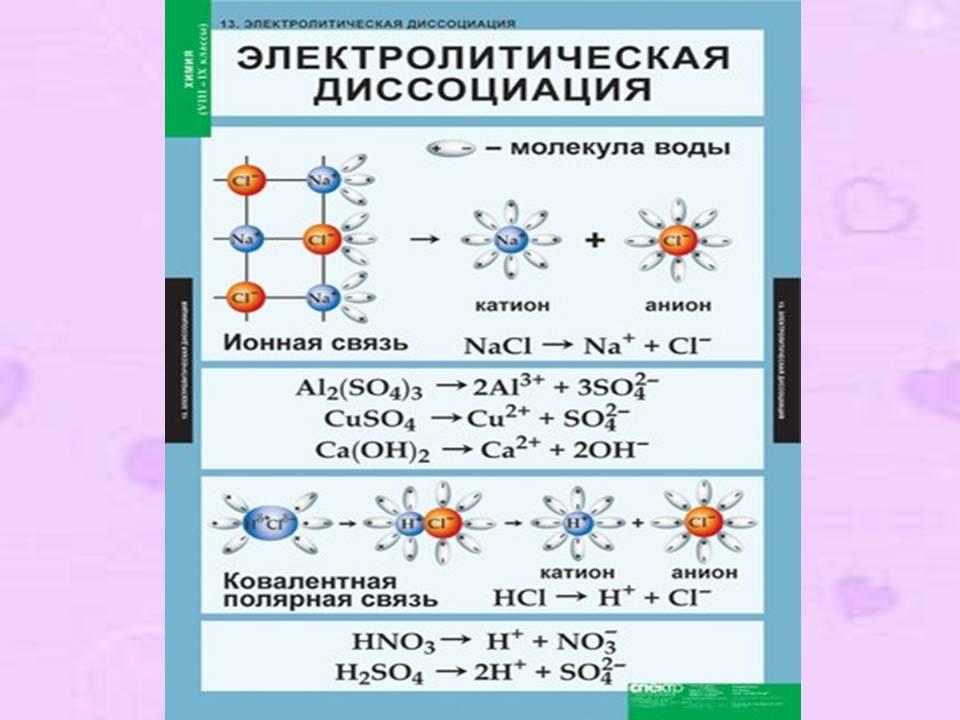
Легче всего диссоциируют вещества с ионной связью, состоящие из ионов. Полярные молекулы воды (диполи) притягиваются к поверхностным ионам вещества; происходит ослабление химической связи между ионами, которое зависит от диэлектрической проницаемости растворителя (у воды оно очень велико 81). Достаточно теплового движения молекул, чтобы вещество распалось на гидратированные ионы.
Расплавы ионных соединений тоже являются сильными электролитами. Высокая температура расплавов способствует их диссоциации на ионы.
Для веществ с ковалентно-полярными связями сначала происходит поляризация связи под действием диполей воды; связь превращается в ионную и происходит диссоциация на гидратированные ионы.
Доказано, что все ионы находятся в растворе в гидратированном состоянии, что препятствует их обратное соединение – ассоциацию. Правильнее написать диссоциацию так:
NaCl + (n+m)H2O Na+nH2O + Cl-mH2O,
Однако, в связи с тем, что неопределенный состав гидратов для решения практических задач не имеет значения, схемы диссоциации записываются без участия воды.
Существует классификация электролитов по величине степени электролитической диссоциации, которую ввел Аррениус.
Электролиты, для которых в децимолярном (С=0,1 моль/л) растворе при 25оС α>0,3, называются сильными. Эта классификация является условной, т.к. степень диссоциации зависит от концентрации раствора, применяемого растворителя. Более удобным показателем силы электролита является константа диссоциации, которая не зависит от концентрации.
