
- •2. Значения, которые принимают квантовые числа.
- •3. Обозначение состояния электрона в атоме.
- •4. Форма и знаки орбиталей.
- •5. Энергия электрона в многоэлектронном атоме.
- •1.2. Периодический закон и Периодическая система химических элементов д.И. Менделеева
- •1.2.1. Закономерности изменения свойств элементов и их соединений по периодам и группам
- •1.2.2. Общая характеристика металлов iа – iiiа групп в связи с их положением в Периодической системе химических элементов д.И. Менделеева и особенностями строения их атомов
- •1.2.3. Характеристика переходных металлов (меди, цинка, хрома, железа) по их положению в Периодической системе химических элементов д.И. Менделеева и особенностями строения их атомов
- •1.2.4. Общая характеристика неметаллов ivа – viiа групп в связи с их положением в Периодической системе химических элементов д.И. Менделеева и особенностями строения их атомов
- •Химические свойства.
- •1.3.1. Ковалентная химическая связь, ее разновидности и механизмы образования. Характеристики ковалентной связи (полярность и энергия связи. Ионная, металлическая и водородная связь.
- •Ионная связь
- •Металлическая связь
- •Водородная связь
- •Водородная связь в молекуле воды
- •Виды химической связи
- •1.3.2. Электроотрицательность. Степень окисления и валентность химических элементов.
- •1.3.3. Вещества молекулярного и немолекулярного строения. Тип кристаллической решетки. Зависимость свойств веществ от их состава и строения.
- •1.4. Химическая реакция.
- •1.4.1. Классификация химических реакций в неорганической и органической химии.
- •Классификация органических реакций
- •1.4.2. Тепловой эффект химической реакции. Термохимические уравнения.
- •1.4.3. Скорость реакции, ее зависимость от различных факторов.
- •1.4.4. Обратимые и необратимые химические реакции. Химическое равновесие. Смещение химического равновесия под действием различных факторов.
- •1.4.5. Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты.
- •Сильные электролиты
- •Слабые электролиты
- •1.4.6. Реакции ионного обмена.
- •1.4.7. Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная.
- •1.4.8. Реакции окислительно-восстановительные. Коррозия металлов и способы защиты от нее.
- •Коррозия металлов и способы защиты от нее.
- •Защита металлов от коррозии
- •1.4.9. Электролиз расплавов и растворов (солей, щелочей, кислот).
- •Закономерности катодного восстановления
- •Закономерности анодного окисления
- •2. Неорганическая химия
- •2.1. Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная)
- •Бинарные соединения
- •Сложные соединения
- •2.2. Характерные химические свойства простых веществ – металлов: щелочных, щелочноземельных, алюминия; переходных металлов (меди, цинка, хрома, железа) Щелочные металлы
- •Щелочноземельные металлы
- •Взаимодействие алюминия с серой при нагревании.
- •2.3. Характерные химические свойства простых веществ – неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния.
- •2.4. Характерные химические свойства оксидов: основных, амфотерных, кислотных.
- •2.5. Характерные химические свойства оснований и амфотерных гидроксидов.
- •Свойства оснований
- •2.6. Характерные химические свойства кислот.
- •2.7. Характерные химические свойства солей: средних, кислых, основных, комплексных (на примере соединений алюминия и цинка)
- •2.8. Взаимосвязь различных классов неорганических веществ.
2.8. Взаимосвязь различных классов неорганических веществ.
Между классами веществ существует возможность их взаимного превращения: из простых веществ получают оксиды, из оксидов – основания или кислоты, из кислот – соли. Возможен и обратный переход от солей к основаниям и кислотам, от основания и кислот к оксидам, а от оксидов к простым веществам.
Подобная связь между классами соединений, позволяющая получать вещество одного класса из вещества другого, называется генетической. Необходимо иметь в виду, что не всегда одно вещество из другого можно получить напрямую. Например, гидроксид меди(II) Cu(OH)2 нельзя получить взаимодействием оксида меди(II) с водой. В этом случае применяют косвенный путь: на оксида меди(II) действуют кислотой и получают соль, а из соли действием щелочи получают гидроксид меди(II).
Генетическую связь между основными классами неорганических соединений можно показать схематически
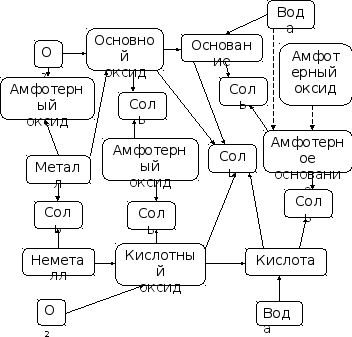
1. Металл, реагируя с кислородом, дает основной или амфотерный оксид. Неметалл при реакции с кислородом дает только кислотный оксид. Реакции проходят при нагревании, так как кислород имеет прочную двойную связь.
2. Металл может реагировать с неметаллом, образуя соль. Только активные металлы и неметаллы реагируют при обычных условиях. Для остальных элементов для проведения реакции необходимо нагревание.
3. Основной оксид может реагировать с амфотерным и кислотным оксидами, образуя соли. Кислотный оксид может реагировать с амфотерным и основным оксидами, образуя соли. Оксиды активных металлов могут реагировать при обычных температурах, а остальные при нагревании.
4. Основной оксид с водой образует основания. Только активные щелочные и щелочно-земельные металлы реагируют с водой при обычных условиях с образованием сильных оснований, для остальных необходим нагрев. Например, оксид магния лучше реагирует с водой при нагревании, так как гидроксид магния малорастворим.
MgO + Н2О = Mg(OH)2
Многие кислотные оксиды реагируют с водой, образуя кислоты. Некоторые кислотные оксиды с водой при обычных условиях не взаимодействуют, поэтому их получают косвенным путем.
Амфотерные оксиды с водой практически не взаимодействуют, поэтому их получают косвенным путем.
5. Основания могут реагировать с амфотерным основаниями и кислотами, образуя соли. Кислоты реагируют с основаниями и амфотерными основаниями, образуя соли.
