
- •3. Состав системы белой крови. Разновидности лейкоцитов. Отличия гранулоцитов и агранулоцитов.
- •4.Общие свойства и функции лейкоцитов.
- •6. Лейкоцитозы. Состояния при которых они х-ны
- •7. Лейкопении, состояния, для которых они характерны
- •8.Лейкоцитарна формула та лейкоцитарний профіль , значення їх визначення у діагностиці.
- •9 Снр, клеточная и гуморальная подсистемы, объекты эффекторы, факторы, функции, механизмы действия
- •10. Иммунная система,клеточная и гуморальная подсистемы,объекты, эффекторы, функции, механизм действия.
- •11. Общая характеристика лейкопоэза, стадии, значение лейкопоэтинов.
- •14.Современные научные данные, которые дополняют фагоцитарную теорию Мечникова.
- •15. Стадии и механизмы эмиграции сквозь сосуды лейкоцитами, во время движения по крови.
- •20. О2 -независимая система бактерицидности, синтез ее компонентов.
- •21. Взаимодействие о2-зависимой и о2-независимой систем бактерицидности (бактериостатичности) в совершении киллинг эффекта фагоцитов
- •24. Возрастные особенности в количестве лейкоцитов. Двойной перекрест в соотношении нейтрофилов и лимфоцитов у детей.
- •25. Генез, структура, общие и спец. Свойства и функции нейтофилов
- •26. Генез,структура основные и специф ф-ии св-ва эозинофилов
- •28.Генез ,особенности структуры , свойства и функции тканевых базофилов
- •31. Иммунные реакции с участием в-системы.
- •32. Генез, строение, особенности и функции т-лимфоцитов
- •35.Генез,структурные особенности,виды ,свойства и функции Мкф.
- •36. Тромбоцитопоэз. Стадии, факторы и механизм регуляции. Причины и последствия тромбоцитопинии.
- •37. Структурные особенности, св-ва и ф-и тромбоцитов
- •39. Синтез та секреція тромбоцитами біологічно активних речовин-тромоцитарних факторів ,їх функціональна роль (структура та властивості)
- •40. Функциональная роль тромбоцитов в первичном и вторичном гомеостазе
- •43.Система сосудисто –тромбоцитарного гемостаза, его составляяющие, стадии, факторы и механизмы регуляции, функциональное значение
- •44. Система вторичного (гемокоагуляционного) гемостаза, стадии, механизмы действия плазменных факторов.
- •46. Внешний путь системы гемокоагуляции, каскадно-комплексная схема вторичного (гемокоагулятивного) гемостаза.
- •47.Внутренний путь системы гемокоагуляции, каскадно-комплексная схема вторичного(гемокоагуляционного) гемостаза.
- •48. Взаимосвязь первичного и вторичного гемостаза, функциональное значение.
- •1. Вазоконстрикция
- •2. Формирование временного тромбоцитарного гвоздя (гемостатической пробки)
- •52.Система фибринолиза (плазминовая ), стадии, факторы та механизмы регуляции, функциональное значение
- •53. Антикоагуляционнная система, ее функциональное значение. Отличие первичных и вторичных антикоагулянтов.
- •56.Фибринолитическая система. Механизмы ее функционирования.
- •58. Отличие гранулоцитов от агранулоцитов.
- •59. Разновидности лимфоцитов,генез,структура,св-ва
44. Система вторичного (гемокоагуляционного) гемостаза, стадии, механизмы действия плазменных факторов.
Под термином «гемостаз» понимают комплекс реакций, направленных на остановку кровотечения при травме сосудов. Значение системы гемостаза намного сложнее и шире. Факторы гемостаза принимают участие в сохранении жидкого состояния крови, регуляции транскапиллярного обмена, резистентности сосудистой стенки, влияют на интенсивность репаративных процессов и др.
По современным представлениям, в остановке кровотечения задействовано два механизма:
1) первичный гемостаз (сосудисто-тромбоцитарный), в котором принимают участие стенки сосудов, тромбоциты и отчасти эритроциты; 2) вторичный гемостаз, когда в процесс свертывания крови включаются белки плазмы крови (плазменные факторы свертывания крови). Следует отметить, что деление гемостаза на клеточные и плазменные является условным, так как в организме эти два звена свертывающей системы крови тесно связаны.
Процесс свертывания крови
При повреждении крупных кровеносных сосудов (артерий, вен, артериол), также происходит образование тромбоцитарной пробки, но она неспособна остановить кровотечение, так как легко вымывается током крови. Основное значение в этом процессе принадлежит свертыванию крови, сопровождающемуся в конечном итоге образованием плотного фибринового сгустка.
Плазменные и клеточные факторы свертывания крови
В свертывании крови принимает участие комплекс белков, находящихся в плазме (плазменные факторы гемокоагуляции), большинство из которых является проферментами. В отличие от тромбоцитарных факторов они обозначаются римскими цифрами.
Механизм свертывания крови
Процесс свертывания крови представляет собой преимущественно проферментно-ферментный каскад, в котором проферменты, переходя в активное состояние, приобретают способность активировать другие факторы свертывания крови. Подобная активация может носить последовательный и ретроградный характер.
Процесс свертывания крови может быть разделен на три фазы: первая включает комплекс последовательных реакций, приводящих к образованию протромбиназы, во вторую фазу осуществляется переход протромбина (фактор II) в тромбин (фактор IIа) и в третью фазу из фибриногена образуется фибрин.
Первая фаза фаза активации— образование протромбиназы может происходить по внешнему и внутреннему механизму. Внешний механизм предполагает обязательное присутствие тромбопластина (фактор III), внутренний же связан с участием тромбоцитов (фактор Р3) или разрушенных эритроцитов. Вместе с тем внутренний и внешний пути образования протромбиназы имеют много общего, так как активируются одними и теми же факторами (фактор ХIIа, калликреин, ВМК и др.), а также приводят в конечном итоге к появлению одного и того же активного фермента — фактора Ха, выполняющего функции протромбиназы. При этом и полный, и частичный тромбопластин служат матрицами, на которых в присутствии ионов Са2+ развертываются ферментативные реакции.
Формирование протромбиназы по внешнему пути начинается с активации фактора VII при его взаимодействии с тромбопластином и фактором ХIIа. Кроме того, фактор VII может переходить в деятельное состояние под влиянием факторов XIa, IXa, Ха, IIа и калликреина. В свою очередь фактор VIIa не только переводит фактор X в Ха (ведет к появлению протромбиназы), но и активирует фактор IX, участвующий в образовании протромбиназы по внутреннему механизму.
Образование протромбиназы по внешнему пути происходит чрезвычайно быстро (за 20—30 с), ведет к появлению небольших порций тромбина (IIа), который способствует необратимой агрегации тромбоцитов, активации факторов VIII и V и значительно ускоряет формирование протромбиназы по внутреннему механизму. Инициатором внутреннего механизма образования протромбиназы является фактор XII, который активируется травмированной поверхностью стенки сосуда, кожей, коллагеном, адреналином, в лабораторных условиях — при контакте со стеклом, после чего переводит фактор XI в XIa. В этой реакции может принимать участие калликреин (активируется фактором ХIIа) и ВМК (активируется калликреином). Фактор XIa оказывает непосредственное влияние на фактор IX, переводя его в фактор IXa. Специфическая деятельность последнего направлена на протеолиз фактора X и протекает при обязательном участии фактора VIII (или VIIIa).
Следует заметить, что активация фактора X под влиянием комплекса факторов VIII и IXa получила название теназной реакции.
Вторая фаза процесса свертывания крови фаза коагуляции — переход фактора II в фактор IIа осуществляется под влиянием протромбиназы (фактор Ха) в присутствии фактора V (Va) и сводится к протеолитическому расщеплению протромбина, благодаря чему появляется фермент тромбин, обладающий свертывающей активностью.
Третья стадия процесса свертывания крови фаза ретракции — переход фибриногена в фибрин — носит этапный характер. Под влиянием фактора IIа от фибриногена отщепляются фибринопептиды и образуется фибрин-мономер (фактор Im). Из него благодаря процессу полимеризации формируются олигомеры и димеры фибрина (фактор Iо и Id), из которых за счет продольного и поперечного связывания образуются протофибриллы — легкорастворимый фибрин, или фибрин S, быстро лизирующийся под влиянием протеаз (плазмина, трипсина). В дальнейшем в процесс образования фибрина вмешивается фактор XIII (фибриназа, фибринстабилизирующий фактор), который после активации тромбином в присутствии ионов Са2+ «прошивает» фибринполимеры дополнительными перекрестными связями, в результате чего появляется труднорастворимый фибрин, или фибрин i (insoluble). В результате этой реакции сгусток становится резистентным к фибринолитическим (протеолитическим) агентам и плохо поддается разрушению.
Последняя стадия — лизис (растворение) тромба. Это также многоступенчатый процесс, в котором протекают ферментативные взаимодействия многих веществ, в конечном итоге приводящих к появлению активного фермента — фибринолизина. Фибринолизин разрушает связи между нитями фибрина и переводит его вновь в нерастворимый фибриноген. В настоящее время принято говорить о существовании самостоятельной фибринолитической системы организма. Конечно, эти процессы в организме протекают значительно сложнее, и в них принимают участие гораздо большее число факторов.
45.
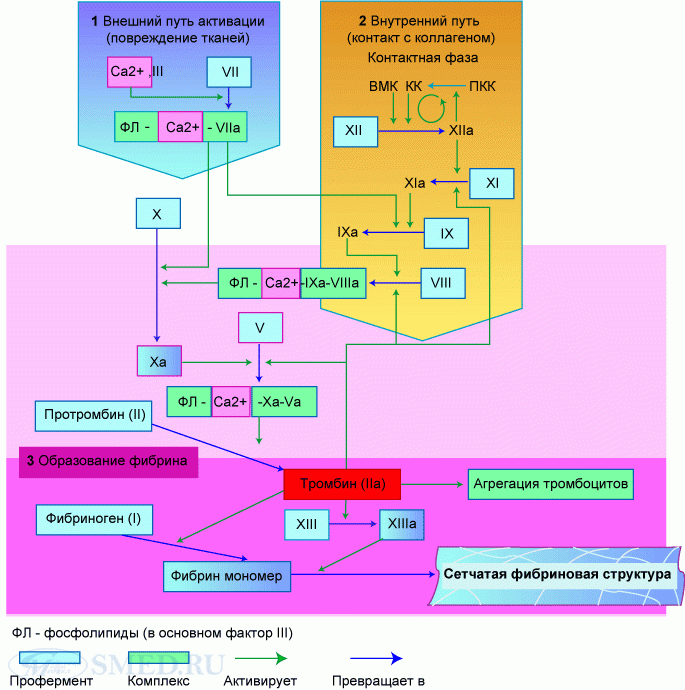
Внешний путь активации свёртывания крови
Основным путём активации свёртывания крови in vivo считается внешний путь. Компоненты этого пути следующие: тканевой фактор (ТФ, фактор III, тканевая тромбокиназа, тканевой тромбопластин), его ингибитор (ингибитор пути тканевого фактора, ИПТФ) и плазменный фактор VII. Тканевой фактор представляет собой внутренний мембранный гликопротеин, имеющийся во многих клетках; он не поступает в кровь до тех пор, пока не образуются протеазы или не произойдёт повреждение клеток in vivo. Тканевой фактор функционирует в качестве кофактора/рецептора, который в присутствии ионов кальция активирует фактор VII. Активация фактор VII приводит к открытию его активного серинового центра. Активация фактора VII может также происходить за счёт незначительного протеолитического действия других сериновых протеаз (тромбина, ФXIIa, ФIXa, и ФXa), а также за счёт самоактивации, однако самоактивация in vivo идёт незначительно. Комплекс ТФ/ФVIIa/Ca 2+ действует на два субстрата: фактор X (запуск общего пути) и ФIX (фактор внутреннего пути).
Внутренний путь активации свёртывания крови
Компонентами внутреннего пути являются факторы XII, XI, IX, XIII, кофакторы – высокомолекулярный кининоген (ВМК) и прекалликреин (ПК), а также их ингибиторы.
Внутренний путь запускается при повреждении эндотелия, когда обнажается отрицательно заряженная поверхность (например, коллаген) в пределах сосудистой стенки. Контактируя с такой поверхностью, активируется ФXII (образуется ФXIIa). Фактор XIIa активирует ФXI и превращает прекалликреин (ПК) в калликреин, который активирует фактор XII (петля положительной обратной связи). Механизм взаимной активации ФXII и ПК отличается большей быстротой по сравнению с механизмом самоактивации ФXII, что обеспечивает многократное усиление системы активации. Фактор XI и ПК связываются с активирующей поверхностью посредством высокомолекулярного кининогена (ВМК). Без ВМК активации обоих проферментов не происходит. Связанный ВМК может расщепляться калликреином (К) или связанным с поверхностью ФXIIa и инициировать взаимную активацию систем ПК-ФXII.
Фактор XIa активирует фактор IX. Фактор IX может также активироваться под действием комплекса ФVIIa/ФIII (перекрёст с каскадом внешнего пути), причём считается, что in vivo это доминирующий механизм. Активированный ФIXa требует наличия кальция и кофактора (ФVIII), для прикрепления к тромбоцитарному фосфолипиду и превращения фактора X в фактор Xa (переход с внутреннего на общий путь). Фактор VIII действует в качестве мощного ускорителя завершающей ферментативной реакции.
Фактор VIII, который также называют антигемофильным фактором, кодируется большим геном, расположенным на конце X-хромосомы. Он активируется под действием тромбина (основной активатор), а также факторов IXa и Xa. ФVIII циркулирует в крови, будучи связанным с фактором фон Виллебранда (ФВ) – большим гликопротеином, продуцируемым эндотелиальными клетками и мегакариоцитами . ФВ служит внутрисосудистым белком-носителем для ФVIII. Связывание ФВ с ФVIII стабилизирует молекулу ФVIII, увеличивает её период полусуществования внутри сосуда и способствует её транспорту к месту повреждения. Однако чтобы активированный фактор VIII мог проявить свою кофакторную активность, он должен отсоединиться от ФВ. Воздействие тромбина на комплекс ФVIII/ФВ приводит к отделению ФVIII от несущего протеина и расщеплению на тяжёлую и лёгкую цепи ФVIII, которые важны для коагулянтной активность ФVIII.
