
- •3. Состав системы белой крови. Разновидности лейкоцитов. Отличия гранулоцитов и агранулоцитов.
- •4.Общие свойства и функции лейкоцитов.
- •6. Лейкоцитозы. Состояния при которых они х-ны
- •7. Лейкопении, состояния, для которых они характерны
- •8.Лейкоцитарна формула та лейкоцитарний профіль , значення їх визначення у діагностиці.
- •9 Снр, клеточная и гуморальная подсистемы, объекты эффекторы, факторы, функции, механизмы действия
- •10. Иммунная система,клеточная и гуморальная подсистемы,объекты, эффекторы, функции, механизм действия.
- •11. Общая характеристика лейкопоэза, стадии, значение лейкопоэтинов.
- •14.Современные научные данные, которые дополняют фагоцитарную теорию Мечникова.
- •15. Стадии и механизмы эмиграции сквозь сосуды лейкоцитами, во время движения по крови.
- •20. О2 -независимая система бактерицидности, синтез ее компонентов.
- •21. Взаимодействие о2-зависимой и о2-независимой систем бактерицидности (бактериостатичности) в совершении киллинг эффекта фагоцитов
- •24. Возрастные особенности в количестве лейкоцитов. Двойной перекрест в соотношении нейтрофилов и лимфоцитов у детей.
- •25. Генез, структура, общие и спец. Свойства и функции нейтофилов
- •26. Генез,структура основные и специф ф-ии св-ва эозинофилов
- •28.Генез ,особенности структуры , свойства и функции тканевых базофилов
- •31. Иммунные реакции с участием в-системы.
- •32. Генез, строение, особенности и функции т-лимфоцитов
- •35.Генез,структурные особенности,виды ,свойства и функции Мкф.
- •36. Тромбоцитопоэз. Стадии, факторы и механизм регуляции. Причины и последствия тромбоцитопинии.
- •37. Структурные особенности, св-ва и ф-и тромбоцитов
- •39. Синтез та секреція тромбоцитами біологічно активних речовин-тромоцитарних факторів ,їх функціональна роль (структура та властивості)
- •40. Функциональная роль тромбоцитов в первичном и вторичном гомеостазе
- •43.Система сосудисто –тромбоцитарного гемостаза, его составляяющие, стадии, факторы и механизмы регуляции, функциональное значение
- •44. Система вторичного (гемокоагуляционного) гемостаза, стадии, механизмы действия плазменных факторов.
- •46. Внешний путь системы гемокоагуляции, каскадно-комплексная схема вторичного (гемокоагулятивного) гемостаза.
- •47.Внутренний путь системы гемокоагуляции, каскадно-комплексная схема вторичного(гемокоагуляционного) гемостаза.
- •48. Взаимосвязь первичного и вторичного гемостаза, функциональное значение.
- •1. Вазоконстрикция
- •2. Формирование временного тромбоцитарного гвоздя (гемостатической пробки)
- •52.Система фибринолиза (плазминовая ), стадии, факторы та механизмы регуляции, функциональное значение
- •53. Антикоагуляционнная система, ее функциональное значение. Отличие первичных и вторичных антикоагулянтов.
- •56.Фибринолитическая система. Механизмы ее функционирования.
- •58. Отличие гранулоцитов от агранулоцитов.
- •59. Разновидности лимфоцитов,генез,структура,св-ва
9 Снр, клеточная и гуморальная подсистемы, объекты эффекторы, факторы, функции, механизмы действия
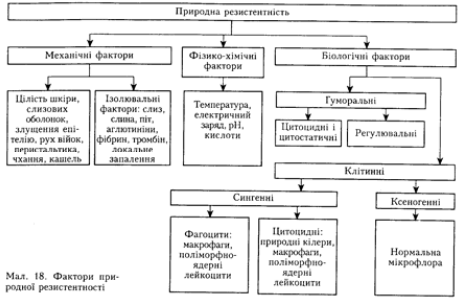
СНР – врожденный природный видовой иммунитет
Врожденный иммунитет (раньше называли неспецифические факторы резыстентности) — осуществляется с помощью большого количества клеточных, гуморальных факторов и физиологических барьеров организма.
1.Физиологические (естественные) барьеры:
а. Анатомические — кожа, слизистые оболочки, которые препятствуют проникновению микроорганизмов в организм;
б. Биохимические барьеры — секреты,выделяемые слизистыми оболочками, которые действуют бактерицидно (желудочно-кишечный сок и др.).
2. Гуморальные факторы (плазменные) – это компоненты системы комплемента, пропердин, калекриин – кининовая система, бета – лизины, лизоцим, фактор некроза опухолей, интерфероны,белки острой фазы воспаления, цитокины и другие.
3. Клеточные факторы – это нейтрофилы, базофилы, эозинофилы, моноциты, макрофаги, тучные клетки, NK(нормальные киллеры), тромбоциты.
Кл.звено – эндоцитоз: фаго и пиноцитоз
– воспаление – неспециф. Локальна или системная, с одной стороны патологическая, а с другой адаптационно-защитная реакция, в результате которой организм ценой частичных утрат сохраняет себя как жизнеспособную систему, форма клеточного неспецифичного врожденного иммунитета, представляющая собой локальную неспецифическую реакцию, характеризующуюся 4мя признаками:
гипертермия
гиперемия
отек – экссудация
боль или зуд
Исключение – аллергия – форма специфического иммунного ответа.
Осуществляется кл-эффекторами фагоцитами и пиноцитами
Гум.звено – система комплементв
– лизоцим (содержится во всех биологических жидкостях)
– катионные белки и пептиды (дефенсины)
– интерфероны
Объект действия чужеродный агент
Учасивуют клетки миелоидно-моноцитарного ряда – фагоцитирующие клетки и естественные киллеры, система фагоцитарных мононуклеаров(система мононуклеарных фагоцитов) – моноциты и макрофаги; костномозговые предшественники,пул относительно незрелых клеток, циркулирующих в крови(моноциты), конечную стадию дифференцировки – органо- и тканеспецифические макрофаги.
Микрофаги – гранулоциты нейтро- базо- и эозинофилы
Все разновидности лейкоцитов, кроме лимфоцитов могут фагоцитировать (В-л. Только пиноцитировать, Т-л. Ни то ни другое)
Основные эффекторы макрофаги и нейтрофилы
Комплемент – это термолабильная система белковых и гликопротеиновых факторов нормальной сыворотки крови. Белки системы компонента составляют около 10% от общего количества белков сыворотки крови. Основным источником образования компонентов системы комплемента являются гепатоциты и макрофаги. Частично компоненты системы комплемента образуются в селезенке, костном мозге, и в лимфоэпителиальных клетках во время воспаления.
Активация компонентов системы комплемента происходит двумя путями.
1.Классический путь активации системы комплемента (иммунный), когда первый компонент С1-активирует иммунный комплекс АГ +АТ, а С1- в свою очередьактивирует следующий компонент С2 и так далее каскадоподобно. Для активации комплемента по классическому пути нужно обязательно образование специфических иммуноглобулинов.
2.Альтернативный— не иммунный путь
Отличием альтернативного пути активации комплемента является то, что:
а). Для активации системы комплемента не нужно образование иммунных комплексов.
б). Альтернативный путь начинается без участия первых трех компонентов системы комплемента.
в). Альтернативный путь активации начинается сразу после попадания антигена в организм, а его активатором могутбытьбактериальные полисахариды, липополисахариды, токсины, вирусы, паразиты, опухолевые клетки и др.
При активации системы комплемента каждый компонент комплемента выполняет соответствующуюфункцию. На фагоцитах и ИГ есть рецепторы к компонентам системы комплементапри помощи, которых онсвязывается с ними.
Общая функциясистемы комплемента.
1.Комплементарный не иммунный ( активация по альтернативному пути ) и иммунный (по классическому ) лизис бактерий в результате образования МАК (мембрано — атакующего комплекса).2.Аутоантителозависимое уничтожение собственных клеток при аутоиммунных заболеваниях ( гломерулонефрит, коллагенозы)3.Нейтрализуюют вирусы.4.Усиливаютфагоцитоз.5.Актвируют тучные клетки, вследствие чего выделяютсямедиаторы воспаления и анафилотоксины, что способствуетусилению хемотаксиса фагоцитов, повышается проницаемость капилляров, что облегчаетпроникновение в очаг инкубации микробов, фагоцитов и антител.5.Принимают участие в элиминации из организма ЦИК. С3-компонент владеет способностью фиксироваться на константных фрагментах Ig и на соответствующих рецепторах фагоцитов. При помощи С3, ЦИК фиксируется на микро — и макрофагах ив такой обойметранспортируется в печень, селезенку, где и выводится из организма. При нарушении этого процессав организме развиваются аутоиммунные заболевания ( гломерулонефриты, коллагенозы и так далее)
Лизоцим-термостабильный белок типа муколитического фермента. Он содержится в тканевых жидкостях животных и человека - в слезах, слюне, перитонеальной жидкости, плазме сыворотке крови, в лейкоцитах, материнском молоке и др. Продуцируется моноцитами крови и тканевыми макроорганизмов. Он вызывает лизис многих сапрофитных бактерий, оказывая выраженное литическое действие на ряд патогенных микроорганизмов и не активен в отношении вирусов. Механизм бактериолитического действия лизоцима состоит в гидролизе связей между М-ацетилмурамовой кислотой и N-ацетилглюкозамином в полисахаридных цепях пептидогликанового слоя клеточной стенки бактерии. Это приводит к изменению ее проницаемости, сопровождающемуся диффузией клеточного содержимого в окружающую среду, и гибели клеток.
Интерферон оказывает иммуномодулирующий, пролиферативный эффект и вызывает в клетке, инфицированной вирусом, состояние противовирусной резистентности. β-лизины вырабатываются тромбоцитами и обладают бактерицидным действием. Трансферрин конкурирует с микроорганизмами за необходимые для них метаболиты, без которых возбудители не могут размножаться. Белок пропердин участвует в активации комплемента и других реакциях. Сывороточные ингибиторы крови, например р-ингибиторы (р-липопротеины), инактивируют многие вирусы в результате неспецифической блокады их поверхности. Отдельные гуморальные факторы (некоторые компоненты комплемента, фибронектин и др.) вместе с антителами взаимодействуют с поверхностью микроорганизмов, способствуя их фагоцитозу, играя роль опсонинов.
Неспецифический клеточный иммунитет обусловлен главным образом наличием в крови лейкоцитов и их фагоцитарной активностью. Способностью к фагоцитозу обладают гранулоциты, моноциты, тромбоциты и лимфоциты. Сильнее всего фагоцитарная активность выражена у моноцитов, которые содержат большое количество лизосомных ферментов, расщепляющих захваченные частицы.
Фагоцитоз – процесс, при котором поглощаются крупные частицы. У высших животных фагоцитоз осуществляется только специфическими клетками (нейтрофилами и макрофагами), которые происходят от одной общей клетки-предшественника и защищают животных и человека от инфекции, поглощая вторгшиеся микроорганизмы, а также утилизируют старые или поврежденные клетки или клеточные оболочки.
Среди макрофагов различают подвижные (циркулирующие) и неподвижные (оседлые) клетки. Подвижные макрофаги – это моноциты периферической крови, а неподвижные – макрофаги печени, селезенки, лимфатических узлов, выстилающие стенки мелких кровеносных сосудов и других органов и тканей.
Активность фагоцитов связана с наличием в сыворотке крови опсонинов. Опсонины – белки нормальной сыворотки крови, вступающие в соединение с микробами, благодаря чему последние становятся более доступными для фагоцитов.
Различают фагоцитоз завершенный (при котором происходит гибель фагоцитированных клеток) и незавершенный (гибель микроорганизмов внутри фагоцита не наступает).
В основе клеточного иммунитета лежит функционирование нескольких субпопуляций T-лимфоцитов, каждый из которых может иметь ту же антигенную специфичность, хотя функции каждой из этих субпопуляций различны.
Натуральные киллеры представляют собой популяцию лимфоцитов, лишенных признаков Т-лимфоцитов и В-лимфоцитов, и составляют до 15% лимфоцитов крови. Их участие в неспецифическом иммунном ответе состоит в способности оказывать прямое цитотоксическое действие на злокачественно- трансформированные и вирус-инфицированные клетки, а также клетки, поглотившие некоторые внутриклеточные бактериальные патогены.
В систему функционирования этих эффекторных T-клеток ( T-эффекторов ) входит:
1. Продуцирование T-хелперами разнообразных растворимых факторов ( лимфокинов ), стимулирующих B-клеточный ответ.
2. Воспалительный эффект. Лимфокины, продуцированные T-хелперами, индуцируют миграцию и активацию моноцитов и макрофагов, что вызывает острую воспалительную реакцию.
3. Пролиферация цитотоксических T-лимфоцитов. Цитотоксические T-лимфоциты сами по себе способны уничтожать другие клетки, прежде всего клетки, зараженные вирусом. При этом рецепторы цитотоксических T-лимфоцитов распознают поверхностные антигены на клетках-мишенях, но меньшей степени, чем антитела, способные распознавать разные штаммы вирусов, т.е. обладают меньшей специфичностью.
4. Если же некоторой части вирусов все же удается уйти из под контроля цитотоксических T-лимфоцитов в виде "раздетой" вирусной частицы в соседние клетки, то система клеточного иммунитета использует другой механизм их инактивации: T-хелперы, стимулированные вирусным антигеном, выделяют лимфокин гамма-интерферон, который придает соседним клеткам непермиссивность для репликации любого проникшего в них вируса. Гамма-интерферон может, кроме того, повышать неспецифическую цитотоксичность NK для зараженных клеток.
5. Регуляторные эффекты. T-супрессоры могут индуцировать супрессию иммунного ответа других эффекторных клеток.
Полностью разделить клеточный иммунитет и гуморальный невозможно: в инициации образования антител участвуют клетки, а в некоторых реакциях клеточного иммунитета важную связующую функцию выполняют антитела.
Наиболее полно изучен гуморальный компонент антиинфекционного иммунитета, однако при детальном исследовании практически при любой инфекции можно доказать значение клеточных факторов. Антитела не являются безразличными для клеточного иммунитета, в большинстве случаев они способствуют ему, а в отдельных случаях могут ослаблять развитие и интенсивность клеточного иммунитета. Перевод клеточного иммунитета на гуморальный ведет к обострению заболевания, защита от которых связана с клеточными факторами.
Неспецифические клеточные и гуморальные механизмы И., взаимодействуя и дополняя друг друга, обеспечивают раннюю и достаточно надежную защиту организма от разнообразных возбудителей. По мере развития инфекции, вызванной высоковирулентными микроорганизмами, неспецифические механизмы противоинфекционной защиты дополняются антиген-специфическими факторами иммунитета.
