
- •Нижегородская государственная медицинская академия
- •Содержание
- •Фенолы, хиноны и их производные как лекарственные препараты
- •Лекарственные вещества
- •Испытание на подлинность
- •Количественное определение фенолов
- •1. Методы галогенирования.
- •2. Метод ацетилирования.
- •3. Фотоколориметрический метод с использованием цветных реакций.
- •Производные нафтохинонов к-витаминного действия (противогеморрагического и коагуляционного)
- •Фитол широко распространен в природе, он содержится в растениях и составляет основную часть растворимого пигмента хлорофилла.
- •Производные пара-аминофенола
- •Парацетамол.
- •Количественное определение парацетомола
- •Ароматические кислоты и их производные
- •Получение
- •Производные фенолокислот
- •Амиды салициловой кислоты
- •Подлинность:
- •Чистота. Определяют примесь n-аминофенола в водном извлечении без предварительного гидролиза.
- •Производные n-аминобензойной кислоты.
- •Синтез амидов пабк
- •Производные орто-аминобензойной кислоты.
- •Лекарственные средства - производные арилалкиламина и оксифенилалкиламина
- •Очистка
- •Количественное определение
- •Адреномиметические вещества.
- •Производные замещенных гидроксипропаноламидов – бета-адреноблокаторы
- •Является наиболее эффективным препаратом этого ряда
- •Чистота
- •Количественное определение
- •Хранение. По списку б, в хорошо укупоренной таре, предохраняющей от действия света.
- •Хранение: По списку б, в хорошо укупоренной таре, предохраняющей от действия света.
- •Биохимические предпосылки получения лекарственных веществ в ряду фенилалкиламинов.
- •Нитрофенилалкиламины
- •Чистота
- •Количественное определение
- •Бензолсульфаниламиды и их производные
- •Сульфаниламидные препараты
- •Классификация по химическому строению
- •Получение
- •Литература
Сульфаниламидные препараты
Амид сульфаниловой кислоты впервые синтезирован в 1908 г. Гельмо. Однако его уникальные лечебные свойства были обнаружены спустя 27 лет. В 1935 году венгерский ученый Домагк исследовал на мышах действие красителя – пронтозила. Все мыши, получившие 10 смертельных доз культуры гемолитического стрептококка, после введения пронтозила остались живы, а все контрольные погибли.
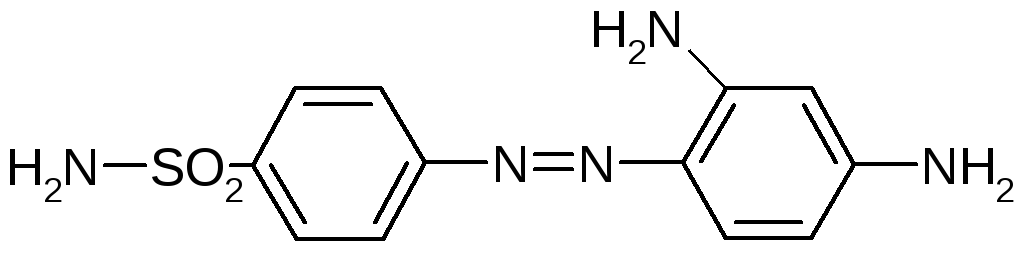
Пронтозил
В России первые работы выполнены в 1935 году под руководством профессоров Рубцова, Магидсона (ВНИХФИ) и Постовским (Свердловский филиал). Синтезирован красный стрептоцид:
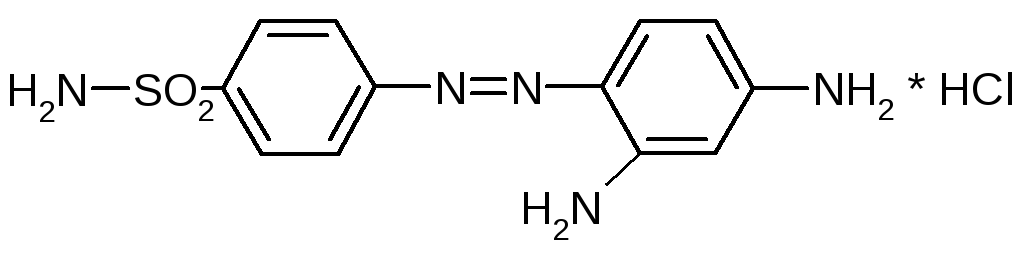
В организме животного красный стрептоцид расщепляется с образованием двух продуктов: сульфаниламида (1) и 1,2,4-триаминобензола (2), физиологически неактивного продукта.
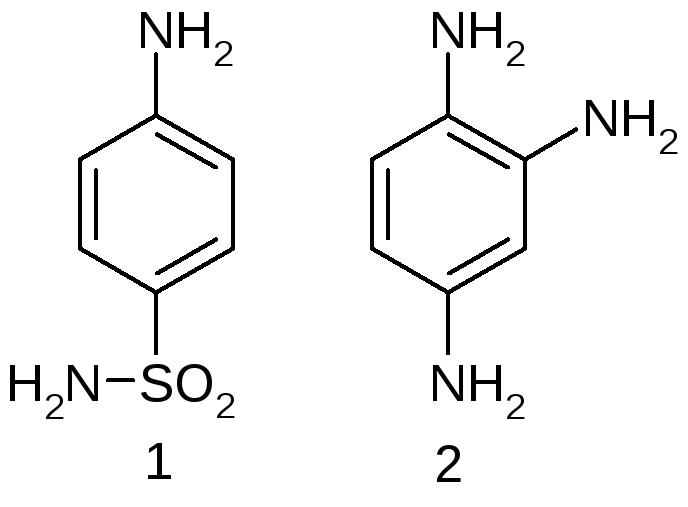
|
Стрептоцид белый |
|
В связи с этим в дальнейшем основное внимание направлено на синтез продукта расщепления (1) и его аналогам. Стрептоцид сократил смертность от многих заболеваний, в том числе менингита, газовой гангрены и др.
Этапы развития:
1935-1945 гг - бурное развитие синтетических работ.
1946-1956 гг - спад по синтезу (появление антибиотиков).
с 1960 года – разработка препаратов прологированного действия.
Классификация по химическому строению
Со свободной ароматической аминогруппой. Некоторые препараты используются в качестве солей, более легко растворимых в воде.

Водород в амидной группе подвижный и легко замещается на натрий.
1.1. Стрептоцид Streptocidum. Белый кристаллический порошок, без запаха;
Тпл.=164-167°С.

n-аминобензолсульфамид
1.2. Стрептоцид растворимый, Streptocidum solubile.Белый кристаллический порошок.

n-сульфамидобензоламинометан сульфат натрия
1.3. Сульфацил – натрий, Sulfacylum-natrium.

n-аминобензолсульфонилацетамид натрий гидрат
N`- ацетил(4-аминобензолсульфамидо)- натрия моногидрат
1.4. Норсульфазол, Norsulfazolum. Белый порошок с желтоватым оттенком; Тпл.=200-204°С.
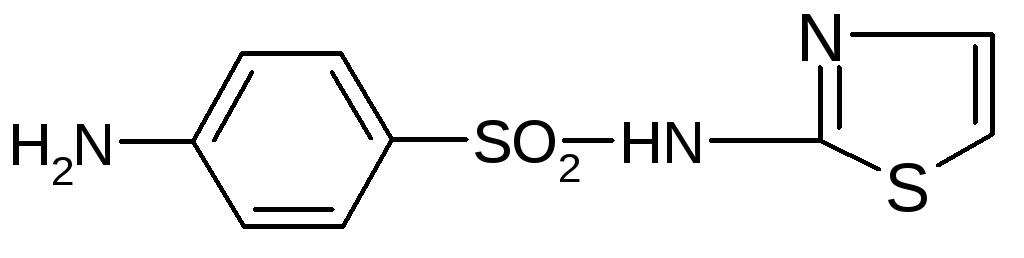
2-(n-аминобензолсульфамидо) - тиазол.
1.5. Сульфапиридазин, Sulfapyridazinum. Светло-желтые кристаллы, без запаха.

6- (n-аминобензолсульфамидо)-3-метоксипиридазин
1.6. Сульфадиметоксин, Sulfadimethoxinum. Белый кристаллический порошок, Тпл.=198-204°С.

6- (n-аминобензолсульфамидо)-2,4-диметоксипиперидин
1.7. Сульфален, Sulfalenum. Белый порошок; Тпл.=173-177°С.
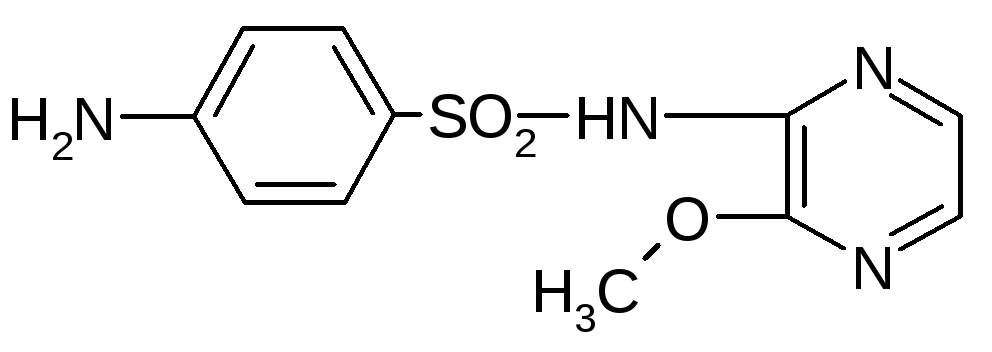
6- (n-аминобензолсульфамидо)-3-метоксипиразин
С заместителями в цикле и аминогруппе
2.1. Фталазол, Phthalazolum.
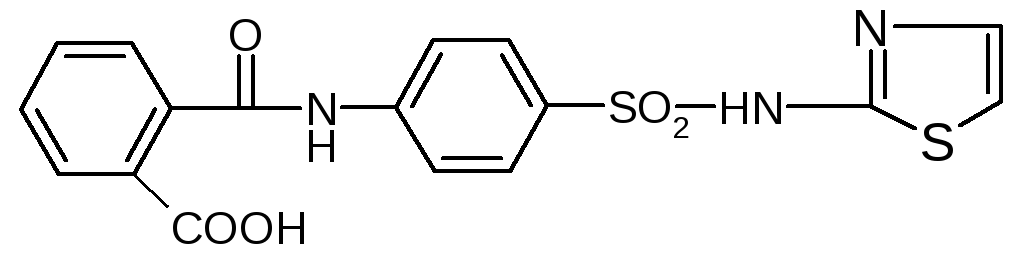
2-(n-фталиламинобензолсульфамидо) - тиазол = фталил - норсульфазол
Фтазин, Phthazinum. Тпл.=180°С.

6-(n-фталиламинобензолсульфамидо)-3-метоксипиридазин
Группа азокрасителей. Салазопиридазин, Salazopyridazinum.

5-(n-[N-(3-метоксипиридазинил-6)-сульфамидо]-фенилазо)-салициловая кислота
Связь строения с действием.
Для проявления противомикробной активности необходимо наличие 4- аминобензолсульфамидного радикала, -NH2 и -SO2NH2 должны находиться в пара-положении. В противоположенном случае антимикробная активность не проявляется.
Введение заместителей в аминогруппу позволяет получать препараты направленного действия (избирательного) – фталазол, салазопиридазин.
При замене ариламиногруппы на -СН3, -Cl и другие заместители характер действия меняется, и вместо антибактериального действия проявляется гипогликемическая активность.
Замена атома водорода в сульфамидной группе приводит к изменению характера действия, например, введение ацетильного радикала ускоряет действие препарата. Препараты с гетероциклическими радикалами оказывают более длительное действие. Продолжительность действия возрастает, если ввести электронодонорные заместители в гетероцикл (сульфален – сверхдлительное действие).
