
- •Нижегородская государственная медицинская академия
- •Содержание
- •Фенолы, хиноны и их производные как лекарственные препараты
- •Лекарственные вещества
- •Испытание на подлинность
- •Количественное определение фенолов
- •1. Методы галогенирования.
- •2. Метод ацетилирования.
- •3. Фотоколориметрический метод с использованием цветных реакций.
- •Производные нафтохинонов к-витаминного действия (противогеморрагического и коагуляционного)
- •Фитол широко распространен в природе, он содержится в растениях и составляет основную часть растворимого пигмента хлорофилла.
- •Производные пара-аминофенола
- •Парацетамол.
- •Количественное определение парацетомола
- •Ароматические кислоты и их производные
- •Получение
- •Производные фенолокислот
- •Амиды салициловой кислоты
- •Подлинность:
- •Чистота. Определяют примесь n-аминофенола в водном извлечении без предварительного гидролиза.
- •Производные n-аминобензойной кислоты.
- •Синтез амидов пабк
- •Производные орто-аминобензойной кислоты.
- •Лекарственные средства - производные арилалкиламина и оксифенилалкиламина
- •Очистка
- •Количественное определение
- •Адреномиметические вещества.
- •Производные замещенных гидроксипропаноламидов – бета-адреноблокаторы
- •Является наиболее эффективным препаратом этого ряда
- •Чистота
- •Количественное определение
- •Хранение. По списку б, в хорошо укупоренной таре, предохраняющей от действия света.
- •Хранение: По списку б, в хорошо укупоренной таре, предохраняющей от действия света.
- •Биохимические предпосылки получения лекарственных веществ в ряду фенилалкиламинов.
- •Нитрофенилалкиламины
- •Чистота
- •Количественное определение
- •Бензолсульфаниламиды и их производные
- •Сульфаниламидные препараты
- •Классификация по химическому строению
- •Получение
- •Литература
Нитрофенилалкиламины
Хлорамфеникол (левомицетин) – антибиотик ароматического ряда, его эфиры - стеарат и сукцинат.
Природный ароматический антибиотик хлорамфеникол продуцируется почвенным актиномицетом Actinomyces venezuelae. Штамм этого продуцента был впервые выделен из почв Венесуэлы (1947), откуда он и получил свое название.
Хлорамфеникол – антибиотик широкого спектра действия. Он действует не только на грамположительные и грамотрицательные бактерии, но и на риккетсии, вызывающие брюшной и сыпной тифы, бруцеллез, холеру и др.
Такой широкий диапазон действия антибиотика привлек к нему большое внимание исследователей, и в течение двух лет было не только изучено его химическое строение, но и осуществлен синтез (США, 1949). Почти одновременно в нашей стране академик М.М.Шемякин с группой сотрудников провел большую работу по синтезу аналогов хлорамфеникола и изучению связи между его строением и антибиотическим действием. При этом оказалось, что биологическая активность хлораминофеникола находится в большой зависимости от пространственной конфигурации молекулы.
Хлорамфеникол относится к производным n-замещенных нитробензолов.

При гидролизе хлорамфеникола получается соединение, содержащее аминогруппу – основание хлорамфеникола (1) и дихлоруксуная кислота (2).
1 2

При конденсации полученных продуктов получается хлорамфеникол (3), молекулу которого можно представить следующим образом:

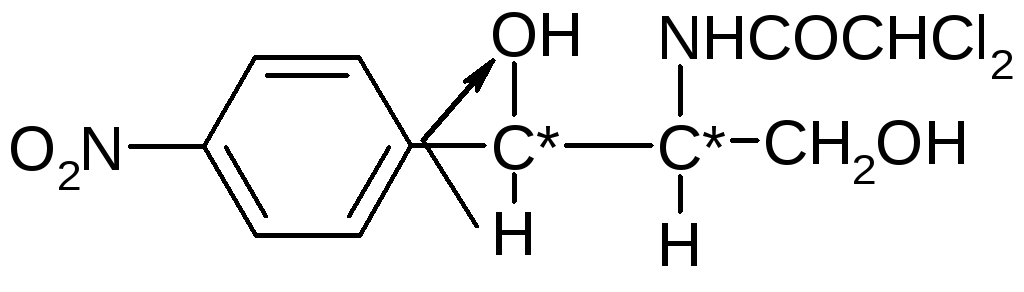
Д(-)-трео-1-(4-нитрофенил)-2-дихлорацетил-аминопропандиол-1,3.
Хлорамфеникол имеет 2 ассиметричных атома углерода, поэтому возможно существование 4 стереоизомеров или 2-х пар антиподов:
Трео-изомер (транс-положение групп): Д(+); Д(-); L(+); L(-), Д(-)-левомицетин, остальные токсичны.

2. Эритро-изомеры (цис-расположение): Д(+); Д(-); L(+); L(-). Оба изомера Д(+); Д(-) и L(+); L(-) – очень токсичны.
Синтез:
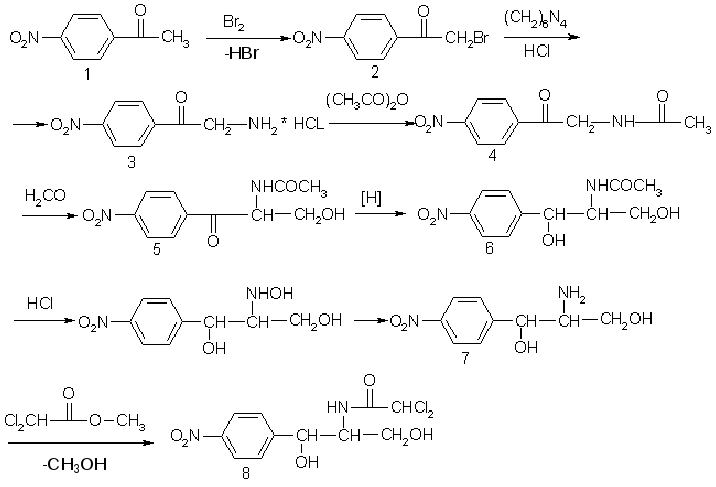
1) n-нитроацетофенон.
2) n-нитро-α-бромацетофенон.
3) n-нитро-α-аминоацетофенона гидрохлорид.
4) n-нитро-α-ацетиламиноацетофенон.
5) n-нитро-α-ацетиламино-β-оксипропиофенон.
6) Д,L-трео-1-n-нитрофенил-2-ацетилацетилпропандиол-1,3.
7) Д,L-трео-1-n-нитрофенил-2-ацетиламинопропандиол-1,3.
8) левомицетин
В реакции 7-8 участвует Д-(-)-трео-изомер, который получается при разделении на оптические антиподы Д,L-трео1-n-нитрофенил-2-ацетиламинопропандиола-1,3.
Смесь Д-(-) трео-изомера (левовращающего) левомицетина и L-(+) - трео-изомера (правовращающего антипода) левомицетина называется синтомицином и используется для наружного применения в виде мазей, линиментов как антибактериальное средство (50% биологической активности).
Медицинские препараты:
1. Левомицетин – Laevomycetinum
Тпл.=149-153°; [α]Д=+18 до +21° 15% раствор в спирте.
Беловато-желтоватый, иногда с зеленым оттенком порошок. Вкус горький, мало растворим в воде, эфире, хлороформе, легко растворим в спирте.
2. Левомицетина стеарат – Laevomycetini stearas

Д-(-)-трео-1-нитрофенил-2-дихлорацетиламинопропандиола-1,3-3-стеарат
Тпл.=88-90°С;[α]Д= +15 до +20° в 5% раствор в спирте.
Трудно растворим в эфире, спирте, воде, легко в хлороформе.
3.Левомицетина сукцинат растворимый – Laevomycetini succinas solubile
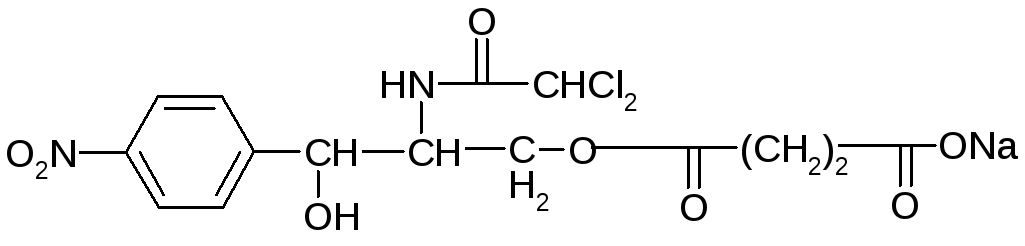
Д-(-)-трео-1-нитрофенил-2-дихлорацетил-аминопропандиол-1,3-3-сукцинат натрия.
[α]Д= -11 до -12,6°(10% раствор в смеси метанола, воды и HCl)
Не растворим в хлороформе, легко растворим в воде.
Препараты различаются по растворимости, удельному вращению, по температуре плавления, по УФ-спектрам:
Левомицетин – λмах.= 278нм.
Левомицетина стеарат - λмах.= 272нм.
Левомицетина сукцинат - λмах.= 275нм.
Физические свойства можно использовать при идентификации.
Химические свойства.
Обусловлены наличием следующих функциональных групп: ароматическая нитрогруппа, сложноэфирная группа, первичная и вторичная аминогруппы, вторичная амидная группа, ковалентно связанный хлор.
Реакции идентификации.
Гидролиз в щелочной среде (НТД)
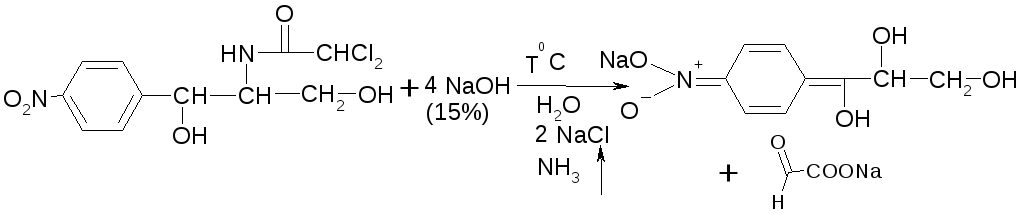
Образуется желтое окрашивание, переходящее в красно-кирпичный осадок, аци-формы n-нитрофенилпропандиола-1,3, выделяется аммиак, который обнаруживают по запаху. Cl- устанавливают по реакции с AgNO3 в HNO3.
При дальнейшем нагревании:
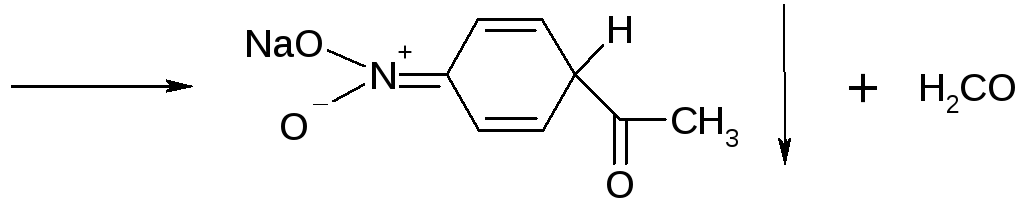
Реакция на ароматическую нитрогруппу
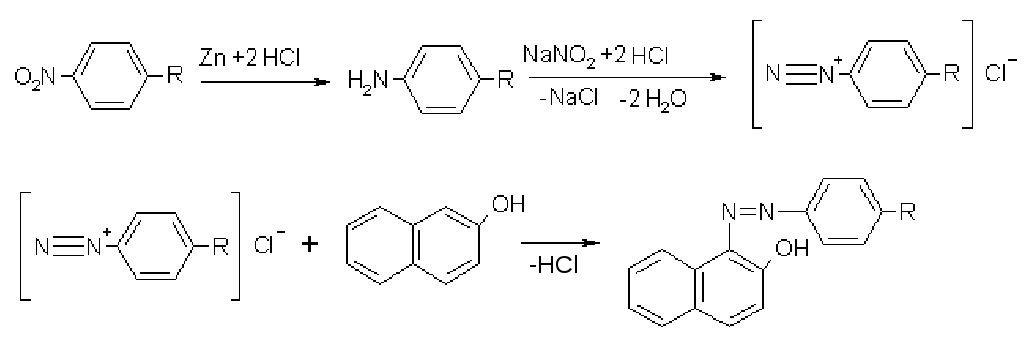
Нитрогруппу восстанавливают порошкообразным цинком в соляной кислоте до первичной аминогруппы, которую затем диазотируют нитритом натрия в кислой среде. Далее с образующейся солью диазония проводят реакцию азосочетания с β-нафтолом в щелочной среде. Образуется красный осадок или раствор.
Реакция комплексообразования с раствором CuSO4 (реакция на гидроксильный спиртовой радикал). Спиртовой бутанольный слой окрашивается в интенсивный сине-фиолетовый цвет.
Реакция гидролиза на сложноэфирную группу (левомицетина стеарат).
После кислотного гидролиза с соляной кислотой выделяются масляные капли стеариновой кислоты, которые при комнатной температуре застывают в виде дробинок.
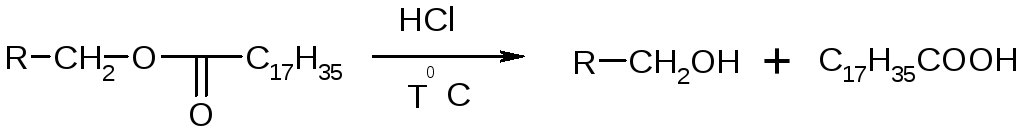
стеариновая кислота
В щелочной среде реакцию не проводят – образуется мыло.
Левомицетина сукцинат доказывают по реакции с серной кислотой в присутствии резорцина (мета-диоксибензола).
Препарат нагревают до появления красно–кирпичного окрашивания, разбавляют водой и раствор подщелачивают. Получают оранжевый раствор с интенсивной флюоресценцией (доказывают янтарную кислоту).

янтарная кислота
янтарный ангидрид
комплекс красно-коричневого цвета.
динатривая соль β-пропионовой кислоты- интенсивное окрашивание.
