
- •Український державний хіміко-технологічний університет
- •2. Математична модель в системі управління
- •2.1. Головні поняття технічної кібернетики
- •2.2.1. Загальні характеристики інформації.
- •2.2.2. Інформаційні процеси
- •2.3.1. Загальні поняття та терміни
- •2.3.2. Графічне відображення оптимізації
- •Var de:text;
- •I,Imin,Imax,dI,р,рc,eps,u,u0 :real;
- •2: Writeln(de); writeln (de, k:3,' I-u-р-dI',I:6:2, u:6:2, р:6:2, dI:10:5);
- •3.3.Масообмінні процеси в системах промивання в гальванотехніці
- •3. Математичне моделювання технологічних процесів в електрохімічних апаратах
- •3.1. Масообмінні процеси в електрохімічних апаратах.
- •3.2 Електрохімічні апарати ідеального змішування
- •3.2.1. Загальна математична модель нестаціонарного масообміну в еха.
- •3.2.2. Математична модель нестаціонарних процесів в непроточних еха ідеального змішування
- •3.2.3. Алгоритми та програма числового моделювання масообміну в еха ідеального змішування.
- •1 Real I,ma,mb,j1,j2
- •2 Data aa,ab,ea,eb,eg,et,t,dt/0.7,0.98,2.18,1.49,0,0,0,0.1/
- •3 Data camin, cbmax, I , ca , cb , V , v0 , j1 , ca1 , cb1
- •23 If(ca.Le.Camin.Or.Cb.Ge.Cbmax) goto 3
- •3.3. Математична модель стаціонарних процесів в проточних еха ідеального змішування
- •1 Real I, j1,j2
- •3.4 Процеси в електрохімічних апаратах ідеального витискування.
- •Var Rom, pR,pO,kap,tok,u,Ut,co,cr,ir,V,h,er,eo,l,dx :real;
- •4. Нестаціонарний масообмін в приелектродному шарі
- •5.5. Моделювання розсіюючої здатності електроліту
- •5. Електричні поля в електрохімічних системах
- •5.1. Двовимірне електричне поле.
- •5.4. Приклади дії електричних полів в системах технічної електрохімії і способи управління полями.
- •6. Моделювання процесів в пористих системах
- •6.1. Об’єкти вивчення
- •6.2. Електричне поле в рідинному пе.
- •6.3. Стаціонарний процес в ріднному пористому електроді. Концентраційні поля.
- •6.4. Стаціонарні транспортні процеси в пористих сепараторах
- •7.Витоки струму в високовольтних електрохімічних пристроях
6.4. Стаціонарні транспортні процеси в пористих сепараторах
В технології широко використовують пористі сепаратори, які відокремлюють електроліти катодних і анодних камер і тим запобігають їх прямому змішуванню. Але через електроліт в поровому просторі сепаратор пропускає струм, фільтраційні і дифузійні потоки, лише частково гальмуючи їх. В стаціонарному режимі роботи електролізера внаслідок руху компонентів з однієї камери в іншу в сепараторі встановлюються деякі стаціонарні концентраційні профілі С(х) всіх компонентів.
Схема розташування сепаратора показана на рис. 6.6
Рис.
6.6. Схема роботи сепаратора. 1,2 – лівий
електрод і електродна камера, 3,4- правий
електрод і електродна камера, 5- сепаратор,
А,К- початкові (дифузійні) профілі
концентрацій
аніона та катіона. Стрілками вказані
знаки напрямків потоків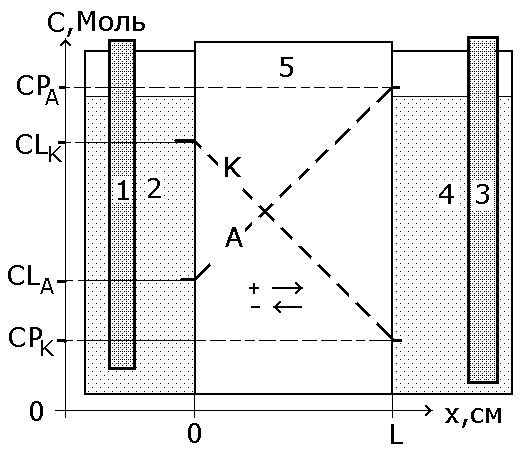
І в пористому електроді і в сепараторі закономірності переносу повністю ідентичні. Різниця полягає лише в тому, що в пористому сепараторі на внутрішній поверхні ніяка реакція не здійснюється. Тому потоки кожного компонента на обох поверхнях сепаратора однакові, а в рівнянні переносу (6.17) в правій частині має бути нуль:
![]() (6.26)
(6.26)
причому
тут градієнт потенціалу
![]() є просто параметр, який визначається
величиною густини струму і ефективною
електро-провідністю розчину в порах.
Густина струму в напрямі 0х постійна
величина, а питома електропровідність
змінюється уздовж координати, бо
змінюються концентрації компонентів
внаслідок переносу.
є просто параметр, який визначається
величиною густини струму і ефективною
електро-провідністю розчину в порах.
Густина струму в напрямі 0х постійна
величина, а питома електропровідність
змінюється уздовж координати, бо
змінюються концентрації компонентів
внаслідок переносу.
Математична модель і алгоритм. В сепараторі внаслідок одночасної дії на іонні компоненти електроліту закону електронейтральності і трьох механізмів переносу - міграції, дифузії та фільтрації, виникають складні нелінійні концентраційні профілі С(х), такі, що три складові частини швидкості кожного іона змінюються вдовж координати “х”, але в будь-якому перетині “х” його сумарний потік залишається незмінним. Підрахувати їх (а також потоки нейтральних речовин в молекулярній формі) за простими аналітичними формулами можна лише в окремих часткових випадках.Числовим моделюванням можна знайти точне рішення.
Рішення знаходять в N точках по товщині сепаратора. Iтераційним методом вирішується система рівнянь переносу (6.26) для всіх компонентів механізмами дифузії, фільтрації та міграції. Рівняння (6.26) переводять в дискретну (різницеву) форму, вирішують відносно концентрації у вузлі n і одержують спільну ітераційну формулу :
![]() ,
(6.27)
,
(6.27)
де С-концентрація компонента, z- його зарядове число (знак «+» або «-»), v=DzF/RT - рухомість іона (см/с), dU/dx=i/–градієнт потенціалу в електроліті в порах, - питома електропровідність розчину в точці 0<x<L, =L/(N-1) - крок дискретизації (dx), N- кількість точок по координаті “х”. Параметри jF , є спільними, а z,v – індивідуальні для кожного іона.
Складовою частиною системи рівнянь є рівняння електронейтральності (6.24), яке означає рівність сумарних концентрацій аніонів і катіонів в будь-якій точці координати «х» (в перетині сепаратора площиною, паралельною його зовнішній габаритній поверхні).
Граничні умови - задані концентрації всіх компонентів в правій (Р) та лівій (L) камерах.
Залежність питомої електропровідності електроліту від сумарної іонної концентрації CS можна використати як апроксимаційний поліном другого ступеню (парабола) з трьома коефіцієнтами а1,а2,а3:
![]() .
(6.28)
.
(6.28)
Послідовність обчислювальних операцій така ж, як в інших алгоритмах.
1. Задають початкові довільні функції розподілу по глибині електроду локальних значень концентрацій всіх компонентів.
2. Далі всі розрахунки виконують в ітераційному циклі:
А-
За формулами (6.26) підраховують функції
розподілу концентрацій компонентів
у вузлах 2..
N-1,
![]() .
Значення в першому і останньому вузлах
задані
.
Значення в першому і останньому вузлах
задані
Б-
Визначають сумарну концентрацію зарядів
![]() ,
і якщо вона не нульова, коректують
індивідуальні концентрації іонів, як
було показано в п.6.3.
,
і якщо вона не нульова, коректують
індивідуальні концентрації іонів, як
було показано в п.6.3.
В- Визначають потоки gi окремих компонентів за виразом в квадратних дужках в (6.26). Для контролю можна визначати цей параметр, наприклад, в різних точках осв 0х – на лівій та на правій межі, в середині. Ці величини для кожного іона повинні бути однаковими.
Г- Перевіряють якість сходження ітерацій, порівнюючи між собою на двох сусідніх ітераціях наприклад, або всі, або окремі значення іонних потоків або концентрацій. Якщо сходження досягнуто і функція співпадає з визначеною кроком раніше, процес припиняють.
Кінцевим результатом рішення є функції розподілу концентрацій по товщині сепаратора С(х) для всіх компонентів реакції а також їх потоки через сепаратор з однієї камери в протилежну.
На
рисунку 6.7 наведено приклад розрахованих
концентраційних профілів в електроліті![]() ,
який містить чотири види іонів різних
знаків(
нумерація
кривих 1-H+,
2-Cu2+
, 3-Zn2+,
4-SO42-).
В правій електродній камері (катод
Cu0/Cu2+
елемента Даніеля-Якобі) міститься розчин
,
який містить чотири види іонів різних
знаків(
нумерація
кривих 1-H+,
2-Cu2+
, 3-Zn2+,
4-SO42-).
В правій електродній камері (катод
Cu0/Cu2+
елемента Даніеля-Якобі) міститься розчин
![]() ,
в лівій (анодZn0/Zn2+)
-
,
в лівій (анодZn0/Zn2+)
-![]() .
Напрямок руху катіонів в сепараторі –
зліва направо, він визначений напрямком
струму при розряді елемента.
.
Напрямок руху катіонів в сепараторі –
зліва направо, він визначений напрямком
струму при розряді елемента.
Рис.6.7.
Концентраційні профілі чотирьох видів
іонів 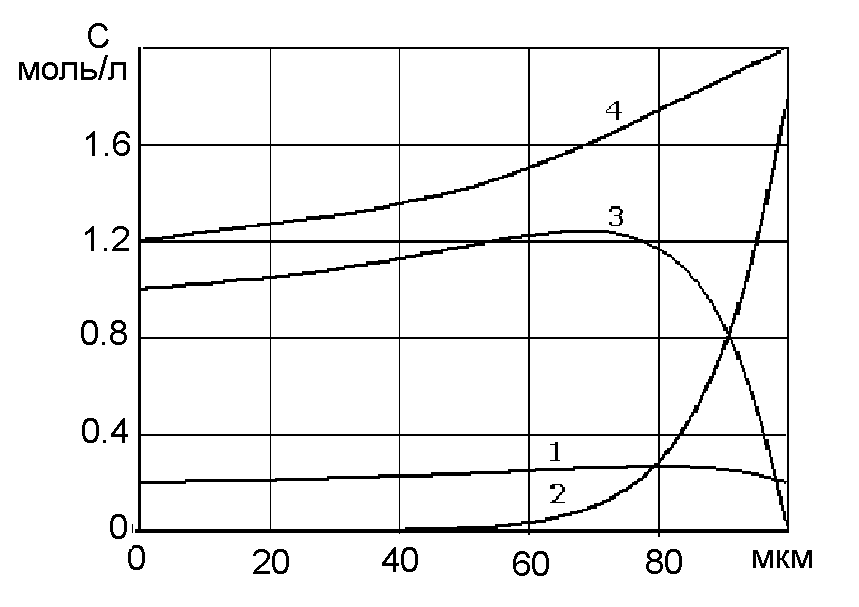
З форми профілю кривої 2 (Cu2+) видно, що справа існує досить сильний дифузійний потік іонів Cu2+ в сепаратор через великий градієнт концентрації. Але він повністю компенсується зустрічним міграційним потоком, тому в даному випадку іони міді в ліву (анодну) камеру не проникають – це видно з того, що в лівій частині концентрація іонів Cu2+ практично нульова.
