
- •П.А. Киселев, с.Б. Бокуть курс лекций по физической химии
- •Введение
- •Лекция 1. Газовые законы
- •1.1. Температура и нулевой закон термодинамики
- •1.2. Законы поведения идеальных газов: уравнение состояния идеального газа
- •1.3. Кинетическое уравнение газов
- •1.4. Уравнение состояния реальных (неидеальных) газов. Уравнение Ван-дер-Ваальса
- •1.5. Закон парциальных давлений Дальтона
- •Лекция 2. Первое начало термодинамики и термохимия
- •2.1. Вводная часть
- •2.2. Некоторые понятия, используемые в термодинамике
- •2.3. Формулировка первого начала термодинамики
- •2.4. Применение первого начала термодинамики к различным процессам
- •2.5. Теплота химической реакции (общие положения)
- •2.6. Закон Гесса
- •2.7. Следствие из закона Гесса
- •Лекция 3. Второе начало термодинамики и его применение
- •3.1. Основной смысл и значение второго закона термодинамики
- •3.2. Обратимые и необратимые процессы
- •3.3. Формулировка и математическое выражение второго начала термодинамики
- •3.4. Изменение энтропии изолированной системы
- •3.5. Статистическая природа второго начала термодинамики
- •Лекция 4. Третье начало термодинамики. Расчеты изменения энтропии при различных процессах
- •4.1. Формулировка третьего начала термодинамики
- •4.2. Абсолютные и стандартные значения энтропии
- •4.3. Расчеты изменения энтропии в различных процессах
- •1. Расчеты изменения энтропии при изотермических процессах
- •2. Расчет изменения энтропии в неизотермических процессах
- •3. Расчет изменения энтропии сложного процесса
- •4.4. Расчет изменения энтропии при протекании химического процесса
- •4.5. Критерии направления протекания процессов и достижения равновесных состояний в открытых и закрытых системах. Понятие об энергии Гиббса
- •Лекция 5. Химические реакции как открытые в термодинамическом смысле системы. Направление протекания химических реакций. Равновесные химические реакции
- •5.1. Понятие о химическом потенциале
- •5.2. Экзергонические и эндергонические реакции
- •5.3. Взаимосвязь энтальпийного и энтропийного факторов в качестве критерия самопроизвольного протекания химической реакции
- •5.4. Понятие о равновесии химической реакции. Обратимые и необратимые реакции
- •5.5. Уравнение изотермы химической реакции и вывод закона действующих масс
- •5.6. Зависимость константы химического равновесия от температуры
- •Лекция 6. Химическое равновесие в гетерогенных и гомогенных системах
- •6.1. Взаимосвязь химического потенциала с другими термодинамическими функциями
- •6.2. Летучесть
- •6.3. Идеальный раствор
- •6.4. Фазовая диаграмма содержит зоны, линии и тройную точку
- •6.5. Уравнение Клаузиуса-Клапейрона
- •6.6. Коллигативные свойства растворов
- •6.7. Понижение точки замерзания и повышение точки кипения растворов
- •6.8. Осмотическое давление
- •6.9. Растворы электролитов
- •Лекция 7. Растворы электролитов
- •7.1. Общие сведения о теории электролитической диссоциации
- •7.2. Сильные и слабые электролиты
- •7.3. Закон разведения
- •7.4. Сильные электролиты
- •7.5. Ионная сила
- •7.6. Произведение растворимости
- •7.7. Электролитическая диссоциация воды
- •7.8. Концентрация водородных ионов
- •7.9. Буферные растворы
- •7.10. Механизм действия буферных растворов
- •7.11. Буферная емкость
- •Лекция 8. Основные понятия химической кинетики
- •8.1. Химическая реакция
- •8.2. Механизм химической реакции
- •8.3. Исходные, конечные и промежуточные вещества
- •8.4. Глубина превращения реакции
- •8.5. Гомогенные и гетерогенные реакции
- •8.6. Скорость химической реакции
- •8.7. Измерение скорости реакции
- •8.8. Порядок реакции и константа скорости реакции
- •8.9. Молекулярность реакции
- •8.10. Количественные соотношения между скоростью реакции и концентрацией реагента
- •8.11. Реакция второго порядка
- •8.12. Уравнение скорости реакции третьего порядка
- •8.13. Уравнение скорости реакции нулевого порядка
- •8.14. Определение порядка реакции
- •8.15. Теоретические основы химической кинетики
- •8.15.1. Теория активных соударений
- •8.15.2. Теория активированного (переходного) комплекса (переходного состояния)
- •8.15.3. Вывод основного уравнения теории переходного состояния
- •8.15.4. Термодинамическая форма основного уравнения теории переходного состояния
- •8.15.5. Сравнение термодинамической формы основного уравнения теории переходного состояния с уравнением Аррениуса
- •Лекция 9. Основы кинетики и механизма ферментативных реакций. Гомогенный и гетерогенный катализ
- •9.1. Понятие катализа
- •9.2. Основы теории гомогенного катализа
- •9.3. Основы теории гетерогенного катализа
- •9.4. Ферменты как биологические катализаторы
- •9.5. Кинетика реакций, катализируемых ферментами
- •9.6. Физический смысл величин Km и Vmax
- •9.7. Уравнение Михаэлиса-Ментен и ферментативные механизмы
- •9.8. Общее уравнение скорости
- •Лекция 10. Электрохимия
- •10.1. Введение в электрохимию
- •10.2. Термодинамика электрохимических систем
- •10.3. Электродный потенциал
- •10.4. Двойной электрический слой на границе между металлом и раствором электролита
- •10.5. Зависимость плотности заряда от концентрации электролита
- •Лекция 11.Электродные и безэлектродные электрохимические системы
- •11.1. Правила записи эдс и электродных потенциалов электрохимических систем
- •11.2. Типы электродов
- •11.3. Диффузионный и межжидкостный потенциалы
- •На электродах протекают реакции
- •11.5. Концентрационные цепи
- •Лекция 12. Поверхностные явления и адсорбция
- •12.1. Общая характеристика поверхностных явлений
- •12.2. Поверхностные явления в дисперсных системах
- •12.3. Поверхностное натяжение и природа вещества
- •12.4. Термодинамика поверхностных явлений в однокомпонентных системах
- •12.5. Равновесие фаз при искривленной поверхности раздела. Капиллярность
- •12.6. Уравнение Томсона
- •12.7. Капиллярные явления
- •Лекция 13. Адсорбция
- •13.1. Уравнение адсорбции Гиббса
- •13.2. Обзор сорбционных явлений
- •13.3. Природа адсорбционного взаимодействия
- •13.4. Термическое уравнение адсорбции. Изотерма адсорбции
- •13.5. Мономолекулярная адсорбция и изотерма Ленгмюра
- •Литература
- •Содержание
10.4. Двойной электрический слой на границе между металлом и раствором электролита
Процессы электрохимического окисления и восстановления связаны с переносом электрона через поверхностный слой на границе между металлическим электродом и раствором, т.е. через двойной электрический слой.
Образующийся двойной слой подобен плоскому конденсатору, расстояние между обкладками которого определяется величиной радиуса ионов. такая упрощенная картина, предложенная Г. Гельмгольцем, справедлива только при больших концентрациях растворов электролитов и больших величинах плотности заряда электрода. В большинстве реализуемых случаев строение двойного слоя отличается от описанного.
В результате электростатического притяжения ионов заряженной поверхностью, с одной стороны, и хаотического теплового движения молекул, под влиянием которого ионы стремятся равномерно распределиться в растворе, – с другой, ионная обкладка приобретает диффузное строение. Концентрация ионов, несущих заряд, противоположный заряду поверхности металла, уменьшается по мере удаления от поверхности, а концентрация ионов, имеющих заряд, одинаковый по знаку с зарядом металла, возрастает по мере удаления от поверхности (рис. 10.1).

Рис. 10.1. образующийся двойной слой можно подразделить на плотную часть (слой Гельмгольца), образуемый ионами, прилегающими непосредственно к поверхности металла, и диффузную часть (диффузный слой)
образующийся двойной слой можно подразделить на плотную часть (слой Гельмгольца), образуемый ионами, прилегающими непосредственно к поверхности металла, и диффузную часть (диффузный слой).
В растворах электролитов толщина диффузного слоя составляет несколько нанометров (или доли нанометра). В разбавленных электролитах она может быть существенно больше, а в чистой воде достигает 1000 нм. Плотный двойной слой можно описать уравнением плоского конденсатора
![]() , (10.18)
, (10.18)
где
![]() – емкость, относится к 1 см2поверхности;
– емкость, относится к 1 см2поверхности;
![]() – разность потенциалов между металлом
и раствором;
– разность потенциалов между металлом
и раствором;
![]() – диэлектрическая проницаемость;
– диэлектрическая проницаемость;
![]() – плотность заряда;
– плотность заряда;![]()
![]() – толщина плотной части двойного слоя.
– толщина плотной части двойного слоя.
Величина поверхностного
натяжения на границе металл – раствор
изменяется при наложении потенциала.
Это позволяет определять емкость
двойного слоя по изменению зависимости
поверхностного натяжения
![]() на границе металл – раствор от потенциала.
Кривая, описывающая указанную зависимость,
называется электрокапиллярной кривой
(рис. 10.2).
на границе металл – раствор от потенциала.
Кривая, описывающая указанную зависимость,
называется электрокапиллярной кривой
(рис. 10.2).

Рис. 10.2. Электрокапиллярная кривая. Область А – двойной слой из анионов; область В – двойной слой из катионов
Дифференциальное уравнение электрокапиллярной кривой, построенное термодинамическим путем, имеет вид
![]() . (10.19)
. (10.19)
Продифференцировав
уравнение (10.19) по
![]() ,
найдем:
,
найдем:
![]() . (10.20)
. (10.20)
Таким образом, дифференциальная емкость равна второй производной поверхностного натяжения по потенциалу, взятой с обратным знаком.
10.5. Зависимость плотности заряда от концентрации электролита
Впервые количественные
расчеты зависимости плотности заряда
от концентрации электролита в растворе
и потенциале электрода, учитывающие
диффузный характер двойного слоя, были
выполнены Ж. Гуи. Заметим, что общая
толщина двойного слоя
![]() ,
где
,
где
![]() – толщина плотной части двойного слоя,
а
– толщина плотной части двойного слоя,
а
![]() – толщина диффузной части. При больших
концентрациях электролита
– толщина диффузной части. При больших
концентрациях электролита
![]() и
и
![]() .
Толщина диффузной части двойного слоя
возрастает с уменьшением концентрации
электролита и повышением температуры.
При равных температуре и концентрации
толщина диффузной части тем больше, чем
меньший заряд несут ионы, концентрирующиеся
в двойном слое.
.
Толщина диффузной части двойного слоя
возрастает с уменьшением концентрации
электролита и повышением температуры.
При равных температуре и концентрации
толщина диффузной части тем больше, чем
меньший заряд несут ионы, концентрирующиеся
в двойном слое.
Диффузную часть двойного слоя принято называть слоем Гуи. В своих расчетах Ж. Гуи рассматривал ионы как точечные заряды. Позднее было показано, что такое представление совершенно неприменимо для плотной части двойного слоя, так как центр иона не может подойти к поверхности металла на расстояние меньшее, чем его радиус. Отсюда, в частности, вытекает, что в плотном слое потенциал изменяется линейно с расстоянием и, следовательно, градиент потенциала в этом слое сохраняет постоянную величину (где – изменение потенциала в двойном слое).
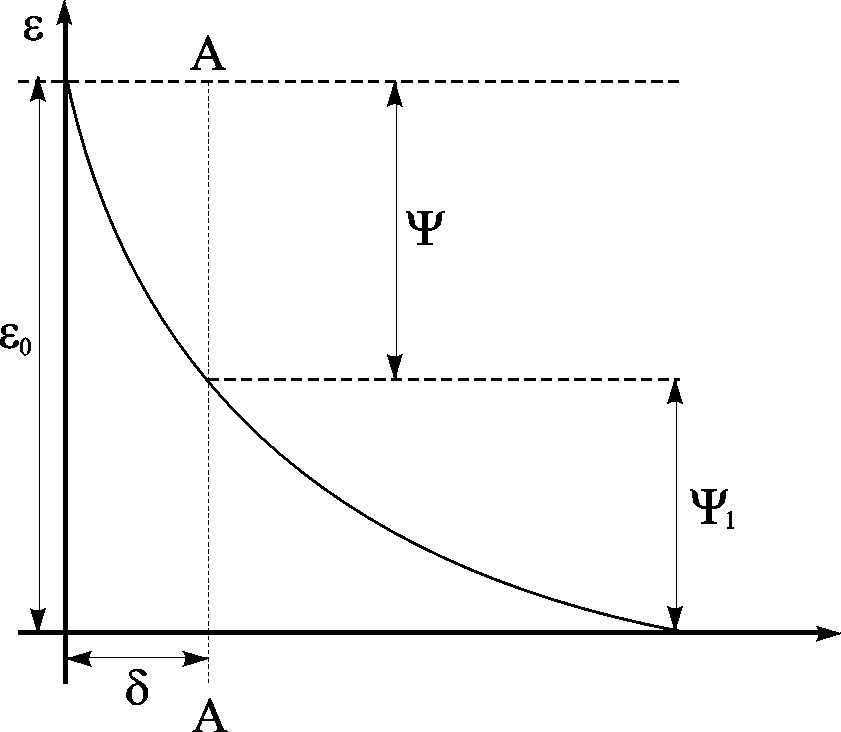
Рис. 10.3. Изменение потенциала в плотной и диффузной частях двойного слоя. Линия АА – граница между плотным и диффузным слоем
Изменение 1(потенциала) в диффузном слое происходит по некоторой кривой. Это изменение представляет собой разность потенциалов между границей плотной части двойного слоя АА и точкой в растворе, в которой концентрацияСа=Ск. Общая разность потенциалов между металлом электролитом° равна° =+1 (рис.10.3).
