
- •12. Азот и фосфор
- •5.1. Общая характеристика. Нахождение в природе. Получение
- •5.2. Простые вещества
- •5.2.1. Структура и физические свойства
- •5.2.2. Химические свойства
- •5.3. Аммиак и соли аммония
- •5.3.1. Получение аммиака
- •5.3.2. Физические и химические свойства
- •5.3.3. Соли аммония
- •5.4. Оксиды и гидроксиды азота. Соли
- •5.4.1. Получение оксидов и кислот
- •5.4.2. Свойства и применение
- •5.4.3. Нитраты и нитриты
- •5.5. Кислородосодержащие соединения фосфора
- •5.6. Минеральные удобрения
- •14. Общая характеристика. Степени окисления
- •7.3.2. Природные соединения алюминия
- •7.3.3. Физические свойства
- •7.3.4. Химические свойства
- •7.3.5. Оксиды и соли p-элементов
- •7.3.6. Производство алюминия
- •16. Углерод и кремний
- •6.1. Общая характеристика. Нахождение в природе. Получение
- •6.2. Структура и физические свойства простых веществ
- •17. Константа равновесия
- •2.3.2. Сдвиг равновесия
- •19. Строение атома и химическая связь
- •3.1. Электронное строение атома
- •3.1.1. Современная модель атома
- •20. Общая характеристика
- •Получение и свойства s-металлов
- •7.2.4. Сложные вещества s-элементов. Производство соды
- •2.1.1. Термохимия
- •2.1.2. Энтропия. Энергия гиббса
- •2.1.3. Формула гиббса. Разрешенность процессов с позиции термодинамики
- •22. Метан
- •6.5. Кислородосодержащие соединения углерода
- •6.5.1. Общая характеристика и свойства
- •6.6.3. Цемент
- •25. Ионное произведение воды. Водородный показатель. Индикаторы
- •4.2.4. Буферные растворы
- •3.2. Получение простых веществ.
- •3.3. Физические свойства г2
- •27. Кислородосодержащие соединения хлора
- •Взаимодействие г2 с водородом. Получение hCl и ее свойства. Галогеноводородные кислоты
- •32. Соли аммония
- •5.4. Оксиды и гидроксиды азота. Соли
- •5.4.1. Получение оксидов и кислот
- •5.4.2. Свойства и применение
- •2.1. Распространенность водорода
- •2.2. Сходство водорода с другими элементами
- •2.2.1. Сходство с галогенами
- •2.2.2. Сходство со щелочными металлами
- •40. Особенности водорода
- •2.2.2. Кинетическое уравнение
- •2.2.3. Механизм химических реакций
- •2.2.4. Влияние температуры на скорость
- •2.2.5. Катализ
2.2.5. Катализ
Катализаторами
называют вещества, которые,
не расходуясь
в ходе процесса, ускоряют
его, ибо они направляют реакцию по
другому
пути
с меньшими
значениями
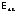 ,
хотя и с бóльшим числом стадий (рис. 1,
линия (б)).
,
хотя и с бóльшим числом стадий (рис. 1,
линия (б)).
1
2Однако, есть сведения, что даже при об.у. не только бактерии, но и человек способен усваивать азот воздуха, если не хватает белка в пище, и т.о.N2может поддерживать жизнь. Кроме того, под высоким давлением азот растворяется в липидах (жировых тканях) животных и человека, оказывая на них наркотическое действие. Так чтоN2приопределенныхусловиях биологически активен.
3Благодаря способностиNH3присоединять протон возможна очистка воды от аммиака с помощьюкатионитов в Н-форме – это твердые нерастворимые в водеоченьмногоосновныекислоты. Ионы Н+данных кислот образуют прочную связь с молекуламиNH3, поэтому аммиак поглощается из воды (при прохождении ее через слои гранул катионита).
4N2Oназывают «веселящим газом», т.к. он оказывает на организм наркотическое действие (правда, слабое), и еще в 1844 года использовался в медицине для обезболивания при операциях.
5Почва считается кислой, если концентрация ионов водорода в ее природном растворе в 300 раз выше, чем в чистой воде.
6В природе встречаются, хотя и редко, также самородки металлического алюминия.
7Самый большой искусственный сапфир, полученный в 2008 году, имеет длину 80 см.
8Очень красивой разновидностью соединений алюминия и кремния является лазурит – минерал интенсивно синего цвета (Al2SiO4(SO4,Cl,S)1-2). Крупные его образцы – драгоценные камни (ванна Екатерины II была сделана из лазурита, что удивляло и восхищало иностранцев). А из его крошки готовят ультрамарин (краска художников эпохи Возрождения). К драгоценным камням относится и сине-зеленая бирюза – водный фосфат алюминия и медиCuO.3A2O3.2P2O5.9H2O. (В результате обезвоживания бирюза старится, поэтому для сохранения ее покрывают животным жиром.)
9Это используют в металлургии (в т.н. «алюмотермии») для полученияCr,Mn,Vи др.
10«Коррозия» в переводе с латинского означает «разъедание».
11Содержание углерода в антраците 96%, в буром угле – 72%, а в сухой древесине – 50%.
12К кварцам относится и горный хрусталь – размер некоторых его природных кристаллов достигает 2 м.
13Из сиенита сложены знаменитые «Красноярские Столбы».
14На практике часто используютконцентрационнуюконстанту равновесия, т.е. выраженную через С (в относительных единицах), поэтому обозначают . Величина
15
16
17
18
19
20
21
22
23
24
25
26
27
28
29
30
31
32
33
34
35
36
37
38
39
40
41
42
43
44
45
