
- •12. Азот и фосфор
- •5.1. Общая характеристика. Нахождение в природе. Получение
- •5.2. Простые вещества
- •5.2.1. Структура и физические свойства
- •5.2.2. Химические свойства
- •5.3. Аммиак и соли аммония
- •5.3.1. Получение аммиака
- •5.3.2. Физические и химические свойства
- •5.3.3. Соли аммония
- •5.4. Оксиды и гидроксиды азота. Соли
- •5.4.1. Получение оксидов и кислот
- •5.4.2. Свойства и применение
- •5.4.3. Нитраты и нитриты
- •5.5. Кислородосодержащие соединения фосфора
- •5.6. Минеральные удобрения
- •14. Общая характеристика. Степени окисления
- •7.3.2. Природные соединения алюминия
- •7.3.3. Физические свойства
- •7.3.4. Химические свойства
- •7.3.5. Оксиды и соли p-элементов
- •7.3.6. Производство алюминия
- •16. Углерод и кремний
- •6.1. Общая характеристика. Нахождение в природе. Получение
- •6.2. Структура и физические свойства простых веществ
- •17. Константа равновесия
- •2.3.2. Сдвиг равновесия
- •19. Строение атома и химическая связь
- •3.1. Электронное строение атома
- •3.1.1. Современная модель атома
- •20. Общая характеристика
- •Получение и свойства s-металлов
- •7.2.4. Сложные вещества s-элементов. Производство соды
- •2.1.1. Термохимия
- •2.1.2. Энтропия. Энергия гиббса
- •2.1.3. Формула гиббса. Разрешенность процессов с позиции термодинамики
- •22. Метан
- •6.5. Кислородосодержащие соединения углерода
- •6.5.1. Общая характеристика и свойства
- •6.6.3. Цемент
- •25. Ионное произведение воды. Водородный показатель. Индикаторы
- •4.2.4. Буферные растворы
- •3.2. Получение простых веществ.
- •3.3. Физические свойства г2
- •27. Кислородосодержащие соединения хлора
- •Взаимодействие г2 с водородом. Получение hCl и ее свойства. Галогеноводородные кислоты
- •32. Соли аммония
- •5.4. Оксиды и гидроксиды азота. Соли
- •5.4.1. Получение оксидов и кислот
- •5.4.2. Свойства и применение
- •2.1. Распространенность водорода
- •2.2. Сходство водорода с другими элементами
- •2.2.1. Сходство с галогенами
- •2.2.2. Сходство со щелочными металлами
- •40. Особенности водорода
- •2.2.2. Кинетическое уравнение
- •2.2.3. Механизм химических реакций
- •2.2.4. Влияние температуры на скорость
- •2.2.5. Катализ
7.2.4. Сложные вещества s-элементов. Производство соды
Получение. Бинарные соединения ЩМ: гидриды, сульфиды и оксиды, – синтезируют из простых веществ. Оксиды же ЩЗМ получают термическим разложением природных карбонатов, а их гидроксиды – действием на оксиды водой. Гидроксиды ЩМ дешевле синтезировать электролизом водных растворов их хлоридов.
Соли s-элементов используют, в основном, природные, а также получают из карбонатов ЩЗМ и гидроксидов ЩМ. Например, поташ – по реакции:
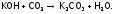
Свойства и применение гидроксидов. Растворимость гидроксидов s-элементов (а следовательно, и едкость их насыщенных растворов) растет в подгруппах от Li к Cs и от Be к Ba из-за снижения ЭО металлов и, значит, повышения ионности связи s-элемента с OH-группой. Так, если все гидроксиды ЩМ а также Ba(OH)2 хорошо растворимы, то Sr(OH)2 и Ca(OH)2 – среднерастворимы , а Mg(OH)2, тем более Be(OH)2 малорастворимы .
Щелочи KOH и (чаще) NaOH используют для получения мыла, при очистке нефти (для нейтрализации серной кислоты); в производстве целлюлозы и красок, для обработки тканей (что придает им блеск, большую прочность и лучшую окрашиваемость). А также при растворении многих веществ или для сплавления с ними с целью переведения их в растворимые соединения и т.д.
Гидроксид магния (магнезия) применяется в медицине. Гашеную известь (Ca(OH)2) и негашеную (СаO), используют в промышленности как дешевые основания (для нейтрализации кислой среды на химических производствах и связывания кислотных оксидов в металлургии), а также в строительстве как белящее средство и для приготовления т.н. известкового раствора (смесь Ca(OH)2, песка и воды). Им соединяют кирпичи, причем настолько прочно, что при разрушении стен трещины идут по кирпичам, а не между ними.
Свойства и применение солей. Как уже говорилось, растворимость (s) сложных соединений, в том числе солей, тем выше, чем более ионной является кристаллическая решетка вещества. Однако величина s зависит также от соотношения как зарядов (z), так и размеров катиона и аниона соли.
А именно: чем меньше разница z, тем ниже s. Так что растворимость соли минимальна, если одинаковы заряды катиона и аниона, и значит, их соотношение в решетке 1:1. Это обусловливает плотную и, следовательно, прочную упаковку ионов в кристалле соли. Вот почему NaCl или CaSO4 менее растворимы, чем CaCl2 или Na2SO4; например, при 200C s (NaCl)=36,4 г, а s (Na2SO4)=63,9 г в 100 г воды. Очевидно, что при одинаковых z, чем меньше сами значения z, тем выше s (закон Кулона); например, NaCl более растворим, чем CaSO4.
С другой стороны, при уменьшении разницы в размерах катиона и аниона соли, тоже повышается плотность их упаковки в решетке и, следовательно, увеличивается ее прочность. Это одна из причин снижения растворимости сульфатов от Mg к Ba (в подгруппе). Благодаря чему можно различить между собой катионы магния, кальция и бария, поскольку при добавлении H2SO4 (или растворимого сульфата) ионы Mg2+ осадка не дают, в отличие от Ba2+, а в случае Ca2+ появляется лишь небольшая муть.
Благодаря тому, что BaSO4 малорастворим, глауберову19соль (Na2SO4.10Н2O) используют как противоядие при отравлении растворимыми солями бария. Она не только связывает Ва2+ в осадок, но и одновременно оказывает послабляющее действие на кишечник, в результате чего барий быстрее выводится из организма. Применяют в медицине и «бариевую кашу» (BaSO4) – ее «едят» перед снятием рентгеновских снимков органов пищеварения, т.к. эта «каша» (из-за наличия ионов Ва) значительно менее прозрачна для рентгеновских лучей, чем мягкие ткани тела.
Используется в медицине и алебастр CaSO4.0,5H2O. (Его получают из природного минерала гипса CaSO4.2H2O обжигом при 150-180°С.) Например, при переломах костей свежеприготовленную смесь алебастра с водой (в виде густой кашицы) наносят на бинты и ими обматывают место перелома. Алебастр постепенно превращается в гипс, а поскольку при этом превращении связывается вода, то материал твердеет. Так достигается жесткая фиксация костей для их правильного срастания. Свойство алебастра «схватываться» (после смачивания его водой) в еще больших масштабах применяется в строительстве: для штукатурных работ, при изготовлении перегородочных плит и панелей, скульптурных украшений. А также для снятия слепков с различных предметов.
Широко используется и природный материал – каменная соль (NaCl): в пищевой промышленности, в дорожном хозяйстве (как средство против гололеда), а главное – в качестве сырья при получении Na, Cl2, NaOH, соды (рис.12) и др.
Соли калия в основном (до 90%) применяют как удобрения, а также в производстве стекла и мыла. Кроме того, именно нитрат калия входит в состав пороха, т.к. является негигроскопичным (в отличие от других селитр), что позволяет «держать порох сухим». Соли лития в малых дозах используют в медицине от подагры и шизофрении, но в больших количествах литий вреден.
Выше уже упоминалось о различных областях применения природных карбонатов кальция: мела (рыхлая разновидность), известняка (еще менее плотный материал) и мрамора (наиболее плотная спрессованная форма). Кроме того, значительное количество известняка идет на получение соды.
Проблемы содового производства. На схеме синтеза соды (рис.10) в затененные прямоугольники помещены формулы исходных веществ и конечных продуктов. Среди последних и раствор хлорида кальция, являющийся отходом данного производства и бедствием для окружающей среды. В частности, сброс его в реки в таких количествах, которые дают содовые предприятия, губит рыбу. Поэтому раствор CaCl2 закачивают в отстойники.
Таким образом создаются «белые моря» (белые из-за неизрасходованной гашеной извести; она полностью не отделяется и придает раствору молочный вид). Эти «моря», во-первых, занимают значительную площадь земли, а во-вторых, повышают постоянную жесткость ближайших природных вод.
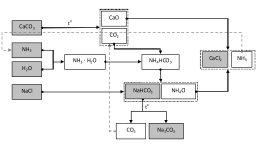
Рис. 10. Схема производства соды.
Однако разработан и уже применяется на некоторых заводах очень эффективный и практически безотходный метод получения соды из нефелинов (Na,K)2[Al2Si2O8] (побочного продукта переработки аппатитов) и известняка, т.е. метод дешев. Кроме того, при его использовании одновременно получают 14 ценных веществ: помимо соды (NaHCO3 и Na2CO3), а также KHCO3 и K2CO3, еще и оксид алюминия, цемент и др.
21.ТЕРМОХИМИЯ. ЭНТРОПИЯ. ЭНЕРГИЯ ГИББСА
Химическая термодинамика – это раздел химии, в котором изучается энергетика химических процессов и определяется направление их протекания.
Для удобства изучения необходимо изолировать объекты исследования от окружающей среды. Завершенная совокупность тел, выделенная из среды, называется системой; а химическая система – это все частицы, вступающие в реакцию, и продукты их взаимодействия.
Если между системой и окружающей средой может осуществляться и массо-, и теплообмен, то система называется открытой; если возможен лишь теплообмен, то – закрытой; если же нет ни массо-, ни теплообмена, то система изолированная.
В изолированной системе энергия (Е) не создается и не исчезает, лишь переходит из одной формы в другую, так что сумма энергий всех ее форм остается постоянной. Это закон сохранения энергии или первое начало термодинамики.
