
- •Кафедра биоорганической химии БГМУ
- •Академик Н.Н.Семенов
- •Активированный комплекс — состояние реагирующих веществ, при котором старые связи еще не разорвались,
- •Химический процесс
- •Скорость лимитирующая стадия И механизм реакции
- •КлассификацияПо направлениюорганическихреакций с учреакцийтом конечного результата:
- •По направлению реакций с учетом конечного результата :
- •По характеру изменений связей
- •Радикальные реакции
- •Свободный радикал
- •Признаки радикальных реакций
- •Признаки радикальных реакций
- •Радикальные реакции
- •Кинетическая кривая скорости свободно-радикальной реакции
- •Галогенирование циклогексана
- •AR у малых циклов (С3 – С4)
- •AR у малых циклов (С3 – С4)
- •Окисление по свободно- радикальному механизму
- •Ионные реакции
- •Реагенты:
- •Реагенты:
- •Признаки ионных реакций
- •AE- реакции электрофильного присоединения
- •Механизм реакции
- •Реакции АЕ у алкенов
- •Реакция гидратации алкенов
- •Направление реакции определяется статическим и динамическим факторами
- •Правило Марковникова в современной интерпретации:
- •Реакции электрофильного замещения у аренов SE
- •Реакция алкилирования фенола
- •Тироксин - гормон щитовидной железы
- •Реакция алкилирования спиртами и алкенами
- •Окисление по боковой цепи
- •Свободно-радикальное замещение в боковой цепи аренов
- •Реакции SN у sp3 гибридного атома углерода и конкурентные реакции E
- •Реакции SN у sp3 гибридного атома углерода и конкурентные реакцииRE
- •В зависимости от строения субстрата: мономолекулярные SN1 E1
- •Конкурентные реакции элиминирования
- •Кислоты
- •Основания
- •ПЖМКО –принцип жестких и мягких
- •Реакции АN у карбонильных соединений
- •Типичные АN реакции карбонильных соединений
- •Реакция ацетализации
- •Механизм:
- •Реакция карбонильных соединений с аминами
- •РЕАКЦИИ ВОССТАНОВЛЕНИЯ
- •Формалин – 40% р-р формальдегида в воде
- •Реакция этерификации
- •Механизм:
- •Ацетилхолин
- •Реакции ацилирования
- •фосфатидилхолин
- •БЛАГОДАРЮ ЗА ВНИМАНИЕ !
- •Реакции окисления
- •Реакция нитрования:

Реагенты:
Нуклеофильные реагенты Nu
а) отрицательно заряженные ионы
:Н :Вr¯ :ОН¯ :OR¯ :SН¯ :SR¯
б) молекулы, имеющие свободную неподеленную пару электронов
.. .. .. ..
HOH ROH RNH2 RSH

Реагенты:
Электрофильные Е
а) положительно заряженные ионы
Н+ |
Br |
+ |
Н |
С + |
Н С + |
|
|
|
3 |
|
5 |
2 |
|
б) |
молекулы |
с |
частичным |
|||
положительным зарядом на одном из
атомов |
- |
|
|
|
+ |
О |
|
|
|
С X (ЭА), |
|
|||
S |
О |
|||
|
|
О |
|
|

Признаки ионных реакций
1.гетеролитически разрывается полярная или легко поляризующаяся ковалентная связь 2.такие реакции протекают в полярных растворителях 3. катализируются кислотами или основаниями
4.являются реакциями I или II порядка

AE- реакции электрофильного присоединения
Алкены
Алкадиены Арены (в особых условиях)
Eсопр. ~ 15 кДж/моль Eсопр. ~ 150 кДж/моль

Механизм реакции |
медленно |
C C
C
Y-
C C
E
σ-комплекс
E+  C
C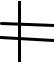 C
C
E+
π-комплекс
C |
C |
|
ст.образования |
|
|||
E |
|
Y |
σ-комплекса |
|
– скорость |
||
|
|
|
лимитирующ |
|
|
|
ая |

Реакции АЕ у алкенов
По механизму АЕ протекают реакции:
С бромной водой (Br2) –качеств. реакция на двойную связь;
Реакция гидрохлорирования (с НCl);
Реакция гидратации (с Н2О):

Реакция гидратации алкенов
НОН – нуклеофил требуется Н+ катализ
H2C |
|
C |
CH3 |
|
|
HOH |
|
H+ |
|
H3C |
|
CH CH3 |
|
|
|
|
|
|
|
||||||
|
||||||||||||
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
||||||
|
|
H |
|
|
|
|
|
AE |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
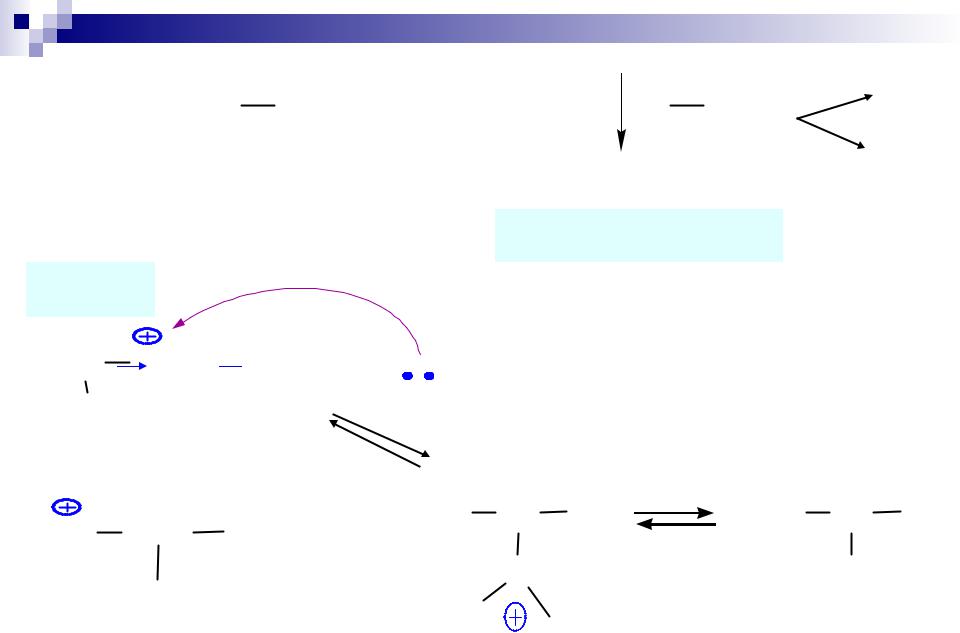
H2C C CH3
C CH3
H
+ ICH3
H2C CH CH3 H
CH3 H
Втор. карбокатион
H2C CH CH3
H
Перв. карбокатион
 H+
H+  H2C
H2C C CH3 H+H
C CH3 H+H
π-комплекс
HOH
H3C CH CH3 |
H3C |
CH CH3 |
|
H |
O |
-H+ |
OH |
H |
|
|
|
|
|
|
|
Оксокатион замещ. гидроксония |
|
||

Направление реакции определяется статическим и динамическим факторами
Статический фактор |
|
|
H2C  C CH3
C CH3
H
I -эффект
Динамический фактор
Учитывает стабильность промежуточных продуктов

Правило Марковникова в современной интерпретации:
направление присоединения реагентов типа НХ к непредельным
соединениям определяется
относительной устойчивостью образующихся карбокатионов
