
- •Кафедра биоорганической химии БГМУ
- •Кислотность и основность- основополагающие понятия, определяющие многие фундаментальные физико-химические и биологические свойства органических
- •ФУНКЦИОНАЛЬНЫЕ ГРУППЫ природных соединений
- •теория Бренстеда-Лоури
- •Электронная теория Льюиса
- •Кислотность
- •Классификация органических кислот
- •pKa — количественная характеристика кислотных свойств
- •рКа некоторых соединений
- •Качественная оценка кислотных свойств органических соединений
- •Стабильность аниона определяется характером делокализации отрицательного заряда и зависит:
- •Электроотрицательность элементов кислотного центра
- •Поляризуемость
- •Если радикалы кислот одинаковы
- •Реакции замещения
- •тиолы окисляются легко
- •Окисление фенолов
- •Окисление спиртов
- •Окисление этанола in vivo
- •Степень делокализации отрицательного заряда в анионе
- •Сравнение кислотности этанола и фенола
- •сравнение кислотности этанола и этановой кислоты
- •сравнение кислотности этанола и этандиола
- •сравнение кислотности фенола, пара-аминофенола, пара- нитрофенола
- •этоксид-анион
- •сравнение кислотности этановой кислоты, этандиовой кислоты
- •кислотность гетероциклов
- •Сравнение кислотности этоксикатиона и этанола
- •Влияние сольватации
- •Основность по Бренстеду; классификация оснований
- •n- ОСНОВАНИЯ
- •Качественная характеристика основности- величина электронной плотности на основном центре
- •Природа атома
- •Влияние радикала
- •Влияние сольватации
- •Влияние сольватации
- •Влияние сольватации
- •Реакции кислотно-основного взаимодействия
- •новокаин
- •Основность гетероциклов
- •Основность гетероциклов
- •Амфотерность органических соединений
- •амфотерность спиртов
- •способность к образованию водородных связей
- •амфотерность многоатомных спиртов
- •амфотерность аминокислот
- •амфотерность имидазола
- •AlCl3 FeCl3 BF3
- •ОСНОВАНИЯ ЛЬЮИСА
- •ПРИНЦИП «ЖЕСТКИХ» И «МЯГКИХ» КИСЛОТ И ОСНОВАНИЙ ПИРСОНА (ЖКМО)
- •Ионизация.Роль ее в проявлении биологической активности
- •Ионизация и биологическая активность
- •БЛАГОДАРЮ ЗА ВНИМАНИЕ!
- •Перераспределение -электронной плотности в сопряженной системе под влиянием заместителя, вступающего в - -
- •Комплексы протопорфирина IX
- •электронодонорные и электроноакцепторные заместители
- •ПОРФИН

Кафедра биоорганической химии БГМУ
Тема лекции 3:
КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Кислотность и основность- основополагающие понятия, определяющие многие фундаментальные физико-химические и биологические свойства органических соединений, позволяющие оценивать реакционные центры, состояние и реакционную способность природных соединений в зависимости от рН среды.
ФУНКЦИОНАЛЬНЫЕ ГРУППЫ природных соединений
- ОН |
гидроксигруппа |
- SH |
сульфгидрильная (тиольная) |
- NН2 |
аминогруппа |
>NH |
иминогруппа |
> C=O |
оксогруппа |
- СООН |
карбоксильная група |
Общим их качеством является способность проявлять кислотно-основные свойства
теория Бренстеда-Лоури
протолитическая теория
кислоты - вещества, способные в растворах отдавать протон
основания - вещества, способные присоединять протон
А — Н + :В |
А- + В — Н |
||
кислота |
основание |
сопряженное |
сопряженная |
|
|
основание |
кислота |
Электронная теория Льюиса
кислота — акцептор пары электронов
основание — донор пары электронов
H+ |
+ |
NH3 |
|
|
|
NH4+ |
|
|
|||||
|
|
|
Кислота
Льюиса
Основание
Льюиса
Кислотность
Классификация органических кислот
ОН-кислоты: спирты, фенолы, карбоновые кислоты, сульфокислоты, гидроксикислоты, аминокислоты
SH-кислоты: тиоспирты, SH-содержащие соединения
NH-кислоты: амины, имины, гетероциклические соединения с атомом азота
СН-кислоты: углеводороды, радикалы гетерофункциональных соединений
Классификация органических кислот
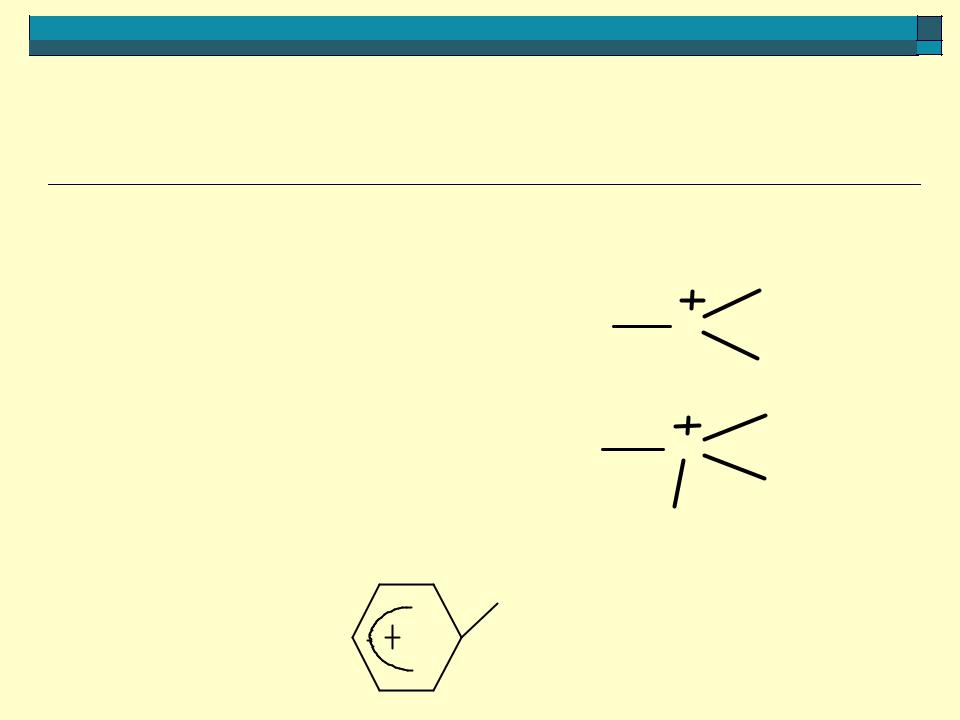
Положительно заряженные ионы:
алкилоксониевый ион
алкиламмониевый ион
|
H |
R |
O |
|
H |
|
H |
R |
N |
|
H |
|
H |
-комплекс E
 H
H
pKa — количественная характеристика кислотных свойств
CH COOH + H O |
CH3COO- + H3O+ |
|
3 |
2 |
|
K |
CH3COO H3O |
|
CH3COOH H2O |
||
|
||
|
Ka K H2O CH3COO H3O |
|
|
CH3COOH |
pKa = -lg Ka

рКа некоторых соединений
R – Н2 С –Н |
R –HN–H |
R –OH |
Алкан |
амин |
спирт |
рКа 40 |
30 |
18 |
ЭО |
С- 2,5 |
N – 3,0 |
O
CH3 — C 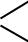 OH
OH
уксусная (карбоновая) кислота
R –SH |
Ar – O-H |
тиоспирт |
фенол |
12 |
10 |
О – 3,5 |
|
Бензойная кислота 4,25
4.75

Качественная оценка кислотных свойств органических соединений
Качественная характеристика кислотности – стабильность аниона, образующегося при диссоциации кислоты
RH 
 R- + H+
R- + H+
чем стабильнее анион, тем сильнее кислота
