
- •Министерство образования и науки рф
- •Введение
- •Раздел I. Основы химической термодинамики
- •1.1 Основные понятия, используемые в химической термодинамике
- •1.2 Первый закон термодинамики
- •1.3 Термохимия
- •1.3.1 Закон Гесса и следствия из него. Расчет тепловых эффектов
- •1.3.2 Понятие о теплоемкости веществ
- •1.3.3 Влияние температуры на тепловой эффект
- •1.4 Второй закон термодинамики. Энтропия
- •1.4.1 Процессы самопроизвольные и несамопроизвольные,
- •1.4.2 Формулировки и математическое выражение
- •II закона термодинамики
- •1.4.3 Изменение энтропии – критерий направления
- •1.4.4 Статистическая интерпретация энтропии
- •1.4.5 Расчет изменения энтропии при протекании
- •1.4.6 Абсолютные значения энтропии твердых, жидких
- •1. Абсолютное значение энтропии твердых кристаллических тел.
- •2. Абсолютное значение энтропии жидкости.
- •3. Абсолютное значение энтропии газа.
- •1.5 Термодинамические потенциалы
- •Критерии оценки направления самопроизвольного протекания процессов
- •Раздел II. Растворы и гетерогенные равновесия
- •2.1 Основные понятия и определения
- •2.2 Химический потенциал
- •Условие термодинамического равновесия в растворе
- •2.4 Условие равновесия в гетерогенной системе
- •2.5 Правило фаз Гиббса
- •2.6 Равновесие в однокомпонентной двухфазной системе.
- •2.7 Применение правила фаз Гиббса к анализу диаграммы
- •2.8 Равновесие в гетерогенных системах, состоящих
- •2.8.1 Равновесие жидкость – пар. Закон Рауля
- •2.8.2 Коллигативные свойства растворов
- •2.8.3 Равновесие жидкость-жидкость. Распределение вещества
- •Раздел III. Химическое равновесие
- •3.1 Уравнение изотермы химической реакции
- •3.2 Влияние внешних условий на протекание химической реакции
- •Раздел IV. Электрохимия
- •4.1 Равновесие в растворах слабых электролитов
- •4.2 Термодинамика растворов сильных электролитов
- •4.3 Электрическая проводимость растворов электролитов
- •4.4 Электродвижущие силы и электродные потенциалы
- •Механизм возникновения электродных потенциалов и их расчет
- •Термодинамика гальванического элемента
- •Основные типы электродов и расчет их потенциала
- •Раздел V. Химическая кинетика и катализ
- •5.1 Основной закон химической кинетики.
- •5.2 Основы формальной кинетики кинетика необратимых реакций
- •5.3 Методы определения порядка реакции
- •3. Метод Вант-Гоффа.
- •5.4 Влияние температуры на скорость реакции
- •5.5 Основные понятия катализа
1.4 Второй закон термодинамики. Энтропия
Первый закон термодинамики позволяет рассчитать тепловые эффекты различных процессов и работу, совершаемую системой, но ничего не говорит о направлении самопроизвольного протекания процесса.
Второй закон термодинамики устанавливает возможность, направление и предел протекания самопроизвольных процессов. С его помощью можно предсказать направление процесса, не прибегая к дополнительному эксперименту, и определить необходимое изменение условий, позволяющее провести процесс в нужном направлении.
Почему многие экзотермические реакции, сопровождающиеся выделением теплоты, не могут протекать самопроизвольно? И почему все-таки протекают эндотермические процессы, подобные испарению? И почему невозможно построить тепловую машину, КПД которой был бы равен 1? На эти вопросы отвечает II закон термодинамики.
Но прежде, чем перейти к изложению сути II закона термодинамики, необходимо дать характеристику самопроизвольным процессам.
1.4.1 Процессы самопроизвольные и несамопроизвольные,
обратимые и необратимые
Все процессы, протекающие в природе, могут быть разделены на самопроизвольные и несамопроизвольные.
Самопроизвольным, или положительным, называется процесс, который совершается в системе без вмешательства со стороны окружающей среды. Например, переход теплоты от горячего тела к холодному, плавление льда при t > 0 С.
П роцесс
протекает самопроизвольно, если в
системе существует градиент соответствующего
свойства, т.е. отсутствует симметрия в
распределении этого свойства. Например,
переход теплоты от горячего тела к
холодному происходит потому, что
существует градиент температур (Т1
> Т2).
При равенстве температур никакого
переноса тепла не будет.
роцесс
протекает самопроизвольно, если в
системе существует градиент соответствующего
свойства, т.е. отсутствует симметрия в
распределении этого свойства. Например,
переход теплоты от горячего тела к
холодному происходит потому, что
существует градиент температур (Т1
> Т2).
При равенстве температур никакого
переноса тепла не будет.
Свойства самопроизвольных процессов.
1) Скорость самопроизвольных процессов измерима (достаточно велика).
2) Достаточно велика и их движущая сила.
3) Самопроизвольные процессы приближают систему к состоянию равновесия, из которого она самопроизвольно выйти не может.
4) Самопроизвольные процессы термодинамически необратимы, т.е. после их протекания систему и окружающую среду одновременно нельзя вернуть в первоначальное состояние: систему можно вернуть в прежнее состояние, затратив работу, но при этом произойдут изменения в окружающей среде (например, изменится энергия окружающих тел).
5) При протекании самопроизвольного процесса совершается работа Ан/о (работа необратимого процесса).
Если при осуществлении процесса система может вернуться в исходное состояние, не оставляя видимых изменений в окружающей среде, такой процесс является термодинамически обратимым. При этом в обратном направлении система проходит через те же промежуточные состояния, что и в прямом. Это значит, что в ходе прямого процесса должна производиться работа Аобр., достаточная для того, чтобы вернуть систему в исходное состояние без помощи внешней среды.
Термодинамическое понятие обратимости не совпадает со значением этого термина в химической кинетике. Обратимой в кинетике считают реакцию, результирующая скорость которой определяется разностью скоростей протекания ее в прямом и обратном направлениях, причем на величину этой разности не накладывается каких-либо ограничений.
Для термодинамической обратимости требуется, чтобы реакция проходила в условиях, бесконечно близких к равновесию, когда скорости прямого и обратного процессов различаются на бесконечно малую величину.
Основные свойства обратимых процессов.
1) Обратимые процессы идут с бесконечно малой скоростью.
2) Движущая сила обратимых процессов бесконечно мала.
3) Для реализации обратимого процесса система должная пройти через бесконечно большое число стадий.
4) Работа, производимая системой в ходе обратимого процесса, максимальна: Аобр. = Аmax
В природе и технике протекают только необратимые процессы. Но любой реальный процесс можно представить протекающим в условиях, сколь угодно близких к условиям обратимого процесса. Сравнивая реальный процесс с обратимым, можно в каждом конкретном случае указать пути повышения эффективности процесса.
Наилучшей моделью обратимого процесса может служить бесконечно медленно протекающий процесс.
В оспользуемся
известным примером изотермического
(Т
= const)
расширения 1 моль идеального газа в
цилиндре с поршнем (рис. 1.3). Поршень
движется без трения. На поршень помещен
груз в виде горки песка, поддерживающий
заданное давление газа р1.
Состояние системы описывается двумя
параметрами – p
и V
(рис. 1.4).
Кривая AEKB
– изотерма равновесия газа. При снятии
груза поршень поднимается, объем газа
увеличивается, совершается работа
расширения.
оспользуемся
известным примером изотермического
(Т
= const)
расширения 1 моль идеального газа в
цилиндре с поршнем (рис. 1.3). Поршень
движется без трения. На поршень помещен
груз в виде горки песка, поддерживающий
заданное давление газа р1.
Состояние системы описывается двумя
параметрами – p
и V
(рис. 1.4).
Кривая AEKB
– изотерма равновесия газа. При снятии
груза поршень поднимается, объем газа
увеличивается, совершается работа
расширения.
И сходное
состояние системы (точкаА)
характеризуется давлением газа в
цилиндре р1
и объемом V1,
конечное состояние (точка В) – давлением
р2
и объемом V2.
Переход системы из начального состояния
в конечное можно осуществить различными
путями.
сходное
состояние системы (точкаА)
характеризуется давлением газа в
цилиндре р1
и объемом V1,
конечное состояние (точка В) – давлением
р2
и объемом V2.
Переход системы из начального состояния
в конечное можно осуществить различными
путями.
1. Сразу снизить нагрузку на поршень до давления р2, объем газа резко возрастет и станет равным V2. При этом совершится работа расширения
A = p2(V2 – V1),
которая равна площади под ломаной кривой АСВ.
2. Процесс можно провести через ряд последовательных стадий, например, снимать с поршня определенные (конечные) порции песка. Как только объем газа достигнет значения, отвечающего новому давлению на поршень, в системе установится равновесие.
Работа возрастет на величину площади фигуры DEFKLC и станет равной
![]() ,
,
где рi – внешнее давление; Vi – изменение объема, отвечающее данному давлению (при снятии соответствующего груза).
При увеличении числа стадий, т.е. при уменьшении снимаемой нагрузки, работа еще более возрастает.
В пределе, когда снимаемый груз бесконечно мал (снимаем по одной песчинке), а число стадий бесконечно велико, система все время будет приближена к состоянию равновесия. Такой процесс будет обратимым, работа его максимальна:
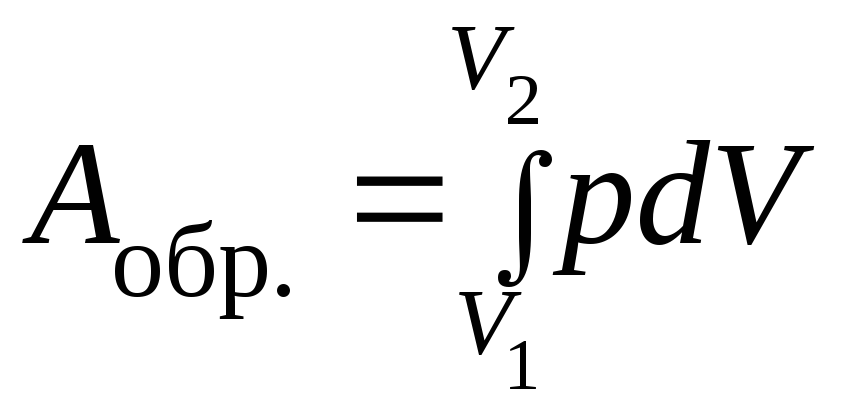 (1.17)
(1.17)
Под интегралом находятся две зависимые переменные – р и V. Произведем замену, используя уравнение состояния идеального газа (1.1):
![]()
![]() .
.
После подстановки в (1.17)
 ,
,
 . (1.18)
. (1.18)
Уравнение (1.18) применяется для расчета работы обратимого расширения 1 моль идеального газа.
Выводы:
1) работа обратимо протекающих процессов максимальна, работа реальных процессов всегда меньше;
2) чем выше степень необратимости процесса, тем меньше работа, производимая системой.
Если I закон термодинамики применим к любым термодинамическим процессам в равной мере, то II закон имеет различное выражение при применении его к обратимым и необратимым процессам.
