
- •Министерство образования и науки рф
- •Введение
- •Раздел I. Основы химической термодинамики
- •1.1 Основные понятия, используемые в химической термодинамике
- •1.2 Первый закон термодинамики
- •1.3 Термохимия
- •1.3.1 Закон Гесса и следствия из него. Расчет тепловых эффектов
- •1.3.2 Понятие о теплоемкости веществ
- •1.3.3 Влияние температуры на тепловой эффект
- •1.4 Второй закон термодинамики. Энтропия
- •1.4.1 Процессы самопроизвольные и несамопроизвольные,
- •1.4.2 Формулировки и математическое выражение
- •II закона термодинамики
- •1.4.3 Изменение энтропии – критерий направления
- •1.4.4 Статистическая интерпретация энтропии
- •1.4.5 Расчет изменения энтропии при протекании
- •1.4.6 Абсолютные значения энтропии твердых, жидких
- •1. Абсолютное значение энтропии твердых кристаллических тел.
- •2. Абсолютное значение энтропии жидкости.
- •3. Абсолютное значение энтропии газа.
- •1.5 Термодинамические потенциалы
- •Критерии оценки направления самопроизвольного протекания процессов
- •Раздел II. Растворы и гетерогенные равновесия
- •2.1 Основные понятия и определения
- •2.2 Химический потенциал
- •Условие термодинамического равновесия в растворе
- •2.4 Условие равновесия в гетерогенной системе
- •2.5 Правило фаз Гиббса
- •2.6 Равновесие в однокомпонентной двухфазной системе.
- •2.7 Применение правила фаз Гиббса к анализу диаграммы
- •2.8 Равновесие в гетерогенных системах, состоящих
- •2.8.1 Равновесие жидкость – пар. Закон Рауля
- •2.8.2 Коллигативные свойства растворов
- •2.8.3 Равновесие жидкость-жидкость. Распределение вещества
- •Раздел III. Химическое равновесие
- •3.1 Уравнение изотермы химической реакции
- •3.2 Влияние внешних условий на протекание химической реакции
- •Раздел IV. Электрохимия
- •4.1 Равновесие в растворах слабых электролитов
- •4.2 Термодинамика растворов сильных электролитов
- •4.3 Электрическая проводимость растворов электролитов
- •4.4 Электродвижущие силы и электродные потенциалы
- •Механизм возникновения электродных потенциалов и их расчет
- •Термодинамика гальванического элемента
- •Основные типы электродов и расчет их потенциала
- •Раздел V. Химическая кинетика и катализ
- •5.1 Основной закон химической кинетики.
- •5.2 Основы формальной кинетики кинетика необратимых реакций
- •5.3 Методы определения порядка реакции
- •3. Метод Вант-Гоффа.
- •5.4 Влияние температуры на скорость реакции
- •5.5 Основные понятия катализа
1.3 Термохимия
Термохимия – раздел химической термодинамики, изучающий взаимосвязь химических и физико-химических процессов с сопровождающими их тепловыми эффектами.
Тепловой эффект – это количество теплоты, которое система выделяет или поглощает в необратимо протекающем процессе.
В любом акте химического превращения принимает участие некоторая совокупность атомов, характеризующая исходные вещества, а после их перераспределения – и продукты реакции. Перегруппировка атомов вызвана изменением химических связей в молекулах реагирующих веществ. Поскольку внутренняя энергия исходных молекул отличается от внутренней энергии продуктов реакции, то происходит изменение внутренней энергии системы, которое сопровождается тепловым эффектом и совершением работы.
Процессы, при протекании которых теплота выделяется, являются экзотермическими. Процессы, протекающие с поглощением теплоты, – эндотермические.
1.3.1 Закон Гесса и следствия из него. Расчет тепловых эффектов
химических реакций в стандартных условиях
Многие химические реакции протекают при постоянном объеме или постоянном давлении. Из первого закона термодинамики следует, что при этих условиях теплота является функцией состояния:
QV = U,
Qp = H.
Эти равенства в применении к химическим реакциям составляют суть закона Гесса, открытого в 1836 г. русским химиком Г.И. Гессом:
Тепловой эффект химической реакции не зависит от пути проведения реакции, а определяется только н6ачальным и конечным состоянием системы при следующих условиях:
1) процесс осуществляется при V = const или p = const;
2) температура исходного и конечного состояний системы одинакова (однако это не означает, что она должна быть постоянной в течение всего процесса);
3) единственным видом работы является работа расширения (сжатия).
Если не выполняется хотя бы одно из условий, закон Гесса не работает.
Д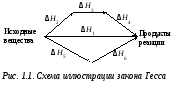 ействие
закона Гесса удобно представить в виде
схемы. Рассмотрим некоторый обобщенный
химический процесс превращения исходных
веществ в продукты реакции, который
может быть осуществлен различными
путями в одну или несколько стадий (рис.
1.1).
ействие
закона Гесса удобно представить в виде
схемы. Рассмотрим некоторый обобщенный
химический процесс превращения исходных
веществ в продукты реакции, который
может быть осуществлен различными
путями в одну или несколько стадий (рис.
1.1).
Согласно закону Гесса, тепловые эффекты всех этих реакций связаны между собой соотношением:
Н1 = Н2 + Н3 + Н4 = Н5 + Н6.
Тепловой эффект изобарного процесса часто называют просто энтальпией.
Уравнение реакции с указанием агрегатного состояния реагентов и теплового эффекта реакции называют термохимическим уравнением. Например, термохимическое уравнение реакции образования бензола в жидком состоянии из простых веществ запишется:
6С (т) + 3Н2 (г) = С6Н6 (ж), Н = 49,03 кДж/моль,
где символы (т), (ж), (г) указывают на агрегатное состояние реагента. Эти символы обычно опускаются, когда агрегатное состояние вещества является очевидным в данных условиях. Верхний индекс «» у теплового эффекта указывает на то, что все реагенты взяты в стандартном состоянии.
Стандартное
состояние
– это состояние чистого вещества при
давлении
1 атм (101325 Па) и заданной
температуре (Т
=const).
При этом вещества должны быть взяты в
том агрегатном состоянии, в котором они
являются термодинамически устойчивыми.
В
справочной литературе приводятся
величины, характеризующие вещество в
стандартном состоянии, определяемом
более узко, а именно
р
= 1 атм и Т
= 298 К.
Стандартную энтальпию реакции, протекающей
при температуре Т,
обозначают
![]() (индексr
означает «reaction»
– реакция).
(индексr
означает «reaction»
– реакция).
Практическое значение закона Гесса состоит в том, что он позволяет рассчитывать энтальпии тех химических процессов, для которых непосредственное определение ΔrН связано с большими экспериментальными затруднениями.
Пусть при p = const протекают реакции:
С + О2 → СО2 + ΔrН1
СО + ½О2 → СО2 + ΔrН2
С + ½О2 → СО + ΔrН3
Энтальпии реакций (1) и (2) ΔrН1 и ΔrН2 могут быть определены с высокой точностью экспериментальным путем, в то время как энтальпию реакции (3) ΔrН3 непосредственно измерить невозможно, так как при горении углерода наряду с СО всегда образуется СО2. На основании исходных данных удобно составить схему возможных путей образования СО2 (рис. 1.2).

Рис. 1.2. Схема расчета по закону Гесса
В соответствии с законом Гесса энтальпия процесса, протекающего первым (прямым) путем, равна энтальпии процесса, протекающего вторым путем через промежуточное состояние:
ΔrН1 = ΔrН2 + ΔrН3.
Неизвестная энтальпия ΔrН3 равна
ΔrН3 = ΔrН1 – ΔrН2.
Таким образом, определив опытным путем тепловые эффекты некоторых процессов, можно, используя закон Гесса, вычислить тепловые эффекты других процессов, связанных с первыми системой термохимических уравнений.
Из закона Гесса вытекают важные следствия, которые позволяют рассчитывать тепловые эффекты (энтальпии) химических реакций.
1 следствие: тепловой эффект химической реакции, протекающей при температуре Т, равен сумме теплот образования продуктов реакции за вычетом суммы теплот образования исходных веществ с учетом стехиометрических коэффициентов:
![]() ,
(1.5)
,
(1.5)
где
![]() – стандартная энтальпия (теплота)
образования вещества (индексf
означает «formation»
– образование);
– стандартная энтальпия (теплота)
образования вещества (индексf
означает «formation»
– образование);
![]() – стехиометрические коэффициенты
продуктов реакции и исходных веществ.
– стехиометрические коэффициенты
продуктов реакции и исходных веществ.
Стандартной энтальпией (теплотой) образования вещества при заданной температуре называют тепловой эффект реакции образования 1 моль данного вещества из соответствующих количеств простых веществ, находящихся в наиболее устойчивом стандартном состоянии. Согласно решению Международного союза чистой и прикладной химии (IUPAC) стандартные теплоты образования простых веществ принимаются равными 0 при любой температуре.
Стандартную
энтальпию образования при Т
= 298 К рекомендуется обозначать
![]() ,
гдеi
–
соединение; j
– агрегатное состояние.
,
гдеi
–
соединение; j
– агрегатное состояние.
Например,
стандартную теплоту образования воды
при Т
= 298 К обозначают
![]() .
Термохимическое уравнение реакции
образования воды приТ
= 298 К запишется
.
Термохимическое уравнение реакции
образования воды приТ
= 298 К запишется
Н2
+ ½О2
= Н2О
(ж) +
![]() .
.
Стандартные энтальпии веществ при Т = 298 К приведены в справочниках.
В качестве примера рассмотрим расчет теплового эффекта химической реакции
СО2 + 4Н2 = СН4 + 2Н2О,
протекающей в газовой фазе при Т = 298 К и р = 1 атм.
Теплота образования водорода по определению равна 0. Следовательно, в соответствии с (1.5), тепловой эффект данной реакции равен
![]() .
.
2 следствие: тепловой эффект химической реакции равен сумме теплот сгорания исходных веществ за вычетом суммы теплот сгорания продуктов реакции с учетом стехиометрических коэффициентов:
![]() , (1.6)
, (1.6)
где
![]() – стандартная энтальпия (теплота)
сгорания вещества (индексс
означает «combustion»
– сгорание).
– стандартная энтальпия (теплота)
сгорания вещества (индексс
означает «combustion»
– сгорание).
Стандартной энтальпией (теплотой) сгорания вещества называют энтальпию реакции полного окисления 1 моль вещества до высших оксидов. Теплоты сгорания высших оксидов принимаются равными 0.
Например, термохимическое уравнение реакции сгорания глюкозы запишется:
С6Н12О6
+ 6О2
= 6СО2
+ 6Н2О
+
![]() .
.
Это следствие обычно используют для расчета тепловых эффектов органических реакций.
