
- •Министерство образования и науки рф
- •Введение
- •Раздел I. Основы химической термодинамики
- •1.1 Основные понятия, используемые в химической термодинамике
- •1.2 Первый закон термодинамики
- •1.3 Термохимия
- •1.3.1 Закон Гесса и следствия из него. Расчет тепловых эффектов
- •1.3.2 Понятие о теплоемкости веществ
- •1.3.3 Влияние температуры на тепловой эффект
- •1.4 Второй закон термодинамики. Энтропия
- •1.4.1 Процессы самопроизвольные и несамопроизвольные,
- •1.4.2 Формулировки и математическое выражение
- •II закона термодинамики
- •1.4.3 Изменение энтропии – критерий направления
- •1.4.4 Статистическая интерпретация энтропии
- •1.4.5 Расчет изменения энтропии при протекании
- •1.4.6 Абсолютные значения энтропии твердых, жидких
- •1. Абсолютное значение энтропии твердых кристаллических тел.
- •2. Абсолютное значение энтропии жидкости.
- •3. Абсолютное значение энтропии газа.
- •1.5 Термодинамические потенциалы
- •Критерии оценки направления самопроизвольного протекания процессов
- •Раздел II. Растворы и гетерогенные равновесия
- •2.1 Основные понятия и определения
- •2.2 Химический потенциал
- •Условие термодинамического равновесия в растворе
- •2.4 Условие равновесия в гетерогенной системе
- •2.5 Правило фаз Гиббса
- •2.6 Равновесие в однокомпонентной двухфазной системе.
- •2.7 Применение правила фаз Гиббса к анализу диаграммы
- •2.8 Равновесие в гетерогенных системах, состоящих
- •2.8.1 Равновесие жидкость – пар. Закон Рауля
- •2.8.2 Коллигативные свойства растворов
- •2.8.3 Равновесие жидкость-жидкость. Распределение вещества
- •Раздел III. Химическое равновесие
- •3.1 Уравнение изотермы химической реакции
- •3.2 Влияние внешних условий на протекание химической реакции
- •Раздел IV. Электрохимия
- •4.1 Равновесие в растворах слабых электролитов
- •4.2 Термодинамика растворов сильных электролитов
- •4.3 Электрическая проводимость растворов электролитов
- •4.4 Электродвижущие силы и электродные потенциалы
- •Механизм возникновения электродных потенциалов и их расчет
- •Термодинамика гальванического элемента
- •Основные типы электродов и расчет их потенциала
- •Раздел V. Химическая кинетика и катализ
- •5.1 Основной закон химической кинетики.
- •5.2 Основы формальной кинетики кинетика необратимых реакций
- •5.3 Методы определения порядка реакции
- •3. Метод Вант-Гоффа.
- •5.4 Влияние температуры на скорость реакции
- •5.5 Основные понятия катализа
1.4.6 Абсолютные значения энтропии твердых, жидких
и газообразных тел
1. Абсолютное значение энтропии твердых кристаллических тел.
Воспользуемся для расчета энтропии кристаллического тела уравнением II закона термодинамики:
![]() .
.
Проинтегрируем уравнение в неопределенных пределах от абсолютного нуля до температуры Т:
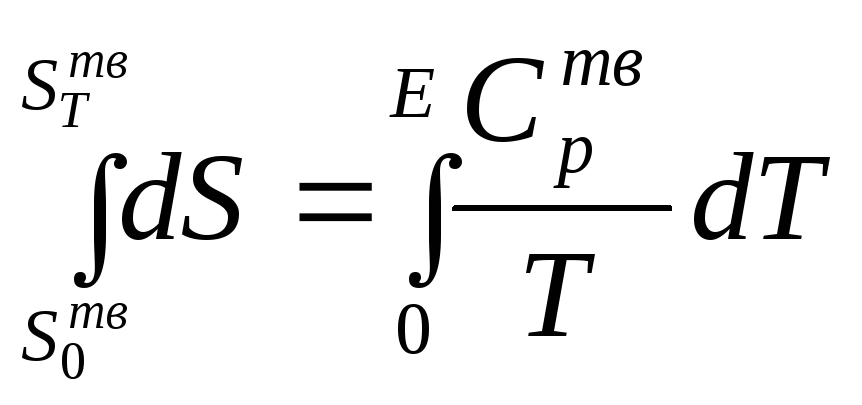 ,
,
 .
.
Для расчета
![]() необходимо знать зависимость
необходимо знать зависимость![]() ,
а также
,
а также![]() ,
то есть энтропию твердого кристаллического
тела при абсолютном нуле.
,
то есть энтропию твердого кристаллического
тела при абсолютном нуле.
Немецкий ученый
Планк сформулировал постулат, в
соответствии с которым: энтропия
идеальной конденсированной системы
вблизи абсолютного нуля равна нулю:
![]() .
.
Идеальная конденсированная система – твердое тело, в кристаллической решетке которого нет дефектов, и наблюдается абсолютный порядок. Термодинамическая вероятность идеального кристалла равна единице, а энтропия равна нулю:
![]()
Постулат Планка иногда называют III началом термодинамики.
Тогда появляется возможность рассчитать абсолютные значения энтропии твердых веществ при любой температуре:
 .
.
2. Абсолютное значение энтропии жидкости.
Абсолютное значение энтропии жидкости при температуре Т равно:
![]() ,
,
где
![]() –
изменение энтропии кристаллического
вещества в интервале температур от
абсолютного нуля до температуры плавленияТпл
(численно равно абсолютному значению
энтропии твердого вещества при Тпл:
–
изменение энтропии кристаллического
вещества в интервале температур от
абсолютного нуля до температуры плавленияТпл
(численно равно абсолютному значению
энтропии твердого вещества при Тпл:
![]() );
ΔSпл
– изменение энтропии при плавлении
твердого кристаллического вещества;
ΔSж.
– изменение энтропии при нагревании
жидкости от Тпл.
до температуры Т.
);
ΔSпл
– изменение энтропии при плавлении
твердого кристаллического вещества;
ΔSж.
– изменение энтропии при нагревании
жидкости от Тпл.
до температуры Т.
Подставляем выражения для ΔSтв, ΔSпл и ΔSж:
 .
.
3. Абсолютное значение энтропии газа.
Абсолютная значение энтропии газа рассчитывается:
![]() ,
,
где ΔSж – изменение энтропии жидкости при нагревании ее от Тпл. до температуры кипения Ткип.; ΔSисп – изменение энтропии при испарении жидкости; ΔSг – изменение энтропии при нагревании газа от Ткип до температуры Т. Тогда
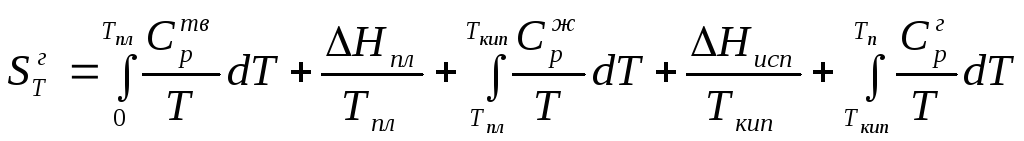 .
.
1.5 Термодинамические потенциалы
и направление самопроизвольных процессов
Изменение энтропии однозначно определяет направление и предел самопроизвольного протекания процесса лишь для наиболее простых систем – изолированных: если в результате расчета окажется, что S > 0, процесс пойдет самопроизвольно, при S = 0 – состояние равновесия, если S < 0, процесс самопроизвольно протекать не будет.
На практике приходится иметь дело преимущественно с системами, взаимодействующими с окружающей средой. В качестве критерия оценки направления самопроизвольных процессов в таких системах используются термодинамические потенциалы.
Термодинамическим потенциалом называют функцию состояния, убыль которой в обратимо протекающем процессе при постоянстве определенных параметров равна максимальной полезной работе.
Наибольшее значение имеют два основных термодинамических потенциала: энергия Гельмгольца F (T, V) и энергия Гиббса G (T, p). В скобках указаны параметры, функциями которых являются термодинамические потенциалы.
Чтобы получить представление о термодинамических потенциалах, воспользуемся объединенным математическим выражением первого и второго законов термодинамики.
![]() .
.
![]() или
или
![]() .
.
![]() ,
,
![]() .
(1.23)
.
(1.23)
Рассмотрим соответствующие процессы.
И з о б а р н о – и з о т е р м и ч е с к и й п р о ц е с с (p, T = const).
Уравнение (1.23) запишется
![]() ,
,
![]() ,
,
где H – TS = G –свободная энергия Гиббса. При p, T = const изменение энергии Гиббса связано с выполнением полезной работы:
![]() .
.
В обратимо
протекающем процессе
![]() .
Тогда
.
Тогда
![]() ,
,
![]() .
.
Таким образом, свободная энергия Гиббса является изобарно-изотермическим потенциалом, так как ее уменьшение характеризует максимальную работу этого процесса.
Если единственным
видом работы является работа расширения
(сжатия), т.е.
![]() ,
то в необратимом, а, следовательно,
самопроизвольно протекающем процессе
,
то в необратимом, а, следовательно,
самопроизвольно протекающем процессе
![]() . (1.24)
. (1.24)
И з о х о р н о – и з о т е р м и ч е с к и й п р о ц е с с (V, T = const).
Уравнение (1.23) примет вид
![]() ,
,
где U – TS = F – свободная энергия Гельмгольца. При V, T = const изменение энергии Гельмгольца связано с выполнением полезной работы:
![]() .
.
В обратимо протекающем процессе
![]() ,
,
![]() .
.
Таким образом, свободная энергия Гельмгольца является изохорно-изотермическим потенциалом.
Если
![]() ,
то в самопроизвольно протекающем
процессе
,
то в самопроизвольно протекающем
процессе
![]() .
(1.25)
.
(1.25)
Неравенства (1.24), (1.25) являются условием самопроизвольного протекания процесса при постоянстве соответствующих параметров: самопроизвольно могут протекать только те процессы, которые приводят к понижению свободной энергии системы; система приходит в состояние равновесия, когда свободная энергия достигает минимального значения (рис. 1.7.).

Процессы, которые сопровождаются увеличением термодинамических потенциалов, протекают лишь при совершении работы извне над системой.
Изменение соответствующего термодинамического потенциала в ходе какого-либо процесса, протекающего при температуре Т, вычисляют по уравнению Гиббса-Гельмгольца:
– для изобарно-изотермического процесса
G = H – TS, (1.26)
– для изохорно-изотермического процесса
F = U – TS. (1.27)
Основываясь на уравнении Гиббса-Гельмгольца (1.26), (1.27), можно оценить вклад энтальпийного и энтропийного факторов в величину ΔG (или ΔF) и сделать некоторые обобщающие заключения о возможности самопроизвольного протекания химических процессов.
1. Экзотермические реакции, ΔH < 0.
Если ΔS > 0, то ΔG всегда отрицательно; экзотермические реакции, сопровождающиеся увеличением энтропии, всегда протекают самопроизвольно.
Если ΔS < 0, реакция будет идти самопроизвольно при H > TS (низкие температуры).
2. Эндотермические реакции, ΔH > 0.
Если ΔS > 0, процесс будет самопроизвольным при H < TS (высокие температуры).
Если ΔS < 0, то ΔG всегда положительно; самопроизвольное протекание эндотермических реакций, сопровождающихся уменьшением энтропии, невозможно.
Термодинамические потенциалы могут играть роль характеристических функций. Это значит, что с помощью их производных можно выразить свойства системы, необходимые для ее характеристики.
Изобарно-изотермический потенциал является функцией двух параметров – давления и температуры, т.е.
![]() .
.
Запишем dG в виде суммы частных производных
 .
(1.28)
.
(1.28)
Учитывая, что
![]() ,
,
получаем:

Изохорно-изотермический потенциал является функцией объема и температуры, т.е.
![]() .
(1.29)
.
(1.29)
По определению
![]() ,
,
откуда следует, что
 .
.
Легко установить связь между G и F. Вычитая из уравнения (1.26) уравнение (1.27), и учитывая, что U = Н – nRT, получим:
G = F + nRT.
Разберем физический смысл изобарно-изотермического и изохорно-изотермического потенциалов.
G = H – TS, F = U – TS;
H = G + TS, U = F + TS,
где H и U – изменение полной энергии в системе при р = const и V = const соответственно; G и F – энергия, которая связана с производством полезной работы; TS – энергия, которая перешла в энергию хаотичного (теплового) движения частиц, вследствие чего она уже не может перейти в работу.
Поэтому G и F называют еще свободной энергией, а TS – связанной энергией.
Т а б л и ц а
