
7 семестр / Основы_физич_химии_Теория_и_задачи_Еремин_и_др_2005_480с
.pdf



338 |
Г л а в а 5. Химическая кинетика |
Экспериментальная энергия активации складывается из энергии активации гетерогенной реакции и энтальпии адсорбции (которая обычно имеет отрицательное значение), что подтверждает уравнение (23.20)
Если же адсорбционная способность продукта мала, а реагента велика, KL,P pP << 1 << KL,S pS, то почти вся поверхность заполнена молекулами реагента, скорость реакции постоянна:
r = k1
и реакция имеет нулевой порядок. Этот режим соответствует максимальной загрузке катализатора.
Кинетика двухсубстратных реакций на поверхности катализатора рассмотрена в примере 23-5.
ПРИМЕРЫ
Пример 23-1. Опишите кинетику реакции специфического кислотного катализа в разбавленном водном растворе, используя квазиравновесное приближение. Выразите скорость образования продукта через:
а) текущую, б) исходную концентрацию субстрата.
Коэффициенты активности принять равными единице.
Решение. Скорость образования продукта пропорциональна концентрации протонированной формы субстрата:
r = k2[SH+] .
В квазиравновесном приближении эту концентрацию можно выразить через константу основности субстрата:
[SH+] = Kb[S][H3O+]
(в разбавленном растворе коэффициенты активности принимаем равными 1). Отсюда следует, что скорость реакции прямо пропорциональна текущей концентрации субстрата, а реакция имеет второй порядок:
r = k2 Kb[H3O+][S] .
Текущая концентрация субстрата связана с его начальной концентрацией уравнением материального баланса:
[S]0 =[S] +[SH+].
Если учесть связь [S] и [SH+] через константу основности и выразить [SH+] через [S]0, то получим следующее выражение для скорости реакции:
r = |
k |
K |
[H |
O+] |
|
2 |
b |
3 |
|
[S] . |
|
|
|
|
|
||
|
1+ Kb[H3O+] |
0 |
|||
|
|
||||

Г л а в а 5. Химическая кинетика |
339 |
Пример 23-2. Найдите константу Михаэлиса и максимальную скорость гидролиза аденозинтрифосфата, катализируемого миозином, по следующим кинетическим данным:
|
0,25 |
|
|
|
0,20 |
|
|
-1 |
|
|
|
с |
0,15 |
|
|
-1 |
|
|
|
мольл |
0,10 |
|
|
, |
|
|
|
|
|
|
|
5 |
|
|
|
r 10 |
0,05 |
|
|
|
0,00 |
|
|
|
0 |
5r / [S] 103, c-110 |
15 |
Решение. Уравнение Михаэлиса–Ментен в данных координатах имеет вид (23.16.б), следовательно, точки пересечения с осями имеют
координаты: (0; rmax) для оси ординат, (rmax/KM; 0) для оси абсцисс. Первая точка пересечения дает значение rmax = 2.1 10–6 моль л–1 с–1. Вторая
точка позволяет найти константу Михаэлиса:
rmax/KM = 14.6 10–3 с–1, KM = 2.1 10–6 / 14.6 10–3 = 1.44 10–4 моль л–1.
Пример 23-3. Ферментативная реакция (KM = 2.7 10–3 моль л–1) подавляется конкурентным ингибитором (KI = 3.1 10–5 моль л–1). Концентрация субстрата равна 3.6 10–4 моль л–1. Сколько ингибитора понадобится для подавления реакции на 65%? Во сколько раз надо повысить концентрацию субстрата, чтобы уменьшить степень подавления до 25%?
Решение. 1) Конкурентное ингибирование описывается формулами (23.17) и (23.18). 65%-ное подавление реакции означает, что скорость ингибируемой реакции составляет 35% от скорости реакции в отсутствие ингибитора:
rmax [S] |
|
|
= 0.35 |
rmax [S] |
|
, |
|||||
|
|
|
|
||||||||
|
|
[I] |
|
|
K |
|
+[S] |
|
|||
KM 1 |
+ |
|
0 |
|
+[S] |
|
M |
|
|
|
|
KI |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
откуда следует, что
KM 1+ |
[I]0 |
+[S] = |
1 |
(KM +[S]) . |
|
KI |
0.35 |
||||
|
|
|
В этой формуле известны значения KM, KI и [S]. Концентрация ингибитора равна:
[I]0 |
= |
0.65 |
KI |
[S] |
+1 =6.5 10–5 моль л–1. |
0.35 |
|
||||
|
|
|
KM |
||

340 |
Г л а в а 5. Химическая кинетика |
Уменьшение степени ингибирования до 25% означает, что скорость ингибируемой реакции составляет 75% от нормальной:
rmax [S] |
|
|
= 0.75 |
rmax [S] |
|
, |
|||||
|
|
|
|
||||||||
|
|
[I] |
|
|
K |
M |
+ [S] |
|
|||
KM 1 |
+ |
|
0 |
|
+ [S] |
|
|
|
|
||
KI |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
где в данном случае известны KM, KI и [I]0. Отсюда можно выразить искомую концентрацию субстрата:
|
|
[I] |
|
|
|
1 |
|
|
|
|
|
|
KM |
0 |
+ 1 |
− |
|
|
|
|
|
||
|
|
KI |
0.75 |
|
|
|
|||||
|
|
|
|
|
|
|
|
–2 |
–1 |
||
[S] = |
|
|
|
|
|
|
|
|
= 1.4 10 |
|
моль л . |
|
|
1 |
|
− |
1 |
|
|
|
|||
|
|
|
|
|
|
|
|
||||
|
|
0.75 |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|||
Таким образом, для уменьшения степени ингибирования до 25% концентрацию субстрата надо увеличить в 1.4 10–2 / 3.6 10–4 = 40 раз.
Пример 23-4. Простейшая схема активации ферментативной реакции описывается уравнениями:
E + S |
|
KS |
|
ES |
k2 |
|
E + P , |
KS = [E][S] / [ES] , |
||
|
|
KA |
|
|
||||||
ES + A |
|
ESA |
βk2 |
E + P + A , |
KA = [ES][A] / [ESA] . |
|||||
|
|
|
|
|
||||||
где A – активатор, β > 1, KS – константа диссоциации комплекса фер- мент–субстрат, KA – константа диссоциации комплекса фермент– субстрат–активатор.
Используя квазиравновесное приближение для комплексов ES и ESA, определите параметры уравнения Михаэлиса–Ментен. Во сколько раз эффективная максимальная скорость больше максимальной скорости ферментативной реакции без активатора?
Решение. Для нахождения скорости реакции образования продукта запишем систему из четырех уравнений:
1)определение скорости,
2)материальный баланс по ферменту, 3)-4) константы двух квазиравновесий:
|
d[P] |
|
|
|
|
|
|
|
|
r = |
|
= k2 [ES] + βk |
2 |
[ESA] |
|||||
dt |
|||||||||
|
|
|
|
|
|
|
|
||
[E]0 = [E] + [ES] + [ESA] |
|||||||||
|
|
|
KS |
|
|
|
|
|
|
|
= [ES] |
|
|
|
|
|
|||
[E] |
|
|
|
|
|
|
|||
[S] |
|
|
|
|
|
||||
|
|
|
|
[A] |
|
|
|||
|
|
|
|
|
|
||||
[ESA] = |
[ES] |
|
|
|
|
|
|||
|
K A |
|
|
||||||
|
|
|
|
|
|
|
|||

Г л а в а 5. Химическая кинетика |
341 |
Подставляя концентрации фермента и комплекса ESA в выражение для начальной концентрации фермента, находим текущие концентрации комплексов ES и ESA:
[ES] = |
|
[E]0 |
|
, |
|
KS |
+ 1 |
+ |
[A] |
||
|
[S] |
K A |
|
||
|
|
|
|
||
[ESA] = [ES] [A] .
K A
С помощью этих концентраций выражаем скорость образования продукта:
|
r = k2 [ES] + βk2 [ESA] = |
|
k2 [E]0 |
|
+ β |
[A] |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
. |
||||||||||||||
|
KS |
|
|
|
|
[A] |
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
K A |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
1 + |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
[S] |
K A |
|
|
|
|
|||||||||
|
Максимальную скорости активируемой реакции находим, устремив |
|||||||||||||||||||||||||||
[S] к бесконечности: |
|
|
|
|
|
1 + β |
[A] |
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
r |
= k |
2 |
[E] |
0 |
|
|
|
|
|
|
KA . |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
max |
|
|
|
1 + |
|
[A] |
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
KA |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
Эта скорость больше максимальной скорости неактивируемой реак- |
|||||||||||||||||||||||||||
|
|
|
1 + β |
[A] |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
ции k2[E]0 в |
|
|
|
K A |
раз. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
1 |
+ |
[A] |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
K A |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
Подставляя |
rmax в r и |
приводя |
полученное |
выражение к виду: |
|||||||||||||||||||||||
r = |
rmax [S] |
|
, находим аналог константы Михаэлиса для активируемой |
|||||||||||||||||||||||||
K M + [S] |
||||||||||||||||||||||||||||
реакции: |
|
|
|
|
|
|
|
|
|
|
|
KS |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
K M = |
|
|
|
|
. |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
[A] |
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
1 + |
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
K A |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Пример 23-5. Напишите кинетические уравнения для двухсубстратной реакции на поверхности катализатора. Рассмотрите два случая:
а) реакция протекает между двумя адсорбированными реагентами; б) один из субстратов реагирует из газовой фазы.
Решение. а) Скорость химической реакции между двумя субстратами на поверхности
S1(адс) + S2(адс) → P(адс) + адс. центр

342 |
Г л а в а 5. Химическая кинетика |
пропорциональна произведению их степеней заполнения, которые определяются уравнением Ленгмюра (23.22):
r = kθS1 θS2 = |
kKL,S KL,S |
|
pS |
pS |
|||
(1+ KL,S |
pS |
+ KL,S |
pS |
+ KL,P pP )2 . |
|||
|
|
|
1 |
2 |
1 |
2 |
|
|
1 |
1 |
|
2 |
2 |
|
|
б) Если один из субстратов реагирует непосредственно из газовой фазы:
S1(адс) + S2(газ) → P(адс),
то скорость реакции пропорциональна степени заполнения одного субстрата и давлению другого и, с учетом уравнения Ленгмюра, кинетическое уравнение имеет вид:
r = kθS |
pS |
|
= |
|
kKL,S |
pS |
pS |
. |
|
1 |
1 |
2 |
|||||
|
|
|
|
|
||||
1 |
|
2 |
|
|
1+ KL,S pS + KL,P pP |
|
||
|
|
|
|
|
|
|
||
|
|
|
|
1 |
1 |
|
|
|
ЗАДАЧИ
23-1. Докажите, что если бы катализатор влиял на положение химического равновесия, то можно было бы построить вечный двигатель второго рода, то есть полностью превращать теплоту химической реакции в работу в циклическом процессе.
23-2. При каких условиях уравнение (23.2) описывает кинетику реакции: а) второго, б) третьего порядка?
23-3. Пиролиз ацетальдегида в газовой фазе характеризуется энергией активации 190 кДж моль–1. В присутствии катализатора – паров иода – энергия активации уменьшается до 136 кДж моль–1. Во сколько раз воз-
растает скорость реакции в присутствии паров иода при 200 °С?
23-4. Представьте соотношение (23.9) между k и h0 в линейной форме, позволяющей определить параметры k2 и Kb с помощью линейной регрессии.
23-5. Опишите кинетику реакции специфического основного катализа в квазиравновесном приближении. Выразите скорость образования продукта через:
а) текущую, б) исходную концентрацию субстрата.
Как зависит эффективная константа скорости от pH? Коэффициенты активности и активность воды примите равными единице.
Г л а в а 5. Химическая кинетика |
343 |
23-6. Используя корреляционные соотношения Бренстеда для общего кислотного катализа, найдите связь между энергией активации каталитической реакции и энергией Гиббса ионизации катализатора.
23-7. Для радикальных реакций в газовой фазе экспериментально обнаружена линейная зависимость между энергией активации E и тепловым эффектом ∆H:
E = α + β∆H.
Определите параметры этой зависимости для элементарных реакций паров натрия с хлорпроизводными метана, пользуясь следующими данными:
R−Cl |
Энергия связи R−Cl, |
Энергия активации реакции, |
|
кДж моль–1 |
RCl + Na → R + NaCl, кДж моль–1 |
CH3Cl |
349 |
37.0 |
CH2Cl2 |
328 |
20.5 |
CHCl3 |
308 |
8.4 |
CCl4 |
286 |
0 |
NaCl |
411 |
– |
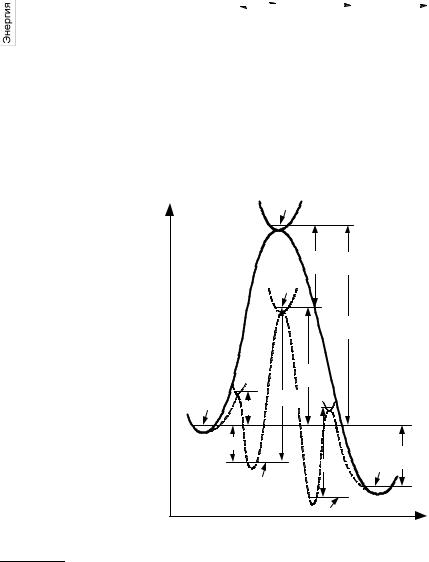
23-8. Для теоретического объяснения линейной зависимости E = α + β∆H (см. задачу 23-7) используют простую модель, в которой химическую реакцию рассматривают как движение частицы по координате реакции, причем зависимость энергии исходных веществ и продуктов реакции от этой координаты – линейная:
Eреаг(x) = a|x|, Eпрод(x) = b|x – R| + ∆H.
Найдите связь между параметрами α и β и параметрами модели a, b и R.
23-9. Гидролиз ацетилхолина катализируется ферментом ацетилхолинэстеразой, число оборотов которой составляет 25000 с–1. Сколько времени потребуется ферменту для расщепления одной молекулы ацетилхолина?
23-10. Изобразите график зависимости скорости ферментативной реакции от концентрации субстрата. Как по графику определить константу Михаэлиса?
23-11. Составьте систему кинетических уравнений для схемы Михаэлиса ферментативной реакции и численно решите ее при значениях пара-
метров:
k1 = 0.83 105, k–1 = 10–4, k2 = 104, [S]0 = 1, [E]0 = 10–4.
Постройте графики зависимости концентраций всех веществ от времени.
