
7 семестр / Основы_физич_химии_Теория_и_задачи_Еремин_и_др_2005_480с
.pdf
404 |
Г л а в а 6. Элементы неравновесной термодинамики |
Разделим обе части этого выражения на объем, V, и продифференцируем по времени, t,:
|
1 δ iQ |
1 di S |
|
|
|
|
|
1 dξ |
|
|
||||||||||||
|
|
dt = T |
|
|
|
|
|
= |
A |
|
|
|
|
|
≥ 0 . |
|
|
|||||
V |
V |
dt |
V |
dt |
|
|
||||||||||||||||
Сравнивая выражения |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
σ = ∑J iYi / T и σ = |
A |
1 dξ |
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
, |
||||||||||||||
|
|
|
||||||||||||||||||||
|
|
i |
|
|
|
|
|
|
|
T |
V dt |
|
|
|||||||||
можно сделать вывод, что в случае химической реакции поток J равен |
||||||||||||||||||||||
|
|
|
J = |
1 |
|
dξ |
. |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
V |
|
dt |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Производная V1 ddtξ характеризует изменение количества вещества в
единицу времени в единичном объеме, т.е. представляет собой ско-
рость химической реакции. Ответ. J = r.
Пример 27-2. Получите выражение для производства энтропии (V = 1) как функции времени, если в системе протекает элементарная обратимая реакция первого порядка
A B.
В начальный момент времени в системе присутствует только вещество А (концентрация а0). Константа скорости прямой реакции равна k1, а обратной k2. Постройте графики зависимости производства энтропии от времени и химического сродства от химической переменной (ξ).
Решение. Производство энтропии в единичном объеме связано с химическим сродством соотношением (см. предыдущую задачу):
di S = A dξ . dt T dt
Для обратимой реакции A B скорость реакции в единице объема равна
dξ |
r |
s |
= k1 (a0 |
− ξ)− k2 ξ = (k1 |
|
k1a0 |
|
|
|
= r |
− r |
+ k2 ) |
|
− ξ |
, |
||
dt |
|
|||||||
|
|
|
|
k1 + k2 |
|
|
||
где r, r – скорости прямой и обратной реакций.
Химическое сродство связано с константой равновесия реакции следующим образом:
− A = µ B − µ A = µ oB − µ oA |
+ RTln |
aB |
= −RT ln K + RTln |
γ B cB |
. |
aA |
|
||||
|
|
|
γ A cA |
||

Г л а в а 6. Элементы неравновесной термодинамики |
405 |
|||||||||||
Если система близка к идеальной (γi = 1), то |
|
|
|
|
|
|||||||
− A = RT ln k2 + RT ln cB = RT ln k2cB = RT ln rr . |
|
|||||||||||
k1 |
|
cA |
|
|
|
k1cA |
|
|
r |
|
|
|
Подставляя в исходную формулу выражения для А и |
|
dξ , получаем |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
dt |
|
формулу для расчета производства энтропии в единичном объеме: |
|
|||||||||||
di S |
= A dξ |
|
|
r |
s |
|
|
|
|
|
|
|
= R (r |
− r)ln rs . |
|
|
|
|
|
||||||
dt |
T dt |
|
|
|
|
|
r |
|
|
|
|
|
Конкретизируем выражения для скорости прямой и обратной реак- |
|
|||||||||||
ций. При интегрировании дифференциальной формы кинетического |
|
|||||||||||
уравнения обратимой реакции 1-го порядка получаем |
|
|
|
|
|
|||||||
|
k a |
(1− e |
−(k +k |
)t |
). |
|
|
|
|
|
||
ξ = k1 1+ k0 2 |
|
1 2 |
|
|
|
|
|
|
||||
Тогда |
|
|
|
|
|
|
|
|
|
|
|
|
rr − rs = k1a0e−(k1 + k2 )t |
и |
rs |
= |
|
k1 + k2 |
|
|
) |
. |
|
||
|
|
|
r |
k2 |
(1− e−(k1 +k2 )t |
|
|
|||||
Производство энтропии в единичном объеме составит |
|
|
||||||||||
di S = Rk1a0e−(k1 + k2 )t ln |
|
k1 + k2 |
) |
. |
|
|
|
|||||
dt |
|
|
k2 (1− e−(k1 + k2 )t |
|
|
|
|
|||||
Графики функций di S |
= f (t) |
и A = f(ξ) представлены ниже. |
|
|||||||||
dt |
|
|
|
|
|
|
|
|
|
|
|
|
di S |
|
|
|
|
|
|
A |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
dt |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
ξe |
ξ |
|
|
|
|
t |
|
|
|
|
|
|
|
|
Пример 27-3. В системе единичного объема протекает обратимая |
|
|||||||||||
элементарная реакция |
|
|
|
|
|
|
|
|
|
|
|
|
|
A |
B. |
|
|
|
|
|
|
|
|
||

406 |
Г л а в а 6. Элементы неравновесной термодинамики |
Константы скорости прямой и обратной реакций одинаковы и равны k. В начальный момент времени в системе присутствует только исходное вещество (a0). Определите коэффициент Онсагера.
Решение. Для элементарной химической реакции обобщенная сила равна химическому сродству A, а поток – скорости химической реакции:
Jr = r = V1 ddtξ .
Учитывая связь между скоростями реакций и химическим сродством
dξ |
r |
s |
A = RT ln |
r |
||
|
= r |
− r , |
s |
, |
||
dt |
||||||
|
|
|
r |
|||
получаем для скорости обратимой одностадийной реакции: r = r (1 − e− A / RT ).
При равновесии A = 0, вблизи состояния равновесия A/RT << 1. Разлагая в ряд выражение для скорости реакции с учетом только первого слагаемого, получаем:
r = rrравн RTA + ...
Сравнивая полученное выражение с феноменологическим соотношением
r = ∑Li A
i
приходим к выводу, что
L = r равн = k(a0 − ξ e ) .
RT RT
Пример 27-4. Докажите, что для самопроизвольного неравновесного процесса, в котором действуют две силы, неотрицательному значению функции диссипации соответствуют неотрицательные значения прямых коэффициентов Онсагера.
Решение. В рассматриваемом случае функция диссипации:
Ψ= J1Y1 + J2Y2 = (L11Y1 + L12Y2)Y1 + (L21Y1 + L22Y2)Y2 = L11Y12 + (L12 + L21)Y1Y2 + L22Y22.
Сучетом соотношений взаимности можно записать:
Ψ = L11Y12 + 2L12 Y1Y2 + L22Y22 .
Функция диссипации Ψ будет неотрицательной, если
L11 ≥ 0, L22 ≥ 0 и L11 L22 ≥ L122 ,
что и требовалосьдоказать.
Г л а в а 6. Элементы неравновесной термодинамики |
407 |
§ 28. Сильно неравновесные системы
Состояние равновесных и слабо неравновесных систем однозначно определяется принципами экстремумов: максимума энтропии или минимума производства энтропии. Для сильно неравновесных систем
общего экстремального принципа нет: такие системы развиваются не-
предсказуемо, при одних и тех же начальных условиях сильно неравновесная система может переходить к разным состояниям.
Изменение во времени (динамика) неравновесных систем описывается дифференциальными уравнениями общего вида:
dx |
= F(x, λ, t) , |
(28.1) |
|
dt |
|||
|
|
где x(t) – набор переменных, характеризующих систему (например, концентрации веществ); λ – набор так называемых управляющих параметров, которые зависят от условий эксперимента (например, скорость потока или разность температур).
Если следить за поведением системы не непрерывно, а через некоторые промежутки времени, то дифференциальное уравнение (28.1) можно заменить эквивалентным разностным уравнением:
xn 1 = F(xn , λ) , |
(28.2) |
+ |
|
где функция x(t) берется только в определенные моменты времени:
xn = x(tn).
Все многообразие динамических явлений в системах, описываемых уравнениями (28.1) и (28.2), определяется видом функции F. Самые интересные и нетривиальные явления происходят там, где функция F нелинейна, а число переменных – больше одной. Такие системы способны проявлять качественно разные типы поведения: от строго регулярного, периодического и предсказуемого до полностью хаотического. Переход от одного типа поведения к другому происходит при изменении управляющих параметров или начальных условий. Такое поведение характерно для сильно неравновесных систем, где большую роль играет нелинейная зависимость потоков от сил.
Простейшим примером, демонстрирующим зависимость поведения нелинейной системы от управляющих параметров, служит логистическое отображение
xn+1 = rxn(1 – xn), |
(28.3) |
которое описывает динамику биологической популяции в замкнутой среде. Здесь xn – численность популяции за n-й год наблюдения (значения xn обычно нормируют на единичный интервал), r – параметр, зави-
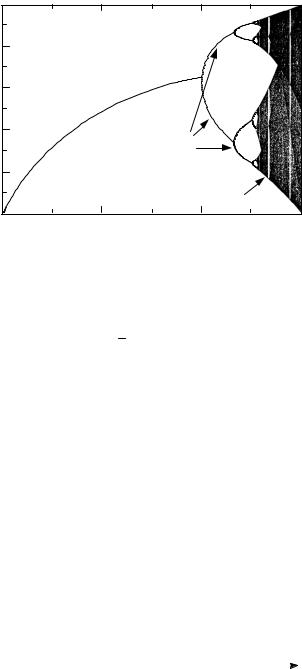





Г л а в а 6. Элементы неравновесной термодинамики |
413 |
Определим их устойчивость.
1) Вблизи X0 = 0, Y0 = 0 система уравнений в линейном приближении имеет тривиальный вид:
|
dX |
|
= k1 AX |
|
|
|
|
|
|
|
dt |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
dY |
|
= −k3Y |
|
|
|
|
|
|
dt |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
и решение, которое является неустойчивым по координате X: |
||||||||
X (t) = X (0) exp (k |
1 |
At ) |
||||||
|
|
|
|
t ) . |
||||
Y (t) = Y (0) exp (−k |
3 |
|||||||
|
|
|
|
|
||||
|
|
|
|
|
|
|
||
Любая небольшая флуктуация числа «жертв» – X – будет экспоненциально возрастать со временем, поэтому данное стационарное состояние неустойчиво.
2) Вблизи ненулевого стационарного состояния система уравнений приобретает вид:
|
dx |
|
= −k3 y |
|
dt |
||||
, |
||||
|
||||
dy |
|
= k1 Ax |
||
|
|
|
||
dt |
|
|
||
где x = X – X0 и y = Y – Y0 – отклонения от стационарного состояния. Для этой системы уравнение на собственные значения (28.6) выгля-
дит следующим образом:
−λ |
−k3 |
|
= 0 |
||
k1 A |
−λ |
|
и имеет чисто мнимые, комплексно сопряженные корни:
λ1,2 = ±i(k1k3A)1/2.
Это соответствует нейтральной устойчивости. В стационарном состоянии переменные X и Y испытывают периодические колебания с частотой (k1k3A)1/2. При малом возмущении этого состояния система перейдет в другое стационарное состояние с периодическими колебаниями.
В этой системе управляющие параметры не влияют на устойчивость стационарных состояний.
Ответ. Двастационарных состояния– неустойчивоеинейтральное.
Пример 28-2. Нелинейная динамическая система Пуанкаре описывается уравнениями:
dx |
|
= αx + βy − x(x |
2 |
+ y |
2 |
) |
|
|||
|
|
|
|
|
|
|||||
dt |
|
|
. |
|||||||
|
|
|
|
|
|
|
|
|
||
dy |
|
= −βx + αy − y(x |
2 |
+ y |
2 |
) |
||||
|
|
|
|
|
||||||
dt |
|
|
|
|
|
|
|
|
|
|
