
1038
.pdfДополнительная энергия, расходуемая на разрушение образцов с метастабильным аустенитом, может быть рассчитана как разность между энергетическими затратами на разрушение с фазовым переходом G1dS и без него G1dS:
δГ = (G1 −G1′)dS, |
(15) |
где G1 и G1′ – интенсивность высвобождающейся энергии при фазовом переходе и без него соответственно, для случая плоской деформации G1 и G1′; dS − площадь поверхности
разрыва, которая составляла (0,50 – 0,55)10– 4 м2.
В этом случае величина δГ, вычисленная по формуле (15), по мере увеличения концентрации никеля принимает значения 0,19 кДж/моль, 0,46 кДж/моль и 0,58 кДж/моль. Отличие значений δГ и ∆Z не превышает 20 %.
Таким образом, в концентрационно-неоднородных порошковых сталях превращение метастабильного аустенита в мартенсит деформации при нагружении способствует как повышению прочности за счет роста напряжений, достаточных для раскрытия характерных дефектов, так и повышению трещиностойкости за счет дополнительных энергетических затрат, необходимых для структурных превращений, которые, в свою очередь, обусловлены изменением термодинамического потенциала зоны разрушения.
31
ELIB.PSTU.RU
Глава 2 СТРУКТУРА И СВОЙСТВА ПОРОШКОВЫХ СТАЛЕЙ,
МЕХАНИЧЕСКИ ЛЕГИРОВАННЫХ ХРОМОМ
ИАЗОТОМ
2.1.Превращения в системе железо – хром
Вотличие от марганца и никеля хром относится к группе легирующих элементов, которые сужают γ-область. Чистый хром во всём интервале температур от точки плавления до абсолютного нуля имеет кристаллическую решётку объ- ёмно-центрированного куба, следовательно, является изомор-
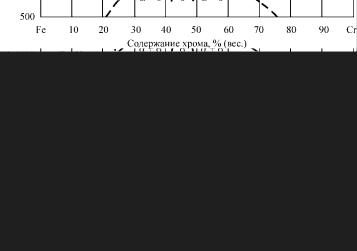
фным α-железу. Рассматривая систему железо – хром (рис. 4), следует отметить, что к замкнутой области γ-твёрдых растворов при относительно высоких содержаниях хрома примыкает гетерогенная область α(σ) + γ-твёрдых растворов, за которой вплоть до чистого хрома следует непрерывный ряд α(σ)- твёрдых растворов. Следовательно, в температурном интервале существования γ-фазы интерметаллических соединений
Рис. 4. Система железо – хром
32
ELIB.PSTU.RU
не имеется. В гетерогенной α+γ-области при температурах выше 900 °С более богатые хромом α-твёрдые растворы находятся в равновесии с более бедными хромом γ-твёрдыми растворами; наоборот, при температурах от 900 до 850 °С в области от 0 до 8,5 % Cr γ-твёрдый раствор богаче хромом, чем α-твёрдый раствор. Отсюда следует практический вывод о том, что во всех случаях, когда в легированных многими элементами железохромистых сплавах появляется смешанная α+γ-структура, кристаллы α-фазы обогащены хромом, хотя предельные концентрации и не могут быть указаны. При образовании такой смешанной структуры в процессе термической обработки хромистых сплавов может появиться расслоение (ликвация), которое сохраняется и после устранения смешанной структуры, если только не будет снова осуществлена полная гомогенизация сплава путём длительного нагрева при высоких температурах (выше 900 °С). Следует обратить внимание на то обстоятельство, что при относительно низких содержаниях хрома (приблизительно до 8 %) температура A3 примерно до 850° снижается и только потом – при
дальнейшем увеличении содержания хрома – сильно повышается. Таким образом, γ-область замыкается примерно при 12 % Cr и температуре 1000 °С. В соответствии с этим в богатых железом сплавах наряду со снижением температуры A3 при увеличении содержания хрома до 8 % наблюдается повышение температуры магнитного превращения (точки Кюри) α-фазы примерно до 5 %, и только затем эта температура начинает снижаться. По влиянию хрома на положение γ-области в сплавах железо – хром (равно как и в хромистой стали) можно выделить три группы сплавов:
1)сплавы с γ→α-превращением;
2)сплавы без γ→α-превращения;
3)сплавы, претерпевающие лишь частичное превращение (со смешанной структурой).
33
ELIB.PSTU.RU
Сплавы первой группы, содержащие также углерод и претерпевающие превращение при охлаждении из γ-облас- ти, относятся к перлитному и мартенситному классам, сплавы второй группы – к ферритному, третьей – полуферритному классам. Ферритом в сплавах железо – хром и в хромистой стали в литературе называют как α- так и σ-твердые растворы.
При температурах выше 900 °С и содержании хрома свыше 13 % сплавы кристаллизуются в виде непрерывного ряда твёрдых растворов во всей области концентраций, при более низких температурах появляется новая фаза. Эта новая фаза, которую обычно называют σ-фазой, наблюдается на диаграмме состояния при содержании хрома в среднем 45 % (вес.) 47 % (атомн.) и приблизительно отвечает составу соединения FeCr. С понижением температуры область существования σ-фазы распространяется на более широкий интервал концентрации относительно указанного среднего состава; это означает, что в σ-фазе могут растворяться значительные количества хрома или железа и что, таким образом, она не имеет точного стехиометрического состава. Гомогенная область σ-твердых растворов ограничивается гетерогенной двухфазной областью. В сплавах с соответствующей концентрацией хрома σ-фаза образуется при длительном нагреве на температуры примерно от 600 до 800° (при весьма длительных нагревах и после предшествующей холодной деформации также и при более низких температурах, вплоть до 500 °С). В этой области температур σ-фаза неферромагнитна. Вследствие своей высокой твердости и хрупкости σ-фаза в хромистой стали является нежелательной структурной составляющей, хотя в отдельных случаях повышение твердости и износоустойчивости за счет σ-фазы может оказаться полезным.
34
ELIB.PSTU.RU
2.2. Сплавы железо – хром – углерод
Физические и технические свойства сплавов железо– хром – углерод обусловлены, по существу, двумя важными свойствами хрома как легирующего элемента:
•ограничением γ-области;
•большой склонностью к образованию карбидов, особенно к образованию специальных карбидов.
Сродство хрома углероду оказывается более сильным, чем сродство железа, что обусловливает образование в структуре стали более устойчивых специальных карбидов. Из возникающих в системе хром – углерод карбидов – кубического
карбида Cr23C6, тригонального карбида Cr7C3 и орторомбического карбида Cr3С2 – в практически применяемых углеродсодержащих сплавах железо – хром наблюдаются только пер-
вые два; карбид Cr3С2 в этих сплавах пока не обнаружен. Карбид Cr3С2 наиболее богат углеродом, а карбид Cr23C6 является самым бедным. Помимо названных карбидов в сплавах с малым содержанием хрома обнаруживаются сложные
карбиды цементитного типа (FeCr)3C.
В цементите растворяется значительное количество хрома, согласно исследованиям он доходит до 18–20 % Cr. Рав-
ным образом карбид хрома Cr7C3 также может растворять приблизительно от 30 до 50 % железа, а карбид хрома Cr23C6 до 35 % железа. При этом так же, как и вообще в твёрдых растворах замещения, под «растворением» следует понимать замещение атомов железа в карбидах атомами хрома и обратное явление. Это обстоятельство учитывается при сле-
дующем способе записи: (Fe, Cr)3C, (Fe, Cr)7C3 и (Fe, Cr)23C6
[2].В низкоуглеродистой стали с содержанием хрома менее 3 % в карбиды входит очень небольшое количество хрома, который почти целиком находится в твердом растворе с железом.
35
ELIB.PSTU.RU

Карбид (Fe, Cr)3C существует в стали перлитного класса с содержанием хрома до 5 %. При нагреве стали этот карбид начинает растворяться при переходе α-железа в γ-железо. Карбиды (Fe, Cr)7C3 и (Fe, Cr)23C6 образуются в высокохромистой стали мартенситного и карбидного классов. Температура диссоциации этих карбидов около 1200 °С [1]. На рис. 5 приведён состав карбидов, электролитически выделенных из хромистых сталей с 0,8–1,0 % С и 0,1–24 % Cr.
Рис. 5. Состав карбидов, выделенных из хромистой стали, содержащей 0,8–1,2 % С [2]
При низких содержаниях хрома γ-область наблюдается даже в безуглеродистых сплавах; при низких содержаниях углерода и высоких содержаниях хрома наблюдается непрерывный ряд α-твёрдых растворов от температуры плавления до весьма низких температур. При более высоком содержа-
36
ELIB.PSTU.RU

нии углерода область α-твёрдых растворов отделяется от γ-области гетерогенной α+γ-областью.
Взаимодействие хрома и углерода проявляется в смещении границ замкнутой γ-области в системе железо – хром. Растворимость углерода в аустените понижается при легировании хромом; с другой стороны, при образовании карбидов последние обогащаются хромом, а твёрдый раствор, соответственно, им обедняется. В системе железо − хром (т.е. в безуглеродистых сплавах) граница замкнутой гомогенной γ-фазы находится примерно при 12 % Cr. Если хром сужает область γ-фазы, то углерод её расширяет (систему железо − углерод). Противоположное влияние этих элементов на положение γ-области видно по данным рис. 6, где показано, как при различном содержании хрома и углерода меняется область существования гомогенной аустенитной фазы в равновесном состоянии, т.е. после полного растворения карбидов.
Рис. 6. Область существования γ-фазы в хромистой стали в зависимости от содержания углерода при различных содержаниях хрома
37
ELIB.PSTU.RU
Из этого следует, что с увеличением содержания хрома наблюдается интенсивное сужение области гомогенной γ-фазы. При этом γ-область может граничить: при высоком содержании углерода с двухфазными областями γ+карбиды и γ+расплав; низком содержании углерода с двухфазными областями α+γ и (σ)α+γ. Верхние острия областей на рис. 6 представляют собой границу трёхфазной области α+γ+расплав, нижние острия – границы трёхфазной области α+γ+карбиды. При низком содержании углерода резко проявляется влияние хрома на ограничение γ-области, при высоком содержании углерода сказывается способность хрома как карбидообразующего элемента связывать углерод в нерастворимые карбиды. То обстоятельство, что в углеродистых сплавах еще при 15 и 19 % Cr имеется, хотя и ограниченная по объему область гомогенного γ-твердого раствора, свидетельствует о том, что граница гомогенной γ-области, которая в безуглеродистых сплавах лежит при 12 % Cr, смещается под влиянием углерода к значительно более высоким содержаниям хрома. Приведенные на рис. 6 соотношения справедливы только для гомогенной γ-области и только для состояния равновесия. Области, в которых γ-твердый раствор существует наряду с α-твердым раствором и карбидами, в данном случае не рассматриваются. Так, например, в сплаве 0,25 % С и 25 % Cr при нагревании на 1250 °С наряду с ферритом образуется ещё до 50 % аустенита. Не учитывается также и влияние местных обогащений твердого раствора хромом и углеродом, которые получаются при растворении карбидов хрома; эти обогащения ликвидируются в результате диффузионного выравнивания лишь после длительного нагрева. Местные обогащения могут приводить к образованию незначительных количеств аустенита, особенно по границам зерен. При этом можно полагать, что при не слишком высоких температурах углерод располагается предпочтительно вблизи атомов хрома [2].
38
ELIB.PSTU.RU
2.3. Порошковые хромистые стали
Для порошковых сталей легирование хромом представляет интерес ввиду эффективности его воздействия и достаточной распространенности. Сдерживает внедрение хромистых сталей высокое сродство хрома кислороду. Хром вводят в шихту в виде лигатур. Чаще всего с этой целью используют порошки сталей Х30, Х13, иногда феррохром. Используют также порошки сплавов, полученные распылением или диффузионным насыщением из точечных источников [1]. Свойства спеченных хромистых сталей в значительной степени зависят от способа введения хрома и формирующейся в зависимости от этого структуры.
Отличительной особенностью хрома является высокая устойчивость его оксидов, температура диссоциации которых достигает почти температуры плавления хрома. Наличие оксидов затрудняет протекание диффузионных процессов, а спекание необходимо проводить при высоких температурах
востроосушенных восстановительных средах (водороде, реже – в диссициированном аммиаке). Поэтому структура спеченных хромосодержащих сталей отличается сильной гетерогенностью и наличием фаз, которые по среднему составу сплава не отвечают равновесной диаграмме состояния [3].
Пластичность материалов из легированных порошков
втри-четыре раза выше, чем у материалов из смесей порошков. Прочность на разрыв находится примерно на одном уровне для низколегированных сталей и несколько выше для высоколегированных. Низкая пластичность и снижение прочности высоколегированных хромистых сталей, полученных смешиванием порошков, связаны с повышенной гетерогенностью структуры. Уменьшение гетерогенности структуры может быть достигнуто увеличением дисперсности исходных порошков или применением менее концентрированных добавок. Свойства железохромового сплава [4], по-
39
ELIB.PSTU.RU
лученного путем введения порошка Х30 различной дисперсности в отожженное карбонильное железо, приведены в табл. 16. С увеличением дисперсности порошков свойства стали повышаются.
Таблица 16
Механические свойства спеченного железохромового сплава
(Tсп = 1300 °С, t = 3 ч)
Дисперсность |
Плот- |
σВ, МПа |
σ0,2, МПа |
δ, % |
ψ, % |
порошков, мкм |
ность, % |
||||
72/40 |
94/98 |
340/430 |
260/300 |
6,4/7,3 |
4,1/4,9 |
5/40 |
94/98 |
480/640 |
399/500 |
4,4/5,2 |
2,9/3,8 |
|
|
|
|
|
|
5/5 |
94/98 |
580/720 |
490/580 |
3,9/4,9 |
2,4/2,9 |
|
|
|
|
|
|
Примечание. В числителе – добавка порошка Х30, в знаменателе – порошок железа.
В работе [5] изучали свойства стали 20X13, полученной механическим смешиванием порошка X13 с графитом при последующем прессовании и спекании. После спекания сталь имела σB = 190…300 МПа, δ = 4…6 %. После закалки от
1100 °С и отпуска при 550–750 °С произошло значительное увеличение прочности – до 590–700 МПа с уменьшением пластичности до 3–4 %. Для получения стабильной структуры и высокого уровня прочностных характеристик предпочтительным является использование гомогенных порошков легированных сталей.
Хромистые спеченные стали широко используются как износостойкие и антифрикционные материалы. В работе [6] установлено уменьшение величины объемного изнашивания при введении в спеченные стали специальных хромистых карбидов. Наибольшую износостойкость имели стали, со-
40
ELIB.PSTU.RU
