
- •Химия воды и микробиология Учебно-методическое пособие к практическим занятиям
- •Введение
- •Химия воды
- •Понятие о растворах. Процесс растворения. Растворимость веществ
- •Решение типовых задач
- •Задачи для самостоятельной работы
- •Количественная характеристика состава раствора
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •1.3. Электролитическая диссоциация. Степень и константа диссоциации
- •Задачи для самостоятельного решения
- •1.4. Свойства кислот, оснований и солей с точки зрения теории электролитической диссоциации
- •Задачи для самостоятельного решения
- •1.5. Диссоциация воды. Водородный показатель
- •Задачи для самостоятельного решения
- •1.6. Гидролиз солей
- •I. Соли, образованные сильным основанием и слабой кислотой
- •II. Соли, образованные слабым основанием и сильной кислотой
- •III. Соли, образованные слабым основанием и слабой кислотой
- •Задачи для самостоятельного решения
- •1.7. Коллоидные растворы
- •Контрольные вопросы
- •1.8. Окислительно-восстановительные реакции
- •Задачи для самостоятельного решения
- •2. Физические и химические свойства технологических процессов водоподготовки
- •2.1. Физико-химическая характеристика природных вод
- •2.2. Физические, химические, биологические показатели качества воды
- •Физико-химические основы коагулирования примесей воды
- •2.4. Коагулянты и флокулянты применяемые для осветления воды
- •2.5. Обеззараживание воды
- •Хлорирование воды.
- •2.5.2. Озонирование воды
- •2.5.3. Применение сильных окислителей и сорбентов. Осаждение
- •2.6. Характеристика бытовых и производственных сточных вод
- •Тест №1
- •3. Микробиология
- •3.1. Основы общей микробиологии
- •3.2. Морфологическая характеристика отдельных групп микроорганизмов
- •1) Меноидный слой с выступами и бугорками; 2) ликополисахаридный слой; 3) каналы; 4) молекулы белка; 5) плотный гликопептидный слой; 6) цитоплазматическая мембрана
- •8) Капсула; 9) мембрана протопласта.
- •3.3. Питание бактерий
- •3.4. Ферменты
- •3.5. Химический состав бактерий
- •3.6. Участие микроорганизмов в круговороте веществ в природе
- •3.7. Водоросли, грибы, простейшие, коловратки, черви и микробактерии
- •5) Surirella saxonica (образование ауксоспор); 6) Asterionella gracillima; 7) Pleurosigma attenuatum; 8) Didymosphenia geminata
- •3.8. Влияние внешних факторов на микробов
- •Тест №2
- •4. Санитарная микробиология
- •4.1. Санитарно-бактериологические методы анализа воды
- •4.2 Физические и физико-химические показатели состава воды
- •4.3. Химические и биохимические показатели
- •Примеси в коллоидном и твердом состояниях
- •Общая минерализация и общая загрязненность воды
- •Примеси в растворенном и коллоидном состояниях
- •Щелочность. Углекислотное равновесие воды
- •Тест №3
- •4.4. Индикаторная роль бактерий группы кишечной палочки
- •5. Биологические факторы самоочищения водоемов
- •6. Вредная деятельность микроорганизмов в системах водоснабжения
- •Тест №4
- •7. Сточные воды и методы их очистки
- •7.1. Очистные сооружения
- •11) Песчаные фильтры; 12) хлораторная; 13) контактный резервуар.
- •7.2. Сооружения механической очистки
- •7.3. Сооружения для биологической очистки.
- •7.4. Аэробные процессы очистки сточных вод
- •7.5. Анаэробные процессы очистки сточных вод
- •7.6. Биологические пруды
- •Тест № 5
- •Заключение
- •Библиографический список
- •Химия воды и микробиология Учебно-методическое пособие к практическим занятиям
Задачи для самостоятельного решения
1.
Какими свойствами — окислительными
или восстановительными —обладают ионы
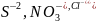 ,
атомы фосфора, фтора, алюминия?
,
атомы фосфора, фтора, алюминия?
2. Составить электронное уравнения, расставить коэффициенты в уравнениях, указать, какие вещества являются окислителями, какие — восстановителями:
а)
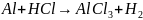 ;
;
б)
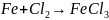 ;
;
в)
 ;
;
г)
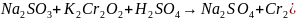 ;
;
д)
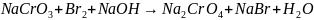 .
.
3. Методом электронного баланса составить уравнения окислительно-восстановительных реакций, протекающих по схемам:
а)
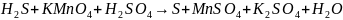 ;
;
б)
 ;
;
в)
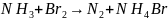 ;
;
г)
 .
.
2. Физические и химические свойства технологических процессов водоподготовки
2.1. Физико-химическая характеристика природных вод
Источниками централизованного водоснабжения являются поверхностные и подземные воды. Поверхностные воды — реки, озера, водохранилища — содержат различные примеси, зависящие от климатических и геоморфологических факторов, почвенно-геологических условий. Состав подземных вод зависит от условий их деформирования.
В состав воды входят соли, органические вещества, газы, диспергированные примеси, гидробионты, бактерии и вирусы. Во взвешенном состоянии в природных водах содержатся глинистые, песчаные, гипсовые и известковые частицы, в коллоидном — различные вещества органического происхождения, гидроксид железа (III).
По А.О. Алехину, химический состав природных вод подразделяется на пять групп:
1)
главные ионы, содержащиеся в наибольшем
количестве (натрий
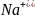 ,
калий
,
калий
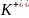 ,
кальций
,
кальций
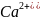 ,
магний
,
магний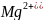 ,
сульфаты
,
сульфаты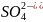 ,
карбонаты
,
карбонаты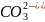 ,
хлориды
,
хлориды
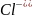 ,
гидрокарбонаты
,
гидрокарбонаты
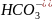 );
);
2)
растворенные газы (азот
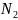 ,
кислород
,
кислород
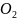 ,
диоксид углерода
,
диоксид углерода
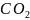 ,
сероводород
и др.);
,
сероводород
и др.);
3) биогенные элементы (соединения фосфора, азота, кремния);
4) микроэлементы — соединения всех остальных химических элементов;
5) органические вещества.
В
отличие от поверхностных, подземные
воды характеризуются небольшим
количеством органических веществ и
значительным содержанием минеральных
солей, а иногда и растворенных газов
(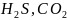 ).
).
Для определения качества воды производят физические, химические, бактериологические, биологические и технологические анализы в наиболее характерные для данного водоисточника периоды времени года.
2.2. Физические, химические, биологические показатели качества воды
В зависимости от целевого назначение к воде предъявляют разнообразные требования, согласно которым ее можно классифицировать для хозяйственно-питьевых целей, коммунальных предприятий, а также для нужд пищевой и некоторых других отраслей промышленности.
Хозяйственно-питьевая вода должна быть безвредной для здоровья человека, иметь хорошие органолептические показатели и быть пригодной для использования в быту.
В табл. 4 приведены показатели качества хозяйственно-питьевой воды соответствующие требованиям СанПиН 2.1.4.1074-01 «Питьевая вода. Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения. Контроль качества» и ГОСТ Р 51232-98 «Вода питьевая. Общие требования к организации и методам контроля качества»
Таблица 4
Требования к качеству хозяйственно-питьевой воды
Показатели |
Единицы измерения |
Норматив |
Органолептические |
||
Мутность |
мг/л |
до 1,5 |
Цветность |
град. |
до 20 |
Запахи и привкусы при 29 °С |
баллы |
до 2 |
Химические |
||
Водородный показатель |
— |
6,5…8,5 |
Общая жесткость |
мг-экв/л |
до 7 |
Фтор |
мг/л |
0,7…1,5 |
Железо |
мг/л |
до 0,3 |
Марганец |
мг/л |
до 0,1 |
Бериллий |
мг/л |
до 0,0002 |
Молибден |
мг/л |
до 0,5 |
Мышьяк |
мг/л |
до 0,05 |
Свинец |
мг/л |
до 0,1 |
Селен |
мг/л |
до 0,001 |
Стронций |
мг/л |
до 2 |
Радий-226 |
Ки/л |
1,2* |
Хлориды |
мг/л |
до 30 |
Сульфаты |
мг/л |
до 500 |
Сухой остаток |
мг/л |
до 1000 |
Остаточный алюминий |
мг/л |
до 0,5 |
Медь |
мг/л |
до 1 |
Цинк |
мг/л |
до 5 |
Гексаметафосфат |
мг/л |
до 3,5 |
Триполифосфат |
мг/л |
до 3,5 |
Полиакриламид |
мг/л |
до 2 |
Нитраты |
мг/л |
до 10 |
Биологические |
||
Общее количество бактерий в 1 мл |
— |
до 100 |
Коли-индекс |
— |
до 3 |
Коли-титр |
— |
более 300 |

