- •Химия воды и микробиология Учебно-методическое пособие к практическим занятиям
- •Введение
- •Химия воды
- •Понятие о растворах. Процесс растворения. Растворимость веществ
- •Решение типовых задач
- •Задачи для самостоятельной работы
- •Количественная характеристика состава раствора
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •1.3. Электролитическая диссоциация. Степень и константа диссоциации
- •Задачи для самостоятельного решения
- •1.4. Свойства кислот, оснований и солей с точки зрения теории электролитической диссоциации
- •Задачи для самостоятельного решения
- •1.5. Диссоциация воды. Водородный показатель
- •Задачи для самостоятельного решения
- •1.6. Гидролиз солей
- •I. Соли, образованные сильным основанием и слабой кислотой
- •II. Соли, образованные слабым основанием и сильной кислотой
- •III. Соли, образованные слабым основанием и слабой кислотой
- •Задачи для самостоятельного решения
- •1.7. Коллоидные растворы
- •Контрольные вопросы
- •1.8. Окислительно-восстановительные реакции
- •Задачи для самостоятельного решения
- •2. Физические и химические свойства технологических процессов водоподготовки
- •2.1. Физико-химическая характеристика природных вод
- •2.2. Физические, химические, биологические показатели качества воды
- •Физико-химические основы коагулирования примесей воды
- •2.4. Коагулянты и флокулянты применяемые для осветления воды
- •2.5. Обеззараживание воды
- •Хлорирование воды.
- •2.5.2. Озонирование воды
- •2.5.3. Применение сильных окислителей и сорбентов. Осаждение
- •2.6. Характеристика бытовых и производственных сточных вод
- •Тест №1
- •3. Микробиология
- •3.1. Основы общей микробиологии
- •3.2. Морфологическая характеристика отдельных групп микроорганизмов
- •1) Меноидный слой с выступами и бугорками; 2) ликополисахаридный слой; 3) каналы; 4) молекулы белка; 5) плотный гликопептидный слой; 6) цитоплазматическая мембрана
- •8) Капсула; 9) мембрана протопласта.
- •3.3. Питание бактерий
- •3.4. Ферменты
- •3.5. Химический состав бактерий
- •3.6. Участие микроорганизмов в круговороте веществ в природе
- •3.7. Водоросли, грибы, простейшие, коловратки, черви и микробактерии
- •5) Surirella saxonica (образование ауксоспор); 6) Asterionella gracillima; 7) Pleurosigma attenuatum; 8) Didymosphenia geminata
- •3.8. Влияние внешних факторов на микробов
- •Тест №2
- •4. Санитарная микробиология
- •4.1. Санитарно-бактериологические методы анализа воды
- •4.2 Физические и физико-химические показатели состава воды
- •4.3. Химические и биохимические показатели
- •Примеси в коллоидном и твердом состояниях
- •Общая минерализация и общая загрязненность воды
- •Примеси в растворенном и коллоидном состояниях
- •Щелочность. Углекислотное равновесие воды
- •Тест №3
- •4.4. Индикаторная роль бактерий группы кишечной палочки
- •5. Биологические факторы самоочищения водоемов
- •6. Вредная деятельность микроорганизмов в системах водоснабжения
- •Тест №4
- •7. Сточные воды и методы их очистки
- •7.1. Очистные сооружения
- •11) Песчаные фильтры; 12) хлораторная; 13) контактный резервуар.
- •7.2. Сооружения механической очистки
- •7.3. Сооружения для биологической очистки.
- •7.4. Аэробные процессы очистки сточных вод
- •7.5. Анаэробные процессы очистки сточных вод
- •7.6. Биологические пруды
- •Тест № 5
- •Заключение
- •Библиографический список
- •Химия воды и микробиология Учебно-методическое пособие к практическим занятиям
Задачи для самостоятельного решения
1.
Изменяется ли окраска фенолфталеина в
растворе соли
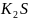 ?
Составьте молекулярное и ионное уравнения
гидролиза этой соли.
?
Составьте молекулярное и ионное уравнения
гидролиза этой соли.
2.
Составить молекулярное и ионное уравнения
гидролиза солей CaS,
Ca(CN
,
MgC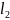 ,
,
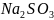 ,
.
,
.
3. Каково значение pH (больше или меньше 7) в растворах каждой из этих солей.
4. В одну пробирку налили раствор щелочи, в другую — раствор кислоты, в третью — раствор хлорида натрия NaCl. Как с помощью индикатора лакмуса определить, в какой из пробирок находится кислота, щелочь и хлорид натрия?
5. Составить молекулярное и ионное уравнения гидролиза солей, в результате которого образуется основная соль, кислая соль, слабое основание, слабая кислота.
6.
Изменится ли окраска индикатора
фенолфталеина в растворах следующих
солей:
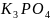 ,
,
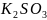 ,
(N
,
(N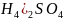 ,
AlC
,
AlC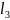 ?
Составить молекулярное и ионное уравнения
гидролиза этих солей.
?
Составить молекулярное и ионное уравнения
гидролиза этих солей.
1.7. Коллоидные растворы
В природе широко распространены дисперсные системы. Данные системы образуются при распределении одного вещества, находящегося в состоянии тонкого измельчения, в другом однородном веществе.
В дисперсионных системах существует дисперсная фаза — мелкораздробленное вещество и дисперсионная среда — однородное вещество, в котором равномерно распределена дисперсная фаза.
В зависимости от размера частиц дисперсной фазы дисперсионные системы классифицируются как показано на рис. 5.
Суспензии — дисперсные системы, в которых дисперсной фазой является твердое вещество, а дисперсионной фазой — жидкость, причем твердое вещество нерастворимо в жидкости.
Эмульсии — это дисперсные системы, в которых и дисперсионная фаза, и дисперсионная среда являются взаимно несмешивающимися жидкостями.
Коллоидные растворы, как видно из схемы (рис. 5), занимают промежуточное положение между грубодисперсными системами и истинными растворами.
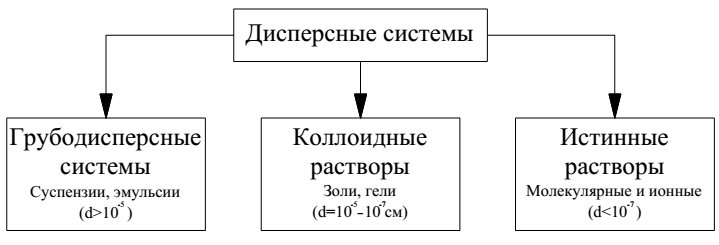
Рис. 5. Классификация дисперсных систем:
d — средний диаметр частиц дисперсионной фазы.
Коллоидные растворы — это высокодисперсные двухфазные системы.
В коллоидных растворах частицы дисперсной фазы представляют собой не молекулы и не ионы, а их сложные ассоциаты.
Коллоидные частицы называются мицеллами.
Рассмотрим процесс образования коллоидной частицы на примере взаимодействия очень разбавленных растворов нитрата серебра и йодида калия:
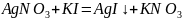 ;
;
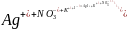 .
.
Молекулы йодида серебра нерастворимы, они образуют ядро коллоидной частицы. Это ядро имеет кристаллическую или аморфную структуру. Оно нерастворимо в дисперсной среде и состоит из нескольких тысяч нейтральных молекул или атомов, то есть m AgI. m[AgI] - ядро коллоидной частицы.
Данное
ядро адсорбирует на своей поверхности
те или иные ионы, которые имеются в
растворе. Адсорбируются обычно те ионы,
которые входят в состав ядра, в нашем
случае это ионы серебра или ионы йода.
Если раствор получали при избытке йодида
калия, то адсорбируются ионы йода, что
приводит к достройке кристаллической
решетки ядра с образованием адсорбционного
слоя и приданием ядру отрицательного
заряда
m[AgI]
n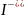 .
Адсорбирующийся ион называется
потенциалопределяющим ионом. В растворе
находятся также противоионы
.
Адсорбирующийся ион называется
потенциалопределяющим ионом. В растворе
находятся также противоионы
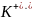 Они
электростатически притягиваются
потенциалопределяющими ионами
адсорбционного слоя и образуют (ядро +
адсорбционный слой) гранулы:
Они
электростатически притягиваются
потенциалопределяющими ионами
адсорбционного слоя и образуют (ядро +
адсорбционный слой) гранулы:
|
||
ядро |
|
адсорбционный слой гранула |
Оставшаяся часть противоионов образует диффузный слой ионов. Ядро с адсорбционным и диффузным слоями называется мицеллой:
|
||
гранула |
|
диффузионный слой |
При добавлении к коллоидным растворам (золям) электролитов происходит уменьшение заряда гранул, что приводит к слипанию частиц. Соединение коллоидных частиц в более крупные агрегаты называется коагуляцией.