
- •Химия воды и микробиология Учебно-методическое пособие к практическим занятиям
- •Введение
- •Химия воды
- •Понятие о растворах. Процесс растворения. Растворимость веществ
- •Решение типовых задач
- •Задачи для самостоятельной работы
- •Количественная характеристика состава раствора
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •1.3. Электролитическая диссоциация. Степень и константа диссоциации
- •Задачи для самостоятельного решения
- •1.4. Свойства кислот, оснований и солей с точки зрения теории электролитической диссоциации
- •Задачи для самостоятельного решения
- •1.5. Диссоциация воды. Водородный показатель
- •Задачи для самостоятельного решения
- •1.6. Гидролиз солей
- •I. Соли, образованные сильным основанием и слабой кислотой
- •II. Соли, образованные слабым основанием и сильной кислотой
- •III. Соли, образованные слабым основанием и слабой кислотой
- •Задачи для самостоятельного решения
- •1.7. Коллоидные растворы
- •Контрольные вопросы
- •1.8. Окислительно-восстановительные реакции
- •Задачи для самостоятельного решения
- •2. Физические и химические свойства технологических процессов водоподготовки
- •2.1. Физико-химическая характеристика природных вод
- •2.2. Физические, химические, биологические показатели качества воды
- •Физико-химические основы коагулирования примесей воды
- •2.4. Коагулянты и флокулянты применяемые для осветления воды
- •2.5. Обеззараживание воды
- •Хлорирование воды.
- •2.5.2. Озонирование воды
- •2.5.3. Применение сильных окислителей и сорбентов. Осаждение
- •2.6. Характеристика бытовых и производственных сточных вод
- •Тест №1
- •3. Микробиология
- •3.1. Основы общей микробиологии
- •3.2. Морфологическая характеристика отдельных групп микроорганизмов
- •1) Меноидный слой с выступами и бугорками; 2) ликополисахаридный слой; 3) каналы; 4) молекулы белка; 5) плотный гликопептидный слой; 6) цитоплазматическая мембрана
- •8) Капсула; 9) мембрана протопласта.
- •3.3. Питание бактерий
- •3.4. Ферменты
- •3.5. Химический состав бактерий
- •3.6. Участие микроорганизмов в круговороте веществ в природе
- •3.7. Водоросли, грибы, простейшие, коловратки, черви и микробактерии
- •5) Surirella saxonica (образование ауксоспор); 6) Asterionella gracillima; 7) Pleurosigma attenuatum; 8) Didymosphenia geminata
- •3.8. Влияние внешних факторов на микробов
- •Тест №2
- •4. Санитарная микробиология
- •4.1. Санитарно-бактериологические методы анализа воды
- •4.2 Физические и физико-химические показатели состава воды
- •4.3. Химические и биохимические показатели
- •Примеси в коллоидном и твердом состояниях
- •Общая минерализация и общая загрязненность воды
- •Примеси в растворенном и коллоидном состояниях
- •Щелочность. Углекислотное равновесие воды
- •Тест №3
- •4.4. Индикаторная роль бактерий группы кишечной палочки
- •5. Биологические факторы самоочищения водоемов
- •6. Вредная деятельность микроорганизмов в системах водоснабжения
- •Тест №4
- •7. Сточные воды и методы их очистки
- •7.1. Очистные сооружения
- •11) Песчаные фильтры; 12) хлораторная; 13) контактный резервуар.
- •7.2. Сооружения механической очистки
- •7.3. Сооружения для биологической очистки.
- •7.4. Аэробные процессы очистки сточных вод
- •7.5. Анаэробные процессы очистки сточных вод
- •7.6. Биологические пруды
- •Тест № 5
- •Заключение
- •Библиографический список
- •Химия воды и микробиология Учебно-методическое пособие к практическим занятиям
2.5.3. Применение сильных окислителей и сорбентов. Осаждение
Реакции окисления и восстановления, в процессе очистки воды, используют для перевода токсичных и вредных примесей в нетоксичные или нерастворимые.
Осаждение химическим способом приводит к образованию малорастворимых соединений, выпадающих в осадок в соответствии с их пределом растворимости. Например, процесс умягчения воды (снятие местности) с применением извести Са(OH)2 или соды Na2CO3, а также фосфатное умягчение с Na3РO4, что приводит к удалению сульфатов, фторидов, фосфатов, кремневой кислоты и многих других веществ.
Так, при добавлении в воду извести протекают реакции перехода углекислоты последовательно в бикарбонаты и карбонаты, что приводит к устранению кальциевой и магниевой карбонатной жесткости:
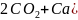 ;
;
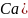 ;
;
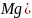 .
.
Одновременно магниевые соли некарбонатной жесткости переводятся в кальциевые:
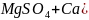 ;
;
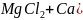 .
.
Следовательно, в результате известкования карбонатная жесткость воды снижается до предела, который определяется растворимостью СаCO3 и Мg(OH)2.
Для ускорения осаждения СаCO3 и Мg(OH)2 добавляется коагулянт FeCl3 или FeSO4. Как уже отмечалось, реагентное умягчение воды проводится с помощью извести совместно с содой.
Применение соды обусловливает дополнительное введение карбонат-ионов, что приводит к выпадению в осадок солей кальция:
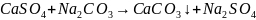 ;
;
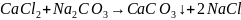 .
.
Фосфатное доумягчение можно записать следующим образом:

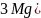
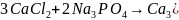

Умягчение воды проводится также методом обмена ионов с помощью ионитов — веществ, способных к сорбционному обмену ионов с раствором электролита. Ионообменные сорбенты могут быть минерального и органического происхождения. К минеральным ионитам относятся различные амоносиликаты, силикаты, гидрат окиси алюминия и другие.
В настоящее время для очистки воды широкое применение нашли ионообменные смолы — это сетчатые трехмерные полимеры, не растворяющиеся в воде и содержащие ионогенные группы, то есть группы, способные к обмену ионов.
По характеру действия ионообменные вещества разделяются на катиониты и аниониты. Если происходит обмен катионами, то такие вещества называются катионитами, а обменивающие анионы — анионитами.
Катиониты
способны диссоциировать на небольшие,
подвижные и способные к ионному обмену
катионы (например, Н+)
и высокомолекулярный анион (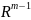 ),
а аниониты дают мелкие, легко
перемешивающиеся анионы (например,
)
и высокомолекулярный катион (
),
а аниониты дают мелкие, легко
перемешивающиеся анионы (например,
)
и высокомолекулярный катион (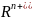 ).
).
Схему диссоциации катионитов и анионитов можно представить следующей схемой:
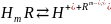
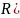
При катионировании через Na-катионит происходят следующие процессы:

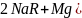

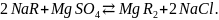
Как видно из данных схем, катионы кальция и магния, обусловливающие карбонатную и сульфатную жесткость воды, сорбируются на катионите, то есть удаляются из воды.
2.6. Характеристика бытовых и производственных сточных вод
Сточными называются воды, которые необходимо удалять с территории населенных мест и промышленных предприятий.
Сточные воды можно разделить на хозяйственно-бытовые, промышленные и атмосферные.
Бытовые сточные воды образуются за счет жизнедеятельности людей (унитазы, ванные, приготовление пищи и т.д.). Они имеют относительно постоянный состав. Биологическое потребление кислорода (БПК5) для этих вод зависит от степени их загрязненности и в течение суток колеблется от 100 до 400 мг/л.
Основной загрязняющей составляющей бытовых стоков являются органические вещества растительного и животного происхождения. К неорганическим загрязнениям можно отнести: песок, глину, минеральные соли, минеральные масла и др.
Бытовые сточные воды в основном содержат различные микроорганизмы: бактерии, дрожжевые и плесневые грибы, яйца гельминтов, вирусы и др.
С.Н. Строганов вывел эмпирическую формулу, по которой определяют концентрацию загрязнений (с, мг/л) в бытовых стоках:
|
(7) |
|
|
|
|
где |
1000 — коэффициент перехода от грамма к миллиграммам. |
|
Среднее значение загрязнений, приходящихся на 1 человека в сутки (см. табл. 5):
Таблица 5
Средние значения загрязнений, приходящихся на 1 человека в сутки
Ингредиент |
, г |
Взвешенные вещества |
65 |
Азот
аммонийный ( |
8 |
Хлориды |
9 |
Фосфаты |
1,7 |
БПКполн отстоянной воды |
40 |
Промышленные сточные воды образуются на предприятиях в процессе производства, промывки цехов и оборудования и т.д.
Промышленные стоки очень разнообразны по своему составу. Способы очистки таких вод требуют специального подхода. Так, стоки гальванических цехов содержат в своем составе ядовитые вещества. Сточные воды кожевенных заводов могут содержать возбудителей сибирской язвы.
Атмосферные или ливневые сточные воды образуются в результате выпадения осадков. Они загрязнены органическими и минеральными веществами.
Анализ сточной воды идет иначе, чем анализ питьевых природных вод.
Отобранный образец сточной воды анализируется в тот же день. При поступлении сточной воды на очистные канализационные сооружения производят следующие анализы:
1) определяют температуру;
2) определяют окраску;
3) определяют запах;
4) определяют прозрачность по шрифту;
5) определяют рН среды;
6) определяют объём осадка в цилиндрах Лисенко через 5, 10, 15, 30, 60 и 120 минут;
7) определяют относительную стабильность по обесцвечиванию метиле-новой сини;
8) определяют концентрацию взвешенных веществ с делением их на летучую (при t = 900 – 1000 °C) и нелетучую части;
9) определяют массовую долю сухой части так же с делением на летучую и нелетучую части;
10) определяют БПК3, БПКполн;
11) определяют общую кислотность и щелочность воды при титровании с различными индикаторами;
12) определяют частичную окисляемость (по KMnO4);
13) определяют химическое потребление кислорода (ХПК).

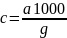 ,
,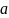 — количество
загрязнений данного вида, приходящееся
на 1 человека в сутки;
— количество
загрязнений данного вида, приходящееся
на 1 человека в сутки;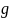 — норма
водоотведения на 1 человека в сутки;
— норма
водоотведения на 1 человека в сутки;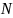 )
)