
- •Химия воды и микробиология Учебно-методическое пособие к практическим занятиям
- •Введение
- •Химия воды
- •Понятие о растворах. Процесс растворения. Растворимость веществ
- •Решение типовых задач
- •Задачи для самостоятельной работы
- •Количественная характеристика состава раствора
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •1.3. Электролитическая диссоциация. Степень и константа диссоциации
- •Задачи для самостоятельного решения
- •1.4. Свойства кислот, оснований и солей с точки зрения теории электролитической диссоциации
- •Задачи для самостоятельного решения
- •1.5. Диссоциация воды. Водородный показатель
- •Задачи для самостоятельного решения
- •1.6. Гидролиз солей
- •I. Соли, образованные сильным основанием и слабой кислотой
- •II. Соли, образованные слабым основанием и сильной кислотой
- •III. Соли, образованные слабым основанием и слабой кислотой
- •Задачи для самостоятельного решения
- •1.7. Коллоидные растворы
- •Контрольные вопросы
- •1.8. Окислительно-восстановительные реакции
- •Задачи для самостоятельного решения
- •2. Физические и химические свойства технологических процессов водоподготовки
- •2.1. Физико-химическая характеристика природных вод
- •2.2. Физические, химические, биологические показатели качества воды
- •Физико-химические основы коагулирования примесей воды
- •2.4. Коагулянты и флокулянты применяемые для осветления воды
- •2.5. Обеззараживание воды
- •Хлорирование воды.
- •2.5.2. Озонирование воды
- •2.5.3. Применение сильных окислителей и сорбентов. Осаждение
- •2.6. Характеристика бытовых и производственных сточных вод
- •Тест №1
- •3. Микробиология
- •3.1. Основы общей микробиологии
- •3.2. Морфологическая характеристика отдельных групп микроорганизмов
- •1) Меноидный слой с выступами и бугорками; 2) ликополисахаридный слой; 3) каналы; 4) молекулы белка; 5) плотный гликопептидный слой; 6) цитоплазматическая мембрана
- •8) Капсула; 9) мембрана протопласта.
- •3.3. Питание бактерий
- •3.4. Ферменты
- •3.5. Химический состав бактерий
- •3.6. Участие микроорганизмов в круговороте веществ в природе
- •3.7. Водоросли, грибы, простейшие, коловратки, черви и микробактерии
- •5) Surirella saxonica (образование ауксоспор); 6) Asterionella gracillima; 7) Pleurosigma attenuatum; 8) Didymosphenia geminata
- •3.8. Влияние внешних факторов на микробов
- •Тест №2
- •4. Санитарная микробиология
- •4.1. Санитарно-бактериологические методы анализа воды
- •4.2 Физические и физико-химические показатели состава воды
- •4.3. Химические и биохимические показатели
- •Примеси в коллоидном и твердом состояниях
- •Общая минерализация и общая загрязненность воды
- •Примеси в растворенном и коллоидном состояниях
- •Щелочность. Углекислотное равновесие воды
- •Тест №3
- •4.4. Индикаторная роль бактерий группы кишечной палочки
- •5. Биологические факторы самоочищения водоемов
- •6. Вредная деятельность микроорганизмов в системах водоснабжения
- •Тест №4
- •7. Сточные воды и методы их очистки
- •7.1. Очистные сооружения
- •11) Песчаные фильтры; 12) хлораторная; 13) контактный резервуар.
- •7.2. Сооружения механической очистки
- •7.3. Сооружения для биологической очистки.
- •7.4. Аэробные процессы очистки сточных вод
- •7.5. Анаэробные процессы очистки сточных вод
- •7.6. Биологические пруды
- •Тест № 5
- •Заключение
- •Библиографический список
- •Химия воды и микробиология Учебно-методическое пособие к практическим занятиям
3.3. Питание бактерий
Питательные вещества, необходимые для жизнедеятельности микроорганизмов, попадают внутрь клетки путем осмотического всасывания через поры клеточной оболочки. Так как поры клеточной оболочки малы, то для проникновения через них питательных веществ, эти вещества должны быть измельчены до молекулярного состояния.
В процессе микробная клетка выделяет в среду биологические катализаторы — ферменты. Под действием ферментов происходит растворение питательных веществ до молекулярного уровня.
После поступления в клетку питательные вещества идут на синтез белков, жиров и углеводов. Часть из них идет на рост клетки, другая расходуется в процессе дыхания микроорганизмов.
Неиспользованные клеткой питательные вещества, переводятся в растворимое состояние и выводятся из клетки через поры в среду.
Типы питания микробов чрезвычайно разнообразны. По способу питания микробы делятся на три группы:
1. Автотрофные — бактерии, использующие углерод неорганических соединений: углекислоты и карбонаты.
Энергию необходимую для жизнедеятельности они получают или при фотосинтезе (усвоении углекислоты зелеными растениями и пурпурными серными бактериями), или хемосинтезе — путем окисления аммония, серы, нитратов, солей железа (II) и др. К этому типу бактерий относятся нитрифицирующие бактерии, железобактерии, бесцветные серные бактерии и тионовокислые.
2. Гетеротрофные — бактерии для синтеза своего организма требуют готовые органические вещества. К этой группе относится большинство микробов — гнилостные бактерии, микробы брожения, плесневые грибы, дрожжи и актиномицеты.
3. Паратрофные — этот тип бактерий для своего питания нуждается в живом белке, в эту группу входят все болезнетворные микробы.
3.4. Ферменты
Это биокатализаторы, синтезируемые живой клеткой. Они, как и любые катализаторы, снижают энергию активации системы путем образования неустойчивых промежуточных соединений с субстратом.
Ферменты по своей природе являются белковыми комплексами. На активность ферментов влияют различные факторы. При резких изменениях температуры и среды, повышении осмотического давления, избыточной концентрации субстрата и т.д. происходит снижение активности ферментов. Наиболее активными ферменты являются при температуре 25-35 °С. При температуре 55-60 °С большинство ферментов разрушается.
Посторонние вещества так же влияют на активность ферментов. Те вещества, которые активизируют ферменты, называются активизаторами, а замедляющие — ингибиторами.
Молекулы большинства ферментов состоят из двух составных частей- белковой части носителя и небелковой части-кофермент.
Одни ферменты действуют вне клетки микроорганизма- эктоферменты, и действующие внутри клетки — эндоферменты.
На рис. 12 схематически представлен механизм действия эктоферментов.

Рис. 12. Схема действия эктофермента:
а) апофермент (белковая часть фермента); б) кофермент (небелковая часть, обладающая специфической активностью); в) фермент; г) временное соединение фермента с субстратом; д) расщепленный субстрат
Все ферменты (энзимы) по характеру своей деятельности можно разделить на 6 классов:
1. Оксидоредуктазы — эти ферменты катализируют окислительно-восстановительные реакции.
2.
Гидролазы — способствуют обменному
разложению внутри-молекулярных связей
в органических веществах с молекулами
воды по уравнению
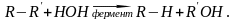
3. Трансферазы — ферменты, способствующие переносу различных химических групп с одной молекулы на другую.
4. Лиазы — ферменты, ускоряющие реакции образования двойных связей или присоединение атомов по месту двойных связей.
5. Изомеразы — ферменты, катализирующие изомерные превращения веществ.
6. Лигазы — ферменты, ускоряющие процессы синтеза белков, нуклеиновых и жирных кислот и других органических соединений, образующихся в живой клетке.
