
- •Н.А. Андреева
- •Введение
- •Сведения о материальных средах
- •1. Системы микрочастиц
- •1.1 Случай классических частиц
- •1.2. Вырожденные коллективы частиц
- •1.2.1. Фермионы
- •1.2.2 Бозоны
- •2. Кристаллические твердые тела
- •2.1 Трехмерные кристаллические системы
- •Индексы Миллера и кристаллографические направления
- •2. 2 Классификация дефектов
- •2.2.2 Дислокации и их движение
- •Плотность дислокаций
- •Взаимодействие дефектов
- •Физические свойства твердых тел
- •3. Тепловые свойства.
- •3.1. Теплоемкость твердого тела
- •3.1.1. Область низких температур
- •Теплоемкость электронного газа
- •3.2. Тепловое расширение твердых тел
- •3.3. Теплопроводность
- •4. Электрические свойства
- •4.1. Дрейф электронов
- •4.2. Время релаксации
- •4.3. Закон Видемана - Франца
- •4.4. Температурная зависимость подвижности носителей
- •4.5. Электропроводность чистых металлов
- •I II III Рис. 4. 4 Температурная зависимость удельного сопротивления металла ост
- •5. Электрон - электронное взаимодействие.
- •5.1. Взаимодействие электронов
- •5.1.1. Какие электроны участвуют во взаимодействии?
- •5.2. Основное состояние сверхпроводника
- •5.2.1. Энергия основного состояния
- •5.3. Энергетическая щель
- •6. Механические свойства.
- •6.1. Деформация растяжения
- •6.1.1. Расчет технической прочности при хрупком разрушении
- •6.2. Пути повышения прочности
- •7. Магнитные свойства твердых тел
- •7.1. Магнетизм веществ
- •7.1.1. Ферромагнетизм
- •7.1.2 Магнитные материалы
- •7.2. Парамагнетизм
- •7.2.1. Теория Ланжевена
- •7.3. Диамагнетизм
- •Получение низких и сверхнизких температур. Низкотемпературные жидкости.
- •8. Физические основы охлаждения.
- •8.1. Изоэнтропное расширение
- •8.2. Дросселирование сжатого газа
- •8.3. Расширение из постоянного объема
- •8.4. Десорбционное охлаждение
- •8.5. Откачка паров кипящей жидкости
- •9. Получение низких температур
- •Конструкция поршневого детандера
- •10. Получение сверхнизких температур
- •10.1 Метод адиабатического размагничивания
- •Криостат
- •10.2. Метод растворения 3Не в 4Не
- •1 0. 3. Метод Померанчука.
- •Энтропия
- •Криостат
- •11. Низкотемпературные жидкости.
- •11.1 Свойства криогенных жидкостей
- •1 1.2. Сверхтекучесть 4Не
- •11.3. Квантовые жидкости
- •11.4. Температурные волны
- •11.5. Квантовая жидкость 3Не
- •Библиографический список
- •Оглавление
10.2. Метод растворения 3Не в 4Не
Э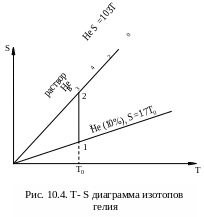 ффект
охлаждения при растворении гелия -3 в
гелии - 4 возникает из-за большой разницы
молярных теплоемкостей и энтропий
жидкого гелия 3 и его слабого раствора
в Не4.
ффект
охлаждения при растворении гелия -3 в
гелии - 4 возникает из-за большой разницы
молярных теплоемкостей и энтропий
жидкого гелия 3 и его слабого раствора
в Не4.
Как видно из рис. 10.4, где представлена температурная зависимость энтропии изотопов гелия. Верхняя линия соответствует зависимости энтропии гелия - 3 в растворе с 4Не от температуры, а нижняя прямая – зависимость энтропии от температуры для чистого 3Не. При изотермическом переходе системы из состояния 1 с энтропией S1 к состоянию 2 с энтропией S2 в соответствии с термодинамическим соотношением поглощается тепло
Q = То (S2 - S1) = То (103 То -17 То) = 86То2.
Откуда видно, что с понижением температуры в квадратичной зависимости от нее падает холодопроизводительность цикла.
О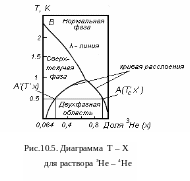 хлаждение
при растворении гелия - 3 в гелий - 4
аналогично адиабатическому размагничиванию.
Роль внешнего магнитного поля играет
внутреннее взаимодейтвие системы при
высокой концентрации гелия - 3,
устанавливающего термодинамический
"порядок" (малая энтропия). В этом
процессе растворения расстояние между
частицами гелия - 3 увеличивается,
взаимодействие уменьшается (ослабляется)
и должен наступить большой беспорядок,
компенсация которого возможна только
за счет снижения температуры.
хлаждение
при растворении гелия - 3 в гелий - 4
аналогично адиабатическому размагничиванию.
Роль внешнего магнитного поля играет
внутреннее взаимодейтвие системы при
высокой концентрации гелия - 3,
устанавливающего термодинамический
"порядок" (малая энтропия). В этом
процессе растворения расстояние между
частицами гелия - 3 увеличивается,
взаимодействие уменьшается (ослабляется)
и должен наступить большой беспорядок,
компенсация которого возможна только
за счет снижения температуры.
Таким образом, чистый жидкий 3Не имеет упорядоченную структуру и малую энтропию, тогда как свойства раствора гелия - 3 в гелии - 4 иные. Особенностью жидкого гелия 4Не является то, что вследствие сверхтекучести и почти нулевой энтропии при Т 0 (5 К) он гидродинамически и термически почти инертен и ведет себя в растворе 3Не - 4Не лишь как "поддерживающая" среда для атомов гелия - 3. Слабый раствор гелия - 3 и гелии - 4 можно рассматривать как идеальный газ, состоящий из атомов 3Не, которые между собой не взаимодействуют; удельная теплоемкость такого идеального газа равна 3/2R и велика его энтропия. Таким образом, растворение гелия - 3 в гелии - 4 приводит к изменению состояния упорядоченности системы.
Рассмотрим
диаграмму Т- X
для смеси 3Не
- 4Не,
которая показана на рис. 10.5. По оси
абсцисс отложена относительная
концентрация гелия - 3 в гелии - 4, (Х =
![]() ),
а по оси ординат – температура. Левая
ветвь диаграммы представляет предельную
концентрацию 3Не
в 4Не,
а правая же – предельную концентрацию
4Не
- 3Не.
Эти две ветви соединяются в точке с
координатами (0,8 К и 0,65) и образуют
область, в которой ниже Т = 0,8 К и содержание
компонентов Х от 0,064 до 0,9 не может
существовать однородный раствор 3Не
и 4Не.
В этой области будут отдельно сосуществовать
две жидкости, причем 3Не
как более легкая, находится в верхнем
слое. Фаза, богатая Не3,
играет роль жидкости, а фаза богатая
Не4
– роль пара; осмотическое давление
раствора эквивалентного давлению пара.
При этом легкая фракция не сверхтекучая,
а тяжелая – сверхтекучая. Выше верхней
точки (расслоение кончается), можно
провести
– линию, которая отделяет области, где
существует сверхтекучесть, и где ее
нет (справа от
– линии).
),
а по оси ординат – температура. Левая
ветвь диаграммы представляет предельную
концентрацию 3Не
в 4Не,
а правая же – предельную концентрацию
4Не
- 3Не.
Эти две ветви соединяются в точке с
координатами (0,8 К и 0,65) и образуют
область, в которой ниже Т = 0,8 К и содержание
компонентов Х от 0,064 до 0,9 не может
существовать однородный раствор 3Не
и 4Не.
В этой области будут отдельно сосуществовать
две жидкости, причем 3Не
как более легкая, находится в верхнем
слое. Фаза, богатая Не3,
играет роль жидкости, а фаза богатая
Не4
– роль пара; осмотическое давление
раствора эквивалентного давлению пара.
При этом легкая фракция не сверхтекучая,
а тяжелая – сверхтекучая. Выше верхней
точки (расслоение кончается), можно
провести
– линию, которая отделяет области, где
существует сверхтекучесть, и где ее
нет (справа от
– линии).
У
этих растворов есть замечательное
свойство: при
![]() максимальная возможная концентрация
3Не
в 4Не
не падает до нуля, а остается равной 6,5
%. Это и позволило создать эффективную
холодильную машину-криостат растворения
с помощью которой удается получать
температуру меньше 10-2
К.
максимальная возможная концентрация
3Не
в 4Не
не падает до нуля, а остается равной 6,5
%. Это и позволило создать эффективную
холодильную машину-криостат растворения
с помощью которой удается получать
температуру меньше 10-2
К.
Что в принципе ограничивает возможности понижения температуры гелия откачкой его паров. Падение плотности пара по закону Больцмана.
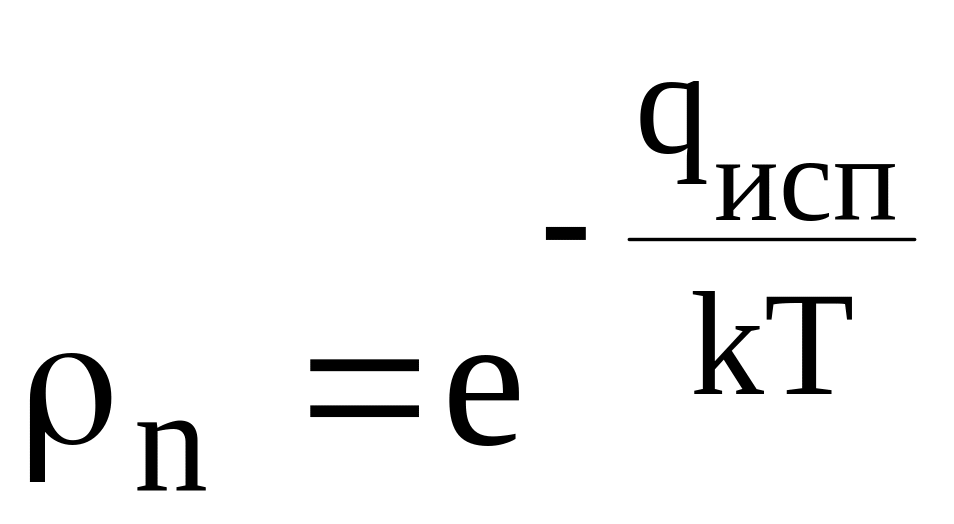 ,
,
где qисп – удельная теплота испарения.
При откачке гелия в единицу времени можно удалить количество пара m не больше
![]() ,
,
где
![]() - средняя тепловая скорость; А - сечение
трубы, по которой идет откачка, ρn
– плотность пара.
- средняя тепловая скорость; А - сечение
трубы, по которой идет откачка, ρn
– плотность пара.
Поэтому
и уносимое количество тепла
![]() ,
при низкой температуре становится
ничтожно малым из-за быстрого уменьшения
плотности пара. Но если в контакт с
жидким гелием - 4 привести жидкий гелий
– 3, то последний будет действовать как
"насос": Гелий - 3 будет как бы
испаряться, растворяясь в 4Не.
Плотность "пара" даже при
будет оставаться высокой.
,
при низкой температуре становится
ничтожно малым из-за быстрого уменьшения
плотности пара. Но если в контакт с
жидким гелием - 4 привести жидкий гелий
– 3, то последний будет действовать как
"насос": Гелий - 3 будет как бы
испаряться, растворяясь в 4Не.
Плотность "пара" даже при
будет оставаться высокой.
Однако существует проблема: теплота испарения, т.е. взятая с обратным знаком теплота растворения гелия - 3 в гелии - 4 уменьшается пропорционально температуре, и это уже не столь быстрое падение.
Принципиальная схема криостата растворения, вернее его рабочего объема без ванны с жидким азотом, показана на рис. 10.6. В ванне предварительного охлаждения находится жидкий азот, а во вторую ступень теплообменника залит изотоп гелия – 4 при температуре 1,2 К. Через оба теплообменника проходит прямой и обратный потоки газа гелий – 3.
Прямой поток гелий – 3, проходя по капилляру, охлаждается в ванне испарителя 2 и по трубке теплообменника 3 поступает в ванну растворения 4, где он растворяется в жидком гелии – 4, находящемся в сверхтекучем состоянии с энтропией равной нулю. Атомы гелия – 3 в этих условиях как бы расширяются в пустоту, поскольку не взаимодействуют со сверхтекучими атомами гелия – 4 и при таком расширении охлаждаются и могут поглотить тепло Q. Пространство для обратного потока в теплообменнике 3 и ванне 2 в основном заполнены сверхтекучим гелием – 4 и в этой среде атомы гелия -3 диффундируют из ванны растворения 4 в ванну испарения 2. Там за счет тепла, отбираемого от потока, протекающего по трубке и дополнительного подогрева qдоп продиффундировавший гелий – 3 испаряется и его пары откачиваются вакуумным насосом – цикл замыкается.
В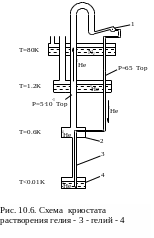 акуумный
насос откачивает пары чистого гелия -
3, и сжимает их до давления 60 – 70 Тор
(прямой поток в установку). Сжатый гелий
охлаждается в ванне жидкого азота до
80 К, затем в ванне с жидким 4Не
с температурой 1,2 К в теплообменнике ,
затем, пройдя по капилляру охлаждается
в ванне 2 испарителя до 0,6 К и теплообменнике
3 и поступает в ванну растворения 4, где
он растворяется в жидком гелии – 4,
находящемся в сверхтекучем состоянии
с энтропией равной нулю.
акуумный
насос откачивает пары чистого гелия -
3, и сжимает их до давления 60 – 70 Тор
(прямой поток в установку). Сжатый гелий
охлаждается в ванне жидкого азота до
80 К, затем в ванне с жидким 4Не
с температурой 1,2 К в теплообменнике ,
затем, пройдя по капилляру охлаждается
в ванне 2 испарителя до 0,6 К и теплообменнике
3 и поступает в ванну растворения 4, где
он растворяется в жидком гелии – 4,
находящемся в сверхтекучем состоянии
с энтропией равной нулю.
Вспомним о процессе ректификации, который применяется для разделения растворов, содержащих разные по летучести компоненты. Суть его в том, что если нагреть смесь из двух жидкостей, то относительное содержание более летучей компоненты в паре будет выше, чем в жидкости.
Для 6,5% смеси 3Не в 4Не при Т=0,5 0,8 К пар будет состоять из чистого 3Не, а плотность его будет примерно такая же, как и плотность пара над чистым жидким 3Не. Значит, его можно будет откачивать насосом и при этом поток газа будет достаточно большим.
Включив нагреватель в ванне испарения, сможем извлекать 3Не из раствора, т.е. очищать жидкий 4Не. Но ведь он находится в контакте с жидким 3Не и пока он не кончится, будет переходить в раствор, поддерживая концентрацию 6,5% и охлаждая ванну испарения. Для того чтобы процесс был непрерывным, необходимо возвращать 3Не, который откачивается насосом, возвращался назад. Для этого используется система теплообменников, один из которых 8 находится в ванне с 4Не в нем 3Не конденсируется охлаждаясь до ~1,2 К за счет откачки паров 4Не (на схеме не показано).
