
Учебное пособие 2150
.pdfспектральная линия соответствует максимуму на кривой
поглощения данного вещества; |
|
2. Фотоколориметрический анализ – |
основан на |
измерении интенсивности окраски стандартного раствора. 2а. Анализ, основанный на использовании рассеяния
света взвешенными частицами (нефелометрия).
2б. Анализ основан на поглощение света в результате светорассеяния (турбидиметрия).
3. Люминесцентный анализ основан на измерении вторичного излучения, возникающего в результате взаимодействия излучения с исследуемым веществом. При облучении ультрафиолетовым светом вещество дает вторичное излучение.
Наибольшее распространение получили фотометрические методы анализа, основанные на
поглощении в видимой области спектра, в интервале длин волн 400-760 нм. Это объясняется возможностью получения множества интенсивно окрашенных органических и неорганических соединений, пригодных для их фотометрического определения в видимой области спектра с помощью достаточно несложных и относительно недорогих приборов.
1. Спектральный анализ основан на исследовании спектров поглощения и испускания исследуемого вещества. Таким методом установлен состав Солнца и звезд. По интенсивности характеристических спектральных линий судят о количественном составе (1859 г. Немецкие ученые Бунзен и Кирхгоф).
Излучение света нагретыми твердыми телами можно наблюдать довольно часто. Когда нагревают кусок стали, то он вначале раскаляется и испускает красный свет; при более высокой температуре свечение становится белым. Этот белый свет состоит из всех цветов видимого спектра, такое излучение называется непрерывным. Если нагревать кристаллы NaI, то они испускают желтый свет, в состав этого
141
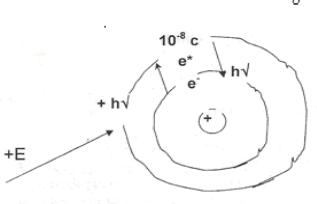
излучения входит, лишь несколько типов излучения катионов




 .
.
Природа излучения различна для различных веществ. Наиболее часто наблюдается линия испускания, соответствующая переходу из первого возбужденного состояния в основное, в состояние с наименьшей энергией. Подобную линию называют резонансной.
Преимущества метода: низкий предел обнаружения (до 10-5 %), экспрессность, для анализа требуется небольшое количество вещества, возможность проведения анализа на расстоянии (натриевый пояс Земли на расстоянии 80 км от поверхности был обнаружен этим методом). Однако по точности он уступает классическим методам.
Приборы: стилометры, стилоскопы, спектрографы и фоторегистрирующие квантометры.
2. Метод эмиссионной спектрометрии.
Метод основан – на способности атомов всех элементов испускать свет определенных длин волн.
Аналитический сигнал метода – интенсивность излучения светового потока I, мкА.
Условия проведения эксперимента – наличие источника возбуждения атомов (рис. 19, табл. 22).
▪ Определяют - катионы 



 ,
, 

 ,
, 



 ,
, 





 .
.
Рис. 19. Физическая основа метода
142
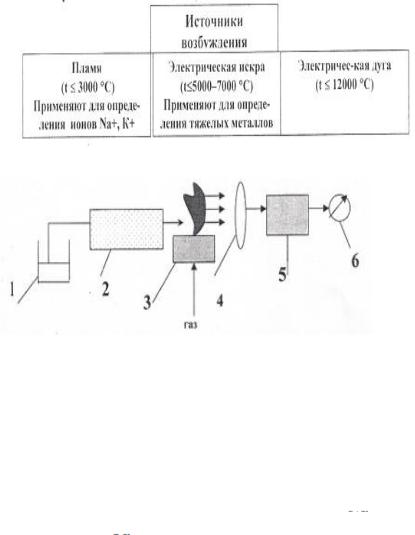
Таблица 22 Классификация источников возбуждения
3. Эмиссионный метод анализа (рис. 20).
Рис. 20. Принципиальная схема пламенно-эмиссионного фотометра: 1 – водная вытяжка почвы; 2 – распылитель (формирует аэрозоли); 3 – баллон с газом; 4 – светофильтр (пропускает излучение только определяемого элемента, а излучение других ионов, присутствующих в пробе задерживает), 5 – фотоэлемент: 6 – микроамперметр
Качественный анализ в методе проводится по:
1. Окраске перлов пламени (катионы 



 – фиолетовый,
– фиолетовый, 


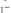


 – в зеленый);
– в зеленый);
2. По спектральным линиям.
Количественный анализ – по уравнению Ломакина:
143









 ,
,
где 
 – константа, связанная с режимом работы прибора
– константа, связанная с режимом работы прибора
(температура и высота пламени); в – константа, связанная с побочными процессами в пламени (ионизации и самопоглощения); С – концентрация определяемого компонента в пробе, моль/дм3.
4.Атомно-абсорбционный метод.
Метод основан – на способности атомов избирательного поглощения излучение определенных длин волн.
Аналитический сигнал метода – интенсивность светопоглощения (абсорбции света), А, мкА.
Качественный анализ – по линиям спектра.
Количественный анализ – по уравнению:







 ,
,
где к – коэффициент атомной абсорбции, b – ширина пламени,
С– концентрация ионов, моль/дм3,
Применяются: для определения катионов 




 ,
, 




 в почвах.
в почвах.
Лекция № 13 Законы светопоглощения. Аналитический сигнал метода.
Условия применения основного закона светопоглощения. Фотоэлектроколориметрия
Фотоколириметрический анализ (молекулярная абсорбционная спектроскопия) относится к оптическим методам анализа. Метод основан, на способности вещества поглощать электромагнитное излучение оптического диапазона. Оптический спектр включает ультрафиолетовую, видимую и ИКобласти. Наибольшее распространение получили фотометрические методы анализа, основанные на поглощении в видимой области спектра, в интервале длин
144

волн 400-780 нм. Излучения видимой области спектра поглощают только окрашенные соединения.
Фотометрический метод анализа широко применяют для решения проблем технологического контроля; в санитарногигиеническом анализе для определения аммиака, нитратов, катионов различных металлов в воде; для определения витаминов в продуктах питания. Метод имеет низкий предел обнаружения (10–5-10–6 М), относительная ошибка большинства определений 1-2 %.
В основе фотометрического метода анализа лежит избирательное поглощение света частицами (молекулами и ионами) вещества в растворе, при некоторых длинах волн светопоглощение происходит интенсивно, а при некоторых
свет не поглощается. Поглощение квантов
электромагнитного излучения оптического диапазона молекулой или ионом обусловлено переходом электронов на орбитали с более высокой энергией (рис. 21).
Цветность как способность к поглощению определенных квантов электромагнитного излучения оптического диапазона определяется электронным строением молекулы. Обычно это связано с наличием в молекуле хромофорных групп. Конкретные хромофорные группы обуславливают возможность осуществления определенных электронных переходов. Каждая молекула обладает определенным набором возбужденных квантовых состояний, отличающихся значением энергии, поэтому интенсивно поглощаются те кванты света, энергия которых равна энергии возбуждения молекулы. Характер поглощения зависит от природы вещества, на этом основан качественный анализ. Для количественного анализа используют зависимость светопоглощения от концентрации определяемого вещества. Аналитический сигнал метода фотоэлектроколориметрии – оптическая плотность раствора (А).
145

Рис. 21. Схема рассеивания излучения
Уменьшение интенсивности света, прошедшего через раствор, характеризуется коэффициентом пропускания (или просто пропусканием) Т:
где  и
и 

 - соответственно интенсивность света, прошедшего через раствор и растворитель.
- соответственно интенсивность света, прошедшего через раствор и растворитель.
Десятичный логарифм коэффициента светопропускания, взятый с обратным знаком, называется оптической плотностью А:
Уменьшение интенсивности при прохождении света через раствор подчиняется закону Бугера-Ламберта-Бера:
или:
или:
146

Основной закон светопоглощения – Закон Бугера- Ламберта-Бера: Слои вещества одинаковой толщины и концентрации при прочих равных условиях (длина волны,
температура) всегда поглощают одну и ту же часть светового потока. Математическая запись закона:

 – молярный коэффициент светопоглощения, см•моль/дм3; l
– молярный коэффициент светопоглощения, см•моль/дм3; l
– толщина светопоглощающего слоя, см; С – концентрация анализируемого компонента в пробе, моль/дм3.
Физический смысл молярного коэффициента поглощения сразу становится ясным, если мы принимаем С = 1 моль/л и l = 1 см, тогда А = ε. Следовательно, молярный коэффициент поглощения равен плотности одномолярного раствора при толщине слоя 1 см. Молярный коэффициент светопоглощения характеризует чувствительность реакции и является постоянной величиной для данного окрашенного соединения. Для повышения чувствительности определения
выбирают реакцию с максимальным значением 
 . Значение
. Значение 

для различных окрашенных соединений различны: для аква комплексов меди и других катионов 
 порядка 10, для
порядка 10, для
аммиакатов 
 = 102-103, для органических соединений
= 102-103, для органических соединений 
 = 104-
= 104-
105. Молярный коэффициент поглощения раствора можно рассчитать, если приготовить серию растворов с известными концентрациями веществ и измерить оптическую плотность раствора. Коэффициент линейной регрессии зависимости A = f(C) представляет собой молярный коэффициент поглощения. Количественное определение вещества по светопоглощению основано на применении закона Бугера-Ламберта-Бера.
Концентрацию можно определить, пользуясь: методом
градуировочного графика A = f(C), методом сравнения или методом добавок. Спектры поглощения одного и того е вещества в координатах А – λ имеют одинаковый вид независимо от толщины слоя раствора или концентрации вещества в растворе и характеризуется максимумом при
147
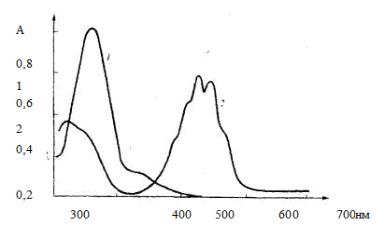
одной и той же длине волны, при которой и проводят все определения, рис. 22.
Рис. 22. Спектры поглощения водных растворов
дихромата и перманганата калия в области 300…700 нм ( l = 1см): 1 – водный 2,4•10–4 моль/дм3 раствор К2Сг2О7;
2 – водный 2,4•10–4 моль/дм3 раствор КМnО4
Для проведения фотометрических исследований необходимо соблюдать ряд условий:
Цветная реакция должна проходить быстро, избирательно, полностью и воспроизводимо, а окраска образующейся аналитической формы должна быть устойчивой во времени и к действию света;
Аналитический реагент вводят в количестве, достаточном для перевода всего определяемого вещества в аналитическую форму;
При проведении реакции выбирают такую область рН,
вкоторой небольшое изменения рН не влияют на светопоглощение, а оно при этом максимально;
Фотометрические измерения проводят в определенном интервале длин волн, при этом ориентируются на большее
148
различие в поглощении аналитической формы и исходных реагентов. Чем больше контрастность, тем удобнее реакция для фотометрирования;
Поглощение всегда измеряют относительно раствора сравнения, поглощение которого принимается за оптический ноль;
Погрешности фотометрических определений возникают вследствие неправильно проведенной химической реакции, использования грязных кювет, невоспроизводимости установки кювет в фотометрическом приборе и неточной настройкой его на оптический ноль, нестабильности работы источника сплошного излучения и оптической схемы, а также за счет погрешностей при построении градуировочного графика. Все эти погрешности относятся к систематическим ошибкам и их можно свести к минимуму при аккуратной работе.
Все фотометрические определения проводят по единой схеме:
Переведение пробы анализируемого вещества в раствор;
Получение окрашенной аналитической формы в результате проведения цветной реакции;
Измерение светопоглощения раствора аналитической формы;
Обработка полученных данных.
Измерение поглощения проводят с помощью фотоэлектроколориметров. Фотоэлектроколориметрия –
анализ на основе измерения поглощения нестрого
монохроматичного излучения. В видимой части спектра воспринимаемый цвет – результат поглощения веществом определенного участка сплошного спектра электромагнитного излучения (белого цвета). Цвет раствора всегда является дополнительным к цвету поглощенного излучения (табл. 23).
149
Цвет светофильтра является дополнительным к цвету раствора и соответствует участку спектра, который этим светофильтром пропускается.
Таблица 23 Наблюдаемые цвета и соответствующие им поглощенные
участки спектра
Интервал длин |
Цвет |
Наблюдаемый |
волн |
поглощенного |
цвет |
поглощенного |
излучения |
(дополнительный |
излучения, нм |
|
цвет) |
400 – 435 |
Фиолетовый |
Желто-зеленый |
435 – 480 |
Синий |
Желтый |
480 – 490 |
Голубой |
Оранжевый |
490 – 500 |
Голубовато- |
Красный |
|
зеленый |
|
500 – 560 |
Зеленый |
Пурпурный |
560 – 580 |
Желто-зеленый |
Фиолетовый |
580 – 595 |
Желтый |
Синий |
595 – 605 |
Оранжевый |
Голубой |
605 – 730 |
Красный |
Голубовато- |
|
|
зеленый |
730 – 760 |
Пурпурный |
Зеленый |
Регистрация аналитического сигнала осуществляется с помощью однолучевых или двухлучевых с компенсационной схемой фотоэлектроколориметров (ФЭК). Принципиальная схема двухлучевого ФЭКа представлена на рис. 23.
Условия применения и выполнения основного закона светопоглощения:
1. Свет, используемый в анализе должен быть монохроматическим (достигают с помощью монохроматоров, фильтров, дифракционных решеток, призм).
2. Необходимо установить характеристическую длину волны (по спектру поглощения).
150
