
Хенке_Жидкостная хроматография [2009]
.pdf
4.2. Эмульгаторы |
71 |
мало подвижной фазе (540 мл). Если потребуется выделить бóльшие количества сложного метилового эфира рициноловой кислоты, то такое же количество пробы можно впрыскивать несколько раз в 4 часовом цикле. Есть еще другая возможность за относительно короткое время получить больше вещества в пике 2, для этого по требовалось бы применение колонок с внутренним диаметром 100 мм. Количество пробы на каждое разделение потребовалось бы повысить на 66 г. Разделение пред ставлено на рис. 4.16. Были выбраны следующие условия разделения:
Колонка: |
1 м + 2 × 2 м, |
|
внутренний диаметр 25/26 мм |
Общая длина слоя геля: |
461 см |
Подвижная фаза/скорость: |
дихлорметан, 2 мл/мин |
Количество пробы: |
4125 мг примерно в 50 мл |
|
дихлорметана |
Сложный метиловый эфир пальмитиновой кислоты Сложный метиловый эфир стеариновой кислоты
Сложный метиловый эфир олеиновой кислоты 1731 мг Сложный метиловый эфир линолевой кислоты Сложный метиловый эфир линоленовой кислоты
Разделение через адсорбцию
tR, мин
Рис. 4.16. Избирательное препаративное выделение сложного метилового эфира рицинолевой кислоты из продукта переэтерификации с помощью ди хлорметана на Сефадексе LH 20
4.2. Эмульгаторы
Эмульгаторы – это поверхностно активные вещества, которые служат для снижения поверхностного натяжения воды благодаря своим физико химическим свойствам.
С помощью эмульгаторов нерастворимые вещества можно «солюбилизиро вать» в воде, т. е. делать их водорастворимыми. Поверхностно активные вещества
могут быть анион или катион активными, а также амфотерными или неионо
генными. В дальнейшем будут представлены неионогенные эмульгаторы класса производных полиоксиэтилена. Их применение в промышленном производстве очень распространено. Где используются поверхностно активные вещества?
•В фармацевтической промышленности для М/В (масло вода) эмульсий, например, чтобы «солюбилизировать» витамины или эфирные масла.
•Для приготовления прядильных препараций, которые служат для произ водства искусственных волокон из полимеров.

72 Глава 4. Примеры разделения из практики
•Для изготовления средств по уходу за телом (косметика), чтобы гарантиро вать качество и стабильность крема.
•В пищевой промышленности.
4.2.1. Полигликоль спирта
Этоксилированные виды спиртов, будь то с короткой или длинной цепью спирты жирного ряда, применяются в качестве неионогенных эмульгаторов в различных отраслях промышленности. Полигликоль спирта, как правило, состоит из несколь
ких компонентов.
Уже при этоксилировании чистого спирта жирного ряда, в зависимости от
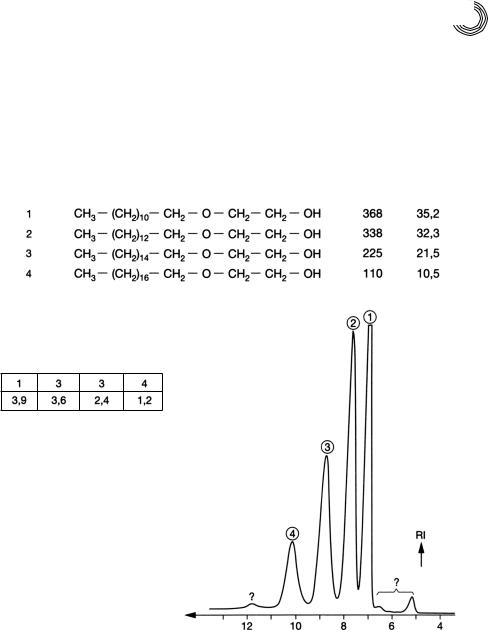
молярного соотношения, возникают продукты присоединения (аддукты) этиле ноксиды с различной степенью этоксилирования. Из лаурилового спирта и эти леноксида может возникнуть следующая смесь:
СН3–(СН2)10–СН2–О–(СН2–СН2–О)n–Н n = 1, 2, 3, 4, 5, 6, 7 и т.д.
Сувеличивающейся длиной единиц (–СН2–СН2–О–) полярность всех аддук тов ЭО (этиленоксида) уменьшается, так как влияние на молекулу полярной гид
роксильной функции становится все меньше с повышающейся длиной цепи. Смеси веществ с компонентами различной полярности можно разделить очень
просто и, тем не менее, эффективно на немодифицированном силикагеле с по мощью дихлорметана, а затем метанола в качестве элюента по возрастающей по лярности (см. раздел 5.4.1).
Спомощью дихлорметана элюируют компоненты с самой сильной гидрофоб ностью, а с помощью метанола с силикагеля десорбируются самые полярные со единения.
4.2.1.1. Полигликоль спирта кокосового масла
Предлагаемый этоксилат после вышеназванного ступенчатого элюирования дал следующий результат:
Количество пробы: |
4 г примерно в 40 мл дихлорметана |
Элюат дихлорметана: |
11,2% |
Элюат метанола: |
88,5% |
Этот простой способ разделения может быть применен для очень многих сме сей веществ независимо от того, являются ли они синтетического или природно го происхождения. С помощью этого метода можно сэкономить много труда на различных пробах, так как смеси веществ в комплексе можно предварительно раз делять по группам по возрастающей полярности, чтобы затем легче и быстрее мож
но было разделить отдельные фракции.
Для нынешнего времени, когда повсюду применяются компьютеры, очень
симптоматично, что такие простые методы, как названные, забываются. Простые и «более старые» методы оцениваются как «устаревшие» и признаются ошибочно
как неприменимые. Но и до сих пор лучшим решением является соединение оп равдавших себя методов с современными.
4.2. Эмульгаторы |
73 |
Для отделения элюата дихлорметана были проведены 3 предварительных раз деления (3 × 4 г), чтобы получить достаточное количество для отделения в препа ративном масштабе.
1050 мг остатка элюата дихлорметана были разделены на 6 готовых стеклян ных колонках Lobar® Lichroprep RP 8, размер В, фирмы Мерк с помощью мета нола (2 мл/мин). Результат этого разделения представлен на рис. 4.17.
Пик № |
|
мг |
% |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1…4: элюат метиленхлорида = 1041 мг
Вес в % в пересчете на пробу оригинала
ч
Рис. 4.17. Препаративное разделение среднеполярных компонентов полигликолей спирта кокосового масла на обращенной фазе С 8 чистым метанолом
Основное количество составляют, как видно из соотношения веса, лауриловый и миристиловый спирты, но есть и доли цетилового и стеарилового спиртов. Как возникают смеси этих спиртов жирного ряда? Как правило, через оксосинтез или посредством снижения соответствующей смеси кислоты жирного ряда. Разделение полигликоля спирта кокосового масла, а также обоих элюатов на Сефадексе LH 20
(5 метровая колонка) с помощью метанола показано на рис. 4.18. Несомненно, луч
шее разделение полигликоля жирного спирта на обращенной фазе С 8.
74 |
Глава 4. Примеры разделения из практики |
|
|
Пик № |
Молеку% |
|
лярный вес |
|
|
|
= 10, 12, 14 и 16 и *= 13 n n
А |
оригинальная проба |
1000 мг |
|
В |
элюат метанола |
885 мг |
88,5 вес в % |
С |
элюат дихлорметана |
112 мг |
11,2 вес в % |
Вода
ч
Вода
ч
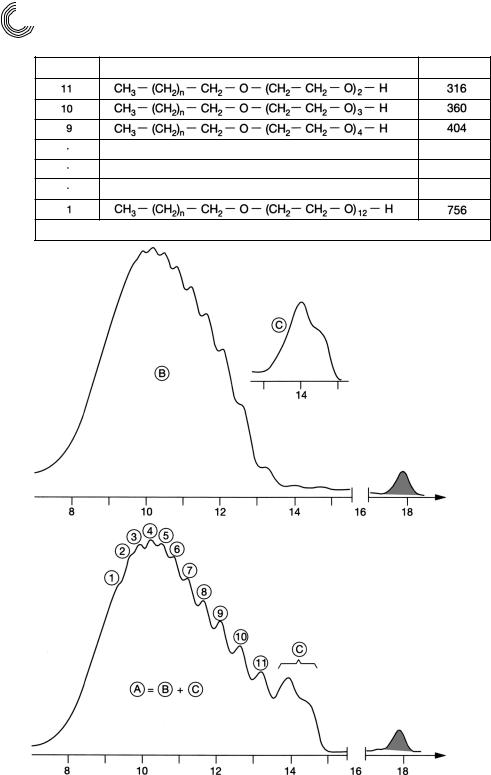
Рис. 4.18. Препаративное разделение среднего и более сильно полярного компонентов этоксилата спирта жирного ряда на Сефадексе LH 20 c помощью метанола

4.2. Эмульгаторы |
75 |
Разница молярной массы между пиком 11 и 10 составляет 12%, а пик 10 на 11% больше пика 9. В смысле обратного ситового эффекта 3 пика должны были разделиться количественно, то что это не так, можно объяснить следующим об разом: в каждом пике могут содержаться 4 вида спирта жирного ряда как соответ ствующий продукт присоединения ЭО, даже если в различном количестве. По молярным массам они отличаются на 2 (–СН2–) группы, и это ведет к расшире нию пика или к понижению степени разделения.
Очень важно перед ступенчатым элюированием на силикагеле определить содержание воды в пробе. Количество воды >1% дезактивирует силикагель и тем самым делает его непригодным для предварительного разделения.
4.2.1.2. Изотридеканолполигликоль
Анализу подвергался стандартный этоксилат изотридецилового спирта со сред
ней степенью этоксилирования 2 (–СН2–СН2–О–) группы (согласно данным изготовителя) на каждый жирный спирт. Изотридеканол – это синтетическая, мно гократно метил разветвленная смесь спирта С13, которая возникает из за одно временного присоединения монооксида углерода и водорода к смеси олефина при 180…200°С в присутствии катализатора кобальта. Эта реакция, протекающая под давлением известная как оксосинтез, при 100…115°С ведет к образованию аль
дегидов. При более высокой температуре реакция идет через гидрирование даль ше к соответствующим видам спирта. Так как продукты присоединения этокси лата состоят из нескольких компонентов, то и предлагаемая смесь может быть выделена дихлорметаном или метанолом с помощью ступенчатого элюирова ния (см. раздел 5.4) на силикагеле в более сильно гидрофобную и полярную фрак цию. Разделение без индикации, однако, количественная оценка через взвеши вание, дало следующий результат:
1.Элюат дихлорметана: 1216 мг = 30,4%.
2.Элюат метанола: 2784 мг = 69,6%.
Были разделены 4000 мг этоксилата. Это обычное количество пробы, которое разделяется на силикагелевом слое 25 × 350 мм. Чем выше доля элюата дихлорме тана, тем больше может быть количество пробы, но следует помнить, что это мо жет привести к перегрузке. Это неизбежно нанесло бы вред разделению.
При получении элюата дихлорметана было сделано интересное наблюдение,
которое дано в форме таблицы:
1. Фракция
Результат взвешивания СН2–Cl2
400 мл |
556 мг |
200 мл |
448 мг |
400 мл |
204 мг |
1208 мг
Затем еще раз прокачали 5 × 200 мл дихлорметана. Взвешивание отдельных
фракций элюата соответственно и остатков привело к следующему результату:

76 Глава 4. Примеры разделения из практики
2. Фракция
Результат взвешивания СН2–Cl2
200 мл |
100 |
мг |
200 мл |
35 |
мг |
200 мл |
26 |
мг |
200 мл |
12 |
мг |
200 мл |
5 |
мг |
|
|
|
|
178 |
мг |
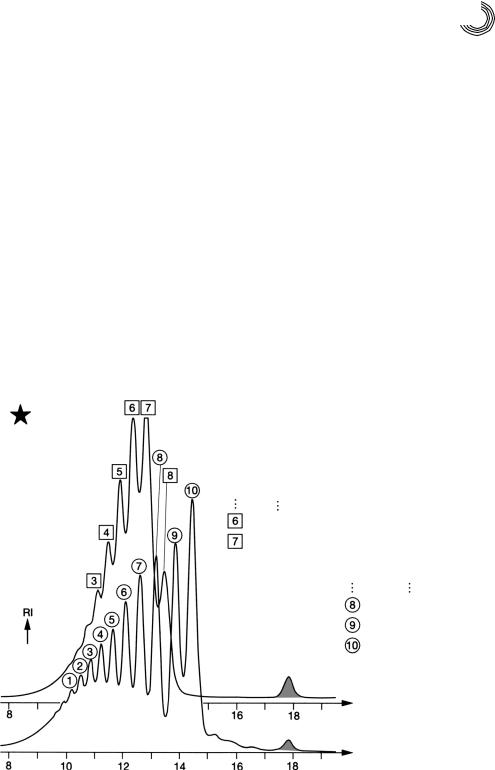
Интерес представлял состав обеих фракций. Половина первой фракции (605 мг) была элюирована метанолом на 5 метровой колонке Сефадекс LH 20. Результат представлен на рис. 4.19а. Пики, как отмечено, разрезаны в углублении и очищены путем впрыскивания со смещением времени и затем идентифицированы с помо
щью спектра 1Н ядерной магнитно резонансной спектроскопии. Смесь можно было бы с аналогичным успехом разделить и на обращенной фазе С 8. Вторая фракция была также подана на колонку Сефадекс LH 20, и результатом стал единственный пик (см. рис. 4.19б). Этот пик, другими словами это вещество, идентично пику пер вой фракции согласно спектру 1Н ядерной магнитно резонансной спектроскопии. Чистота пика легко объяснима. Элюирование первой фракции из силикагелевой колонки было прервано в пике 1 и остаток элюирован дихлорметаном 5 × 200 мл. Ближайшие более высокие компоненты с тремя и более (–СН2–СН2–О–) едини цами уже настолько полярные, что они не могут быть десорбированы дихлормета
ном вообще или только по прошествии длительного времени элюирования.
Колонка: |
1 м + 2 × 2 м, внутренний диаметр 25/26 мм |
Высота слоя геля: |
461 см |
Подвижная фаза/скорость: |
метанол, 2 мл/мин |
Количество пробы: |
а) 605 мг, б)178 мг |
CH13H27 (разветвленный по метильной группе) – ОН 556 мг
CH13H27 (разветвленный по метильной группе) – О – СН2 – СН2 – ОН 448 мг
178 мг
CH13H27 (разветвленный по метильной группе) – …..
….. – О – СН2 – СН2 – О – СН2 – СН2 – ОН 204 мг
ч |
ч |
Рис. 4.19. Препаративное разделение среднеполярных частей фракций полигликоля изотридеканола на Сефадексе LH 20 с помощью метанола: а) первая фракция; б) вторая фракция
4.2. Эмульгаторы |
77 |
С элюата метанола был выполнен только 1 спектр 1Н ядерной магнитно ре зонансной спектроскопии с результатом, что средняя степень этоксилирования составляет 4. Вследствие этого полярная часть фракций состоит из следующих компонентов (см. рис. 4.19):
CH13H27(разветвленный)–О–(–СН2–СН2–О)n–Н.
n = 3…5
4.2.1.3. Этоксилированные спирты
На хроматограммах рис. 4.20 представлено прямое сравнение 2 эмульгаторов поли
этиленгликоля спирта. После того как была представлена первая хроматограмма, бумажная лента самописца была вновь свернута и запущено элюирование второй
пробы на том же самом месте, как у первого этоксилата. Это сравнение должно было дать свидетельство о качестве обоих эмульгаторов. По кривой элюирования можно было уже признать, что это этоксилаты двух различных спиртов. Уже при использовании обоих эмульгаторов отчетливо просматривалась разница, т. е. пер вый продукт присоединения этиленоксида (внизу) не мог быть заменой второму этоксилату (вверху). Первый этоксилат с помощью спектра 1Н ядерной магнитно
Колонка: |
5 м*стандарт |
Наполнитель колонки: |
Сефадекс LH*20 |
Подвижная фаза/скорость: |
метанол в качестве элюента |
|
(2 мл/мин) |
Количество пробы: |
по 950 мг, растворенных |
|
примерно в 25 мл метанола |
Разветвленный спирт с 1 • ЭО |
|
с 3 • ЭО с 2 • ЭО (этиленоксид)
Эмульгаторы
1*додеканол • 2 • ЭО
1*додеканол • 1 • ЭО
1*додеканол
Вода < 1%
ч
Вода < 1%
ч
Рис. 4.20. Сравнительное разделение 2 этоксилированных спиртов на Сефадексе LH 20
78 Глава 4. Примеры разделения из практики
резонансной спектроскопии был идентифицирован как 1 додеканолполигликоль. Второй зарегистрированный над ним продукт присоединения этиленоксида невоз можно было точно идентифицировать. Согласно спектру 1Н ядерной магнитно ре зонансной спектроскопии компонент спирта короче С12 и к тому же разветвлен по метильной группе. Очень вероятно, что это смесь спиртов с изомерией положения. Были выбраны следующие условия разделения (см. рис. 4.20).
4.2.1.4. Эфир диэтиленгликольмоноцетила
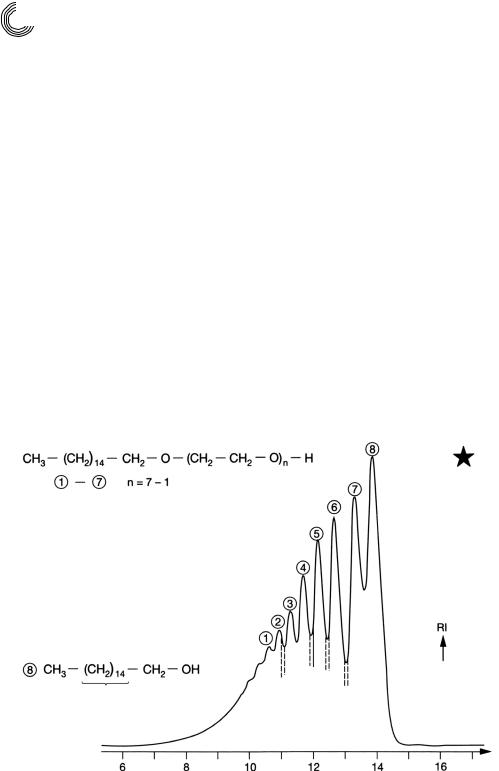
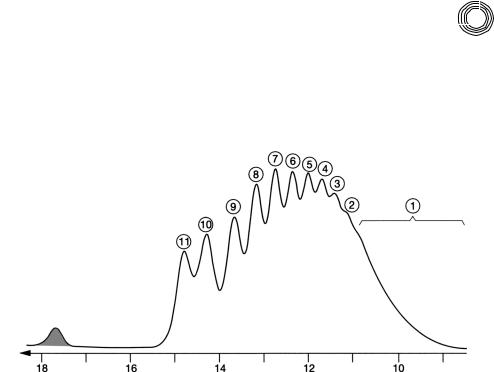
После препаративного гель хроматографического разделения пробы эфира ди этиленгликольмоноцетила (торговое имя Брий 52, с указанием качества чис тый) больше бы соответствовало обозначение полигликоль цетилового спирта (см. рис. 4.21).
Пик 8 по времени элюирования соответствует цетиловому спирту или 1 гек
садеканол, который также подтверждается анализом 1Н ядерной магнитно ре зонансной спектроскопии. Пики 4…7 срезаны на минимуме. При этом можно было отказаться от промежуточной фракции. Как это часто бывает в таких слу чаях, пики очистили впрыскиванием через определенные промежутки времени и идентифицировали с помощью спектров 1Н ядерной магнитно резонансной спектроскопии и FD/масс cпектрометрии. Результат также можно получить из
рис. 4.21. Как видно, доля эфира диэтиленгликольмоноцетила (пик 7) 16,3% весь ма скромная.
170 мг
Пик |
|
163 мг |
|
|
151 мг |
||
Колонка: |
1 м + 2 × 2 м, |
||
|
|||
|
внутренний диаметр 25/26 мм |
||
Наполнитель |
Сефадекс LH*20 |
120 мг |
|
колонки: |
|||
Высота |
461 см |
|
|
гелевого слоя: |
95 мг |
||
Подвижная фаза |
метанол, 2 мл/мин |
||
скорость: |
|
||
Количество пробы: |
1000 мг |
|
|
Правильнее было бы название: этоксилат цетилового спирта!
Цетиловый спирт или 1*гексадеканол
ч
Рис. 4.21. Препаративное разделение простого эфира «диэтиленгликоль» моноце тила на декстрангеле Сефадекс LH 20
|
|
|
4.2. Эмульгаторы |
79 |
|
Колонка: |
5 м*стандарт, внутренний диаметр 25/26 мм |
|
|
||
Наполнитель колонки: |
Сефадекс LH*20 |
|
|
|
|
Высота гелевого слоя: |
461 см |
|
|
|
|
Подвижная фаза/скорость: |
метанол, 2 мл/мин |
|
|
|
|
Количество пробы: |
950 мг этоксилат |
|
|
|
|
1…4 |
|
352 мг |
|
|
|
5 |
1*додеканол • 6 • ЭО |
73 мг |
|
|
|
6 |
1*додеканол • 5 • ЭО |
96 мг |
7 • ЭО |
|
|
7 |
1*додеканол • 4 • ЭО |
94 мг |
|
|
|
8 |
1*додеканол • 3 • ЭО |
99 мг |
8 • ЭО |
≥ 1 • ЭО |
|
9 |
1*додеканол • 2 • ЭО |
79 мг |
9 • ЭО |
|
|
|
|
|
|
|
|
|
1*додеканол • 1 • ЭО |
77 мг |
|
|
|
|
1*додеканол |
|
|
|
|
Вода
ч
Рис. 4.22. Препаративное разделение простого эфира «триэтиленгликоль» моно лаурила на Сефадекс LH 20
4.2.1.5. Эфир триэтиленгликольмонолаурила
То, что данные стандартного продукта не всегда должны совпадать с фактическим составом, мы могли еще раз установить. Препаративное гель хроматографическое разделение метанолом на 5 метровой колонке Сефадекс LH 20 показывает, что эфир триэтиленгликольмонолаурила (торговое имя Брий 30) представляет собой комп лексную смесь, как видно из хроматограммы на рис. 4.22. И в этом случае пики 5…11 для идентификации почистили оправдавшим себя методом, т. е. разрезали и прове ли впрыскивание через определенные промежутки времени (со смещением време ни). Идентификация проводилась также с помощью спектров и данных 1Н ядер ной магнитно резонансной спектроскопии и FD/масс cпектрометрии. Для этого продукта правильнее было бы название ПЭГ 400 эфира монолаурила. Пики с бо
лее высокой степенью этоксилиривания (1…4) не были идентифицированы, но их размещение не должно быть проблематичным. В идентифицированных пиках про
дукт присоединения тетрадеканол ЭО был подтвержден, но не идентифицирован. Неудовлетворительное отделение по сравнению с эфиром диэтиленгликольмоно цетила является результатом загрязнения 1 додеканола через 1 тетрадеканол. Это ведет к расширению пика и, как следствие, сниженной степени разделения.
4.2.1.6. Полигликоль 1,6 гександиола
Сложные эфиры кислот жирного ряда этоксилированного 1,6 гександиола, как и
другие продукты присоединения ЭО, применяются в различных отраслях промыш ленности в качестве эмульгаторов.
80 Глава 4. Примеры разделения из практики
Для качественного и количественного анализа пробы сложного эфира в распо ряжении было небольшое количество экстракта дихлорметана. Вначале у экстракта был сделан спектр 1Н ядерной магнитно резонансной спектроскопии. Из него мож но было узнать, что, вероятно, это смесь сложных эфиров дилауриновой кислоты
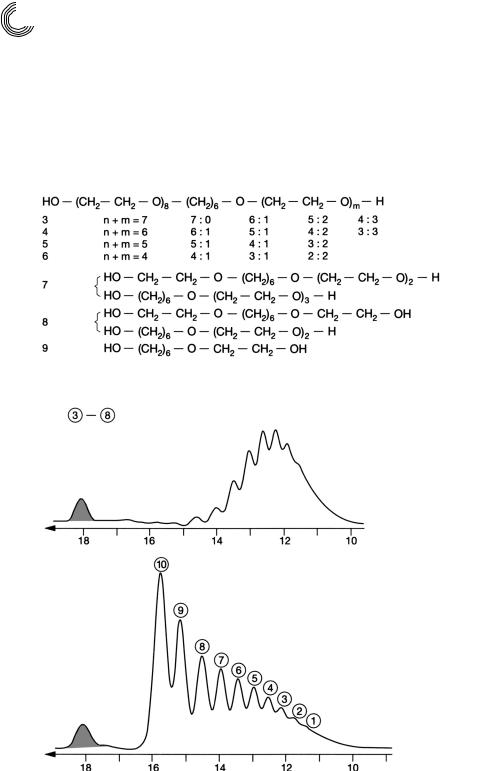
В соответствии со спектром 1Н*ядерной магнитно*резонансной спектроскопии и FD/масс*cпектрометрии пики 3…8 состоят из изомеров положения!
Возможные присоединения этиленоксида к 1,6*гександиолу:
симметрично
асимметрично
Количество пробы: 350 мг Молярное соотношение: 1 : 2
Согласно 1Н*ядерной магнитно*резонансной спектроскопии и FD/масс*cпектрометрии пики состоят из изомеров положения!
Вода |
800 мг |
|
ПЭГ 400 |
||
|
ч
1,6*гександиол
Вода
ч
Рис. 4.23. Препаративное гель хроматографическое разделение этоксилированного 1,6 гександиола
