
- •Содержание
- •Введение
- •1. Аналитический обзор и патентный поиск
- •2. Выбор и технико-экономическое обоснование проектных решений
- •3. Стандартизация
- •4. Технологическая часть
- •4.1. Теоретические основы процесса
- •4.2. Характеристика сырья и готового продукта
- •Характеристика сырья, материалов, полупродуктов и энергоресурсов [8]
- •4.3. Описание технологической схемы Получение раствора нитрата магния (магнезиальной добавки)
- •Нейтрализация азотной кислоты газообразным аммиаком с получением растворов аммиачной селитры
- •Упаривание полученного раствора аммиачной селитры до состояния высококонцентрированного плава и перекачивание плава наверх грануляционной башни
- •Гранулирование плава амселитры с последующим охлаждением гранул
- •Очистка отработанного воздуха, выбрасываемого в атмосферу
- •4.4. Расчеты химико-технологических процессов
- •4.4.1. Расчеты материальных балансов
- •4.4.1.1.Материальный баланс приготовления магнезиальной добавки с использованием магнезита
- •4.4.1.2.Материальный баланс приготовления магнезиальной добавки с использованием брусита
- •4.4.1.3.Материальный баланс процесса нейтрализации
- •4.4.1.4.Материальный баланс процесса донейтрализации
- •4.4.1.5.Материальный баланс процесса упаривания
- •4.4.1.6.Материальный баланс процесса кристаллизации
- •4.4.2 Расчеты тепловых балансов
- •4.4.2.1.Тепловой баланс приготовления магнезиальной добавки с использованием магнезита
- •4.4.2.2.Тепловой баланс приготовления магнезиальной добавки с использованием брусита
- •4.4.2.3.Тепловой баланс процесса нейтрализации
- •4.4.2.4.Тепловой баланс процесса донейтрализации
- •4.4.2.5.Тепловой баланс процесса упаривания
- •4.4.2.6.Тепловой баланс процесса кристаллизации
- •4.5. Выбор и расчет основного и вспомогательного оборудования Конструктивный расчет аппарата итн Расчет реакционной части
- •Расчет сепарационной части
- •4.6. Аналитический контроль [8]
- •5. Автоматизация и асуп [8]
- •6. Охрана труда и окружающей среды
- •6.1. Анализ степени опасности технологического процесса
- •6.2.2. Оценка уровня загрязнения воздушной среды вредными веществами
- •6.2.3 Выбор и расчет системы вентиляции
- •6.2.4 Оценка степени воздействия выбросов вредных веществ на окружающую среду
- •6.2.5 Оценка степени воздействия проектных решений на водные объекты
- •6.2.6 Отходы производства
- •6.2.7 Платежи за загрязнение окружающей среды
- •6.3. Оценка взрывопожарной и пожарной опасности Пожарная профилактика
- •6.4. Санитарно-гигиенические требования к выбору систем освещения
- •6.5. Обеспечение безопасного обслуживания – источника физического фактора воздействия
- •6.6. Электробезопасность
- •7. Экономическая оценка принятых проектных решений
- •7.1 Расчет текущих производственных издержек
- •7.2. Условно-годовая экономия и годовой экономический эффект
- •Заключение
4.4.2.6.Тепловой баланс процесса кристаллизации
Приход
1. Тепло, приходящее с 99,7%-м плавом аммиачной селитры:
QАС = (сNH4NO3·nNH4NO3 + сMg(NO3)2·n Mg(NO3)2 + cH2O·nH2O)· tвх,
tвх = 170ºС
Теплоемкости компонентов рассчитываем для данной температуры аммиачной селитры, используя температурные ряды [9]
сNH4NO3 = 139,3 Дж/моль·К
сMg(NO3)2 = 141,9 Дж/моль·К
cH2O = 39,02 + 0,07664·(170+273) + (11,96·105/(170+273)2) = 79,06 Дж/моль·К
QАС = (16162,5·139,3 + 232,9·141,9 + 166,6·78,1)·443 = 1,02·106 кДж
2. Тепло, приходящее с воздухом:
QВ = G·c·tвоз = 2133801,00535 = 7,5·106 кДж/ч,
где G – количество поступающего воздуха, кг/ч
с – удельная теплоемкость воздуха, кДж/(кгС)
tвоз. – температура воздуха, С
3. Тепло, выделяющееся при кристаллизации, т.е. превращение расплавленной соли в кристаллическую модификацию III, стабильную в пределах 32,3-84,2С
70,25 + 51,28 + 17,47 = 139 кДж/кг,
где 70,25; 51,28; 17,47 – теплоты превращения: Плав I, I II, II III соответственно, кДж/кг
При заданной нагрузке количество тепла, выделяющееся при кристаллизации, составит:
QКр. = 1,3·106139 = 1,8·108 кДж/ч
Расход
1. Тепло, уходящее с кристаллическим продуктом:
QКП = (сNH4NO3·nNH4NO3 + сMg(NO3)2·n Mg(NO3)2 + cH2O·nH2O)· tвых,
tвых =60ºС
Теплоемкости компонентов рассчитываем для данной температуры аммиачной селитры, используя температурные ряды [9]
сNH4NO3 = 139,3 Дж/моль·К
сMg(NO3)2 = 141,9 Дж/моль·К
cH2O = 39,02 + 0,07664·(60+273) + (11,96·105/(60+273)2) = 75,32 Дж/моль·К
QКП = (15500·139,3 + 232,9·141,9 + 213,3·75,32)·443 = 7,32·105 кДж
2. Тепло, расходуемое на испарение воды:
Qисп. = G·r = 28,4·2262,6 = 64257 кДж/ч
где G – количество влаги, испаряемой из плава при грануляции, кг/ч
r – теплота парообразования при абсолютном давлении 1 кгс/см2, кДж/кг
3. Тепло, уходящее с воздухом:
QВ = G·c·tвоз = 213417,41,00575 = 1,6·107 кДж/ч
Сводим тепловой баланс в таблицу:
Таблица 4.4.2.10
Приход |
Расход |
||
Статья прихода |
Q, Дж |
Статья расхода |
Q, Дж |
Тепло с плавом аммиачной селитры |
1,02·106 |
Тепло с кристаллическим продуктом |
7,32·105 |
Тепло с воздухом |
7,5·106 |
Тепло,расходуемое на испарение воды |
64257 |
Тепло,выделяющееся при кристаллизации |
1,8·108 |
Тепло с воздухом |
1,6·107 |
Всего |
1,8·108 |
Всего |
1,7·108 |
4.5. Выбор и расчет основного и вспомогательного оборудования Конструктивный расчет аппарата итн Расчет реакционной части
1) Сечение реакционного стакана:
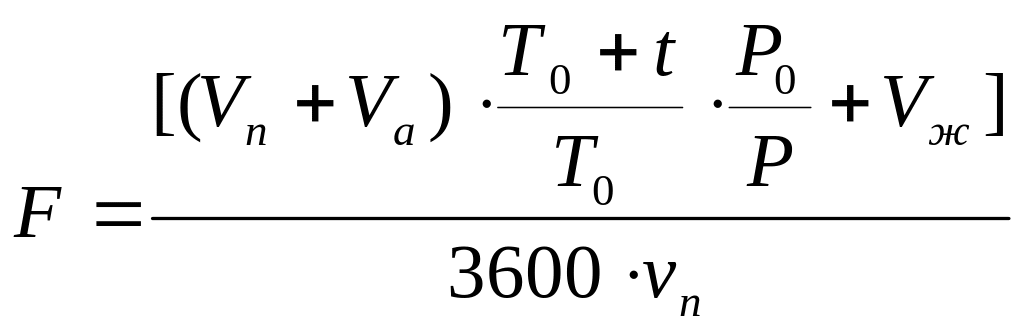 (4.5.1)
(4.5.1)
где Vп – объем водяного пара, образующегося в реакторе, м3/ч;
Vа – объем аммиака, м3/ч:
Т0 = 273 К, Р0 = 105 Па;
t = 160 ºС – температура в аппарате, ºС;
vп – скорость парожидкостной смеси, м/c.
Из материального баланса:
mп = 34508,5 кг/ч;
mам = 12183,6 кг/ч;
mр-ра = 63111,1 кг/ч
Vп = mп22,4 / Мп = 34508,5 22,4 / 18 = 42943,9 м3/ч
Vам = mам22,4 / Мам = 12183,6 22,4 / 17 = 16053,7 м3/ч
Vр-ра = mр-ра /р-ра = 63111,1 / 1700 = 37,3 м3/ч
Принимаем, что vп = 9,0 м/с
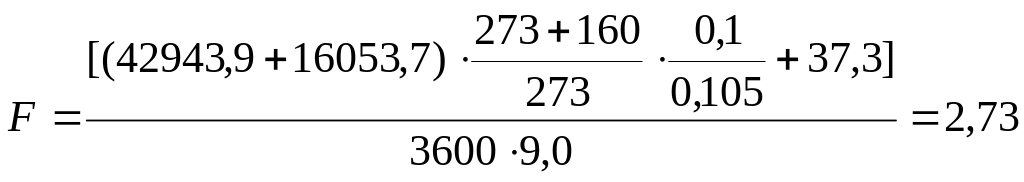 м2
м2
2) Диаметр реакционного стакана:
![]() м
(4.5.2)
м
(4.5.2)
Рабочая скорость wп = 8,96 м/с
Время пребывания смеси в реакционном стакане = 0,5 - 1 с
Принимаем = 0,51 с
3) Длина реакционного стакана:
L = vп = 0,518,96 = 4,57 м (4.5.3)
Принимаем длину реакционного стакана L = 4,6 м
4) Пересчитаем время:
= L / Vп = 4,6 / 8,96 = 0,513 с
